- 无机物的推断
- 共127题
下列各组物质中,物质之间通过一步反应就能实现图示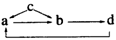
正确答案
解析
略
知识点
某酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。实验室用下图模拟工艺流程,利用常用的酸、碱和废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
(1)甲的化学式是 ,乙的化学式是 , G 的化学式是 。
(2)过程Ⅰ中共发生了 个化学反应,写出其中不属于置换反应的离子方程式 。
(3)过程Ⅰ、Ⅱ、Ⅲ、Ⅳ中均进行的实验操作的名称是 。
(4)过程Ⅱ中加入稀硫酸的目的是 。
(5)由A生成D的实验现象是 。
(6)由D生产铁红的化学方程式是 。
正确答案
见解析。
解析
(1)Fe HNO3 CuO
(2)4 2Fe3++Fe=3Fe2+
(3)过滤
(4)除去过程Ⅰ中加入的过量铁粉;使Fe2+循环利用
(5)生成白色絮状沉淀迅速变成灰绿色,最终变成红褐色
(6)
知识点
已知一定条件下A、B、C、D之间的转化关系如图所示。下列说法正确的是

正确答案
解析
略
知识点
由短周期前10号元素组成的物质T和X,如下图所示的转化(图中球与球之间连线代表化学键单键或双键)。X不稳定,易分解。为使得下列转化能够成功进行,方框内不可能加入的反应试剂是
正确答案
解析
略
知识点
下图表示从固体混合物中分离X的两种方案,请根据方案1和方案2指出下列说法合理的是
正确答案
解析
略
知识点
下表中各组物质之间不能通过一步反应实现下图转化的是
正确答案
解析
略
知识点
(1)A为用惰性电极电解饱和食盐水(含少量Ca2+、Mg2+)的装置。
①电解一段时间后,B中出现浑浊现象,请用离子方程式表示原因 。
此时电极a附近的现象为 ,因此工业上电解所用的食盐水需精制。
②随反应的进行,C中溶液红色褪去,主要原因有两种可能。请按要求填写表格。
(2)电解饱和食盐水所得气体X,可应用于提取溴单质。现有流程图如下:
请回答:
① 气体X的化学式为 ,反应II的化学方程式为 。
② 在母液苦卤中含有较多的NaCl、KCl、MgCl2、MgSO4等物质。用沉淀法测定苦卤中镁元素的含量(g/L),实验过程中应测定的数据有 。
③ 电解200kg 质量分数为25%的饱和食盐水,当浓度下降到20%时,收集到氯气的物质的量为 (溶于溶液中的氯气忽略不计,计算结果保留一位小数) 。
正确答案
见解析。
解析
(1) ① Cl2 + S2-= 2Cl-+ S↓
有无色气泡产生,溶液出现浑浊
②
(2) ① Cl2
SO2+Br2+2H2O=2HBr+H2SO4
② 苦卤样品的体积、Mg(OH)2沉淀的质量
③ 97.7 mol
知识点
酒石酸是某种降压药物的载体,可用1,3-丁二烯为原料合成,其流程如下:
已知:①
② D的分子组成是C4H8O2Cl2 ,核磁共振氢谱显示其有三个峰。
(1)D中所含官能团的名称是 。
(2)C转化为D的反应类型是 。
(3)B存在顺反异构,它的顺式结构式是 。
(4)D转化为E的化学反应方程式是 。
(5)与C组成相同、属于酯类、能发生银镜反应的有机化合物的结构简式 。
(6)F转化为G的化学反应方程式是 。
(7)F与乙二醇在一定条件下可以发生缩聚反应,该反应的化学方程式是___________。
(8)欲得到较纯净的酒石酸,需将G从其溶液中分离提纯,查阅相关资料得知G的溶解度受温度影响较大,则分离提纯G的方法是 。
正确答案
见解析。
解析
(1) 羟基、氯原子
(2) 加成反应
(3)
(4)
(5)
(6)
(7)
(8)重结晶
知识点
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图。请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素在元素周期表中的位置为__________,向水中加入X物质,X对水的电离平衡的影响是__________填“促进”、“抑制”或“无影响”) 。
②A与C的水溶液混合后生成B反应的离子方程式为__________。
(2)若A为固态非金属单质,A与X同周期,同时A在X中燃烧,产生白色烟雾,常温常压下C为白色固体,B分子中各原子最外层均为8电子结构。
①若A为该元素的白色固体单质,则1mol A单质中含共价键数目为 NA ,B的电子式为__________。
②X与水反应的离子方程式为__________。
(3)若A、B、C的焰色反应呈黄色,水溶液均为碱性,常温下,X为气态酸性氧化物。
①A中所含有的化学键类型是__________。
②C溶液中离子浓度由小到大的顺序是__________。
正确答案
(1)①第三周期IIIA族;抑制;②3[Al(OH)4]-+ Al3+=4Al(OH)3↓
(2)①6;PCl3(电子式略);② Cl2+H2O= H++Cl-+ HClO
(3)离子键、共价键;C(CO32-)<C(H+)<C(OH-)<C(HCO3-)<C(Na+)
解析
略。
知识点
下图是一些重要工业生产的转化关系(反应条件略去):
请完成下列问题:
(1)若D是单质,且与A属于同一主族,反应在高温下进行,则:
①此反应的化学方程式是 。
②D单质的一种重要用途是 。
(2)若B为黄色固体,D为固体化合物,则该反应为4FeS2+11O2 
①当有1molC生成时,该反应转移电子的总数是 。
②将C通入足量的酸性KMnO4 溶液中,发生反应的离子方程式为 。
(3)若B是一种碱性气体,D为化合物,则:
①该反应的化学方程式是 。
②B在加热条件下与CuO反应有Cu生成,该反应的化学方程式为 ;有人提出产物Cu中可能还含有Cu2O。已知Cu+在酸性溶液中不能稳定存在,为验证Cu2O是否存在,可取少量反应产物,滴加足量稀硫酸,若溶液由无色变为蓝色,则证明含有Cu2O。请写出发生反应的化学方程式:_________。
正确答案
(1)①2C+SiO2 
(2)①3.31×1024
②2MnO4-+5SO2+ 2H2O ===2Mn2++5SO42- +4H+
(3)①4NH3+5O2 
②2NH3+3CuO
解析
略
知识点
扫码查看完整答案与解析

























