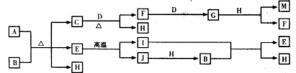- 无机物的推断
- 共127题
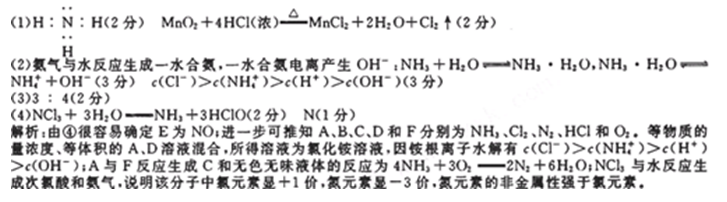
26.已知A~G有如图所示的转化关系(部分生成物已略去),其中A、G为单质,D是能使湿润的红色石蕊试纸变蓝色的气体,E、F均能与NaOH溶液反应。
请回答下列问题:
(1)写出F的电子式:( )
(2)①C溶液与D反应的离子方程式为( )
②F溶液与NaOH溶液共热反应的化学方程式为( )
(3)①C溶液显 ( )(填“酸性”、“中性”或“碱性”),理由是( )(用离子方程式解释)
②F溶液中离子浓度由大到小的顺序为( )
(4)将5.4gA投入200mL 2.0mol/L某溶液中有G单质产生,且充分反应后有金属剩余,则该溶液可能是 ( )(填代号)
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
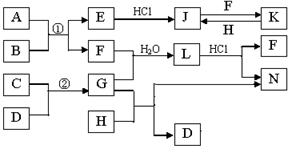
28.下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。已知:E为红棕色固体,K为浅绿色溶液;反应①②是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为极易溶于水且易液化.
(1)化合物A中含有的短周期元素是 (写元素符号),E的化学式_______。
(2)如何检验化合物N中的阳离子 ( ) 。
(3)写出J与F反应的离子方程式:( ),G与H反应的化学方程式:( )。
(4)等物质的量F和H的混合气体通入品红溶液中的现象为( ),原因是(用化学反应方程式表示)( ) 。
(5)已知C与D反应生成1.7g G 时放出4.26kJ的热量,则该反应的热化学方程式为 ( )。
正确答案
(1)S ; Fe2O3
(2)取少量样品于试管中,加水溶解,滴加NaOH浓溶液后加热,将湿润的红色石蕊试纸置于管口附近,试纸变蓝,则说明有NH4+
(3)2Fe3++ Fe =3Fe2+ ; 8NH3+3Cl2=6NH4Cl+N2
(4)品红溶液褪色 ; SO2+Cl2+2H2O=H2SO4+2HCl
(5)N2(g)+3H2(g)=2NH3(g) △H=-85.2kJ/mol
解析
解析已在路上飞奔,马上就到!
知识点
10.已知G是一种具有和卤素单质相似的直线型分子,J是一种角型分子,G和J按物质的量之比1:1反应后生成直线型分子L和分子M(组成G、J、L、M的原子序数均小于10)。分析图示,指出下列判断中错误的选项是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
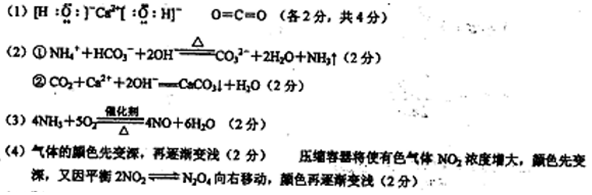
29.已知A为酸式盐,B为某二价主族金属元素(其原子序数不超过20)的化合物,常温常压下C、D、F、G、I均呈气态,H为无色液体。等物质酌量的A、B充分混合后加热能恰好完全反应(如下图所示),E的相对分子质量为100,G是红棕色气体,C气体可使湿润的红色石蕊试纸变为蓝色。图中反应条件(除加热外)均已略去。
(1)写出B的电子式______________,I的结构式______________。
(2)写出下列反应的离子方程式:①向A溶液中加入过量的NaOH溶液,并加热___________。 ②将少量的气体I通入B溶液中_____________________。
(3)写出C和D反应的化学方程式_____________________。
(4)若对盛有气体G的密闭容器(带可移动的活塞)进行压缩操作,产生的现象是_______,原因是___________________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28. A、B、C、D、E是由短周期元素组成的六种常见物质。已知:
①常温下均呈气态,其中B、C、F为单质;
②实验室制取B时,用排饱和食盐水法收集可减少B的水中的溶解;
③A与B反应生成C和D,A的水溶液呈碱性,D的水溶液呈酸性;
④C与F在放电条件下反应生成E,E遇空气变色。
回答下列问题:
(1)A的电子式是( ),实验室制取B的化学方程式为( ) 。
(2)A的水溶液呈碱性的原因是( )(结合化学用语说明),将等物质的量浓度、等体积的A、D溶液混合,所得溶液中离子浓度由大到小依次排列为( ) 。
(3)一定条件下A与F反应可生成C和一种无色无味液体,该反应中氧化剂与还原剂的物质的量之比为( )。
(4)组成C、B两物质的元素,按原子个数1:3形成化合物G,G是一种淡黄色液体,遇水即发生水解可生成一种具有漂白性的物质,写出反应的方程式 ( );该反应说明组成C、B两物质的元素中非金属性较强的是 ( )。(填元素符号)
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析