- 无机物的推断
- 共127题
26.(15分)下图是A~Z在一定条件下的转化关系(部分反应物或产物未列出)。其中,A是生活中广泛使用的金属单质,常温下B是一种常见液体化合物,E、F、X均为气体。物质Y和Na2AO4均有强氧化性,可用于杀菌消毒,Z是一种红褐色固体。
请回答下列问题:
(1)Y的电子式为 ( );A元素在元素周期表中的位置 ( )
反应①的化学方程式是 ( )
(2)在①~⑧中属于氧化还原反应,但又不是化合反应的是 ( )(填序号)
(3)将Y和M的溶液混合后的现象是 ( )
(4)反应⑤的离子方程式是 ( )
(5)若在反应④中转移电子数为2NA,则消耗的F在标准状况下的体积是 ( ) L。
(6)反应⑧的化学方程式是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.已知A、B为单质,C为化合物。能实现上述转化关系的是( )
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
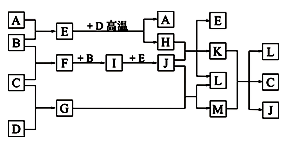
26.如图,常温下单质A、B为气体,单质C为固体,它们依次分别由短周期元素甲、乙、丙组成,甲元素原子核外电子数等于其电子层数,乙、丙同主族;E常温下为液体,G、H为黑色固体,D是常见金属(反应条件多数略去)。
回答下列问题:
(1)化合物E的沸点高于化合M的沸点,原因是( )。
(2)甲、乙两种元素可以形成两种化合物,其中一种化合物含有4个原子核,该化合物的结构式为( )。
(3)E与D高温反应的化学方程式为 ( ) 。
K与M在水溶液中反应的离子方程式为( )。
(4)实验室在保存L溶液时,需加入少量D,理由是( ) 。实验室检验L水溶液中的阳离子的方法是 ( )。
(5)已知一定条件下,每1 mol F与单质B完全反应生成I放出热量98.0 kJ,若2 mol F与1 mol B在此条件下发生反应,达平衡时,放出热量为176.4 kJ,则F的转化率为( )。若保持温度和压强不变(反应混合物都为气体)按下列四种配比作为起始物质充入,达到平衡时各物质的物质的量与上述平衡状态相同的是( )。
① 4 mol F、2 mol B ② 2 mol F、2 mol B、2 mol I
③ 1 mol F、0.5 mol B、1 mol I ④ 3 mol I、1mol Ne
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.A、B、C、D、E、F六种化合物。其中A、B、C、D、E均由短周期元素组成,焰色反应均呈黄色,B、C、E均由三种元素组成,B、C的组成元素相同,且C的摩尔质量比B大80g/mol请回答下列问题:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为( )(填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(2)下表为B与F实验的部分内容:
写出B与稀H2S04反应的离子方程式:( );
写出②中反应的化学方程式:( )。
(3)现由6种粒子Mn2+、MnO4一、H十、H2 0、X2Y82一(C中含有的阴离子)、XY42一完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4一需氧化剂的物质的量为( )。
(4)化合物D和E可以相互转化:
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.(12分)有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D、F均为常见金属元素。A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。下图中均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应,均含F元素的乙(单质)、丙、丁微粒间(均为无毒离子)的转化全为氧化还原反应。
请回答下列问题:
(1)化合物甲的电子式为( )。
(2)F元素在周期表中的位置( );化合物A2C的稳定性( )(填“大于”、“小于”或“等于”)A2E。
(3)均含有D元素的乙与丁在溶液中发生反应的离子方程式( )。
(4)丙、丁分别是含F元素的简单阳离子,检验含丙丁两种离子的混合溶液中的低价离子,可以用酸性KMnO4溶液,其对应的离子方程式为:( )
(5)已知常温下化合物FE的Ksp=6×10-18,常温下将1.0×10-5mol·L-1的Na2S溶液与含FSO4溶液等体积混合,若有沉淀FE生成,则所需的FSO4的最小浓度为 ( )。(忽略混合后溶液的体积变化)
正确答案
(1)
(2)第四周期第VIII族 ,(2分)大于(2分)
(3)Al3++3AlO2-+6H2O=4Al(OH)3↓(2分)
(4)5Fe2+ + MnO4- + 8H+ = 5Fe3+ + Mn2+ + 4H2O(2分)
(5)2.4×10-12 mol·L-1(2分)
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析