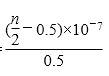- 海水资源及其综合利用
- 共118题
11.下列说法正确的是()
正确答案
解析
A、在电解池中,阴极被保护,阳极被腐蚀,故可以将船体做电解池的阴极,锌做电解池的阳极,故锌需要定期更换,故A正确;B、催化剂不能使平衡移动,故使用高效的催化剂平衡不移动,则原料的转化率不能改变,故B错误;C、将图中的活塞快速推至A处,则气体的浓度瞬间增大,故颜色瞬间变深,但由于增大压强后平衡2NO2⇌N2O4右移,故颜色又逐渐变浅,但由于平衡的移动只能减弱改变,故颜色变浅后还是比原来的深,故C正确;D、等体积、等浓度NaOH溶液和CH3COOH溶液混合后所得的溶液为醋酸钠溶液,醋酸钠是强碱弱酸盐,水解显碱性,故pH>7,故D错误.
故选AC
考查方向
解题思路
A、在电解池中,阴极被保护,阳极被腐蚀;B、催化剂不能使平衡移动;C、改变影响平衡的一个条件,平衡向能够减弱这种改变的方向移动;D、等体积、等浓度NaOH溶液和CH3COOH溶液混合后所得的溶液为醋酸钠溶液.
易错点
可逆反应规律
知识点
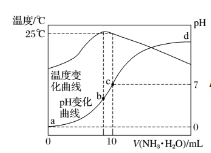
13.在某温度时,将n mol·L-1氨水滴入10 mL 1.0 mol·L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法正确的是( )
正确答案
解析
A.如果n=1,当体积为10ml时两者恰好完全反应生成氯化铵,是强酸弱碱盐水解呈碱性;
B.b点时溶液温度最高,说明氨水与盐酸恰好反应,则b点溶质为氯化铵,铵根离子促进了水的电离,则此时水的电离程度最大;由于d点溶液pH未知,则无法判断a.d两点水的电离程度大小;
C.c点溶液呈中性,所以c(H+)=c(OH-),由电荷守恒分析解答;
D.25℃时溶液的pH=7,则c(H+)=c(OH-)=10-7 mol•L-1,c(NH4+)=c(Cl-)=0.05mol/L,根据物料守恒可知:c(NH3•H2O)=(0.5n-0.05)mol/L,然后结合铵根离子的水解平衡常数表达式计算。
考查方向
解题思路
结合题干和选项对图进行细致的分析
易错点
准确分析图
知识点
10.某浓差电池的原理示意如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。下列有关该电池的说法正确的是()
正确答案
解析
A.生成氯气的Y极发生氧化反应,为负极,电子由Y极通过外电路移向X极,故A错误;B.电池工作时,Li+向正极移动,故B错误;C.在X极上生成氢气,发生还原反应,电极方程式为2H++2e-═H2↑,故C错误;D.Y极每生成1 mol Cl2,则转移2mol电子,有2molLi+向正极移动,则a区得到2 mol LiCl,故D正确。
故选D
考查方向
解题思路
加入稀盐酸,在X极上生成氢气,发生还原反应,电极方程式为2H++2e-═H2↑,为正极反应,Y极生成Cl2,为负极反应,发生Cl--2e-=Cl2↑,以此解答该题.
易错点
正负极易混淆,正负极反应方程式的书写不准确
知识点
5.下表是3种物质在水中的溶解度(20 ℃),下列说法中正确的是()
正确答案
解析
A.有含有固体MgCO3的溶液中,c(Mg2+)不等c(CO32-),因为碳酸根离子是弱酸根离子,在水中要水解 ,错误;B.除去粗盐中含有的MgCl2杂质,最佳除杂试剂为NaOH溶液,如果用 Na2CO3溶液,会引进碳酸根离子,错误; C.MgCl2+2H2O Mg(OH)2+2HCl,加热MgCl2溶液,平衡向右移动,最后打破平衡,蒸干后得到Mg(OH)2,灼烧Mg(OH)2,Mg(OH)2分解得到MgO,MgCO3+2H2O Mg(OH)2+H2CO3,加热MgCO3溶液,平衡向右移动,最后打破平衡,蒸干后得到Mg(OH)2,灼烧后,也得到MgO,故三者最终的固体产物相同,正确;D.不会生成MgCO3沉淀,MgCO3在碱性环境下不能稳定存在,错误。
考查方向
解题思路
举一反三,仔细审题,大概分析实验过程以此解题
易错点
概念模糊而导致计算错误,实验方法记忆不准确,
知识点
【化学——选修2化学与技术】
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
19.为提高锌灰的浸取率,可采用的方法是 (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
20.步骤Ⅱ所得滤渣中的物质是 (写化学式)。
21.步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________。
22.步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ,
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为_______________________________;
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是 。
23.若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
正确答案
①②③⑤
解析
①研磨 ②多次浸取 ③升高温度 ⑤搅拌均可提高锌灰的浸取率
考查方向
解题思路
工业生产流程方程式
易错点
工业生产流程的理解和分析
正确答案
Fe(OH)3、ZnCO3
解析
由流程图可知滤渣物质为Fe(OH)3、ZnCO3
考查方向
解题思路
工业生产流程方程式
易错点
工业生产流程的理解和分析
正确答案
Zn(或锌)
解析
试剂b为还原物,为了不引入杂质,b为锌单质
考查方向
解题思路
工业生产流程方程式
易错点
工业生产流程的理解和分析
正确答案
①取最后的洗涤液少许于试管,滴加几滴BaCl2溶液,若出现浑浊则未洗净,反之则已洗净
②Na2SO4+CH4
③蒸发浓缩,降温结晶,过滤
解析
①检验ZnS固体是否洗涤干净,只需检测最后一次洗涤液中是否含有硫酸根离子,所以可取最后的洗涤液少许于试管,滴加几滴BaCl2溶液,若出现浑浊则未洗净,反之则已洗净;
②由条件可得化学反应方程式为Na2SO4+CH4
③因为Na2SO4·10H2O的溶解度随温度升高而升高,Na2SO4的溶解度随温度升高而降低,所以从滤液中得到Na2SO4·10H2O的操作方法为蒸发浓缩,降温结晶,过滤
考查方向
解题思路
工业生产流程方程式
易错点
工业生产流程的理解和分析
正确答案
65(Vc-b-d)g
解析
所得硫酸钠物质的量为cvmol,则溶液总共含有cvmol锌元素,步骤Ⅱ加入了bmol锌元素,步骤Ⅲ所得Cd为dmol,即加入了试剂b即锌dmol,所以锌灰中含有锌元素65(Vc-b-d)g
考查方向
解题思路
工业生产流程方程式
易错点
工业生产流程的理解和分析
扫码查看完整答案与解析