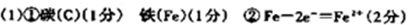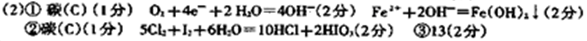- 原电池和电解池的工作原理
- 共168题
大气中可吸入颗粒物PM2.5主要来源为燃煤、机动车尾气等。
(1)若取某PM2.5样本,用蒸馏水处理,测得溶液中含有的离子有:K+、Na+、NH4+、SO42-、NO3-、Cl-,则该溶液为 ___________(填“酸性”或“碱性”)溶液,其原因用离子方程式解释是:__________ 。
(2)“洗涤”燃煤烟气可减轻PM2.5中SO2的危害,下列可适用于吸收SO2的试剂有__________
a.CaCl2溶液
b.氨水
c.Ca(OH)2悬浊液
d.浓H2SO4
(3)煤烟气中的氮氧化物可用CH4催化还原成无害物质。若常温下,1molNO2与CH4反应,放出477.5kJ热量,该反应的热化学方程式是__________ 。
(4)安装汽车尾气催化转化器也可减轻PM2.5的危害,其反应是:__________
2NO(g) + 2CO(g) 
①该反应平衡常数表达式K=__________;温度升高K值__________(填“增大”或“减小” )
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是__________ 。
(5)使用锂离子电池为动力汽车,可减少有害气体的排放。锰酸锂离子蓄电池的反应式为:
Li1-xMnO4 + LixC
下列有关说法正确的是__________
a.充电时电池内部Li+向正极移动
b.放电过程中,电能转化为化学能
c.放电时电池的正极反应式为:Li1-xMnO4+xe—+xLi+=LiMnO4
d.充电时电池的正极应与外接电源的负极相连
正确答案
见解析。
解析
(1)酸性,NH4++H2O
(2)b c
(3)2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(l);△H= -955kJ/mol
(4)①
(5)c
知识点
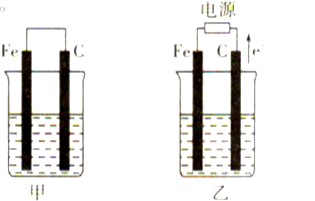
30.甲、乙两池的电极材料都是铁棒与碳棒(如图)。
请回答下列问题:
(1)若两池中均盛放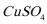
①有红色物质析出的是:甲池中的( )棒;乙池中的____棒;
②甲池中负极的电极反应式是( )。
(2)若两池中均盛放饱和NaCl溶液,反应一段时间后
①甲池中( )棒附近首先出现白色浑浊,用离子方程式表示该电极附近白色浑浊出现的原因( )。
②将湿润的淀粉KI试纸放在乙池的( )棒附近,发现试纸变蓝,待一段时问后又发现试纸蓝色褪去,这是因为过量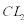
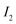
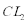
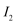
③若乙池转移0.02 mol电子后停止实验,池中溶液的体积是200 ml.,则将溶液混匀后的pH=( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13. 将羧酸的碱金属盐电解可生成烃类化合物,例如:


正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13. 一种新型燃料电池,是用两根金属铂做电极插入KOH溶液中,然后向两极上分别通入CH3OH和O2,下解说法不正确的是
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.查处酒后驾驶采用的便携式乙醇测量仪以燃料电池为工作原理,在酸性环境中,理论上乙 醇可以被完全氧化为

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析