- 元素周期律的实质
- 共71题
5.已知X、Y、Z、W都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,W的族序数比X的族序数大1,则下列说法错误的是()
正确答案
解析
由X原子的电子层数与它的核外电子总数相等推知为H。由Z原子的最外层电子数是次外层的3倍推知为O。Y和Z可以形成两种以上气态化合物则Y为N。再由它们的原子序数依次递增,W的族序数比X的族序数大1,得知W为Mg。N与O可形成N2O5质量比达到7:20,A正确。形成的NH4NO3中X、Y、Z元素原子个数比为4 :2 :3,故B正确。Mg3N2与H2O反应生成氢氧化镁与氨气二种碱性物质,C正确。形成的10电子微粒有H2O、NH4+、NH3、OH-等多种,D错误。
考查方向
解题思路
由原子核外电子排布信息进行推断,再结合选项逐一分析。
易错点
周期表结构不熟无法推断
知识点
9.
正确答案
解析
X、Y、Z、W是原子序数依次增大的短周期主族元素,X原子最外层有7个电子,四种元素中原子序数X最小,所以X为F元素;Y原子最外层电子数是最内层电子数的一半,而且原子序数大于F,则Y为Na元素;Z最高正价是最低负价绝对值的3倍,则Z的最高正价为+6价,所以Z为S元素,W的原子序数大于S,W为Cl元素;A.Y为Na元素,X为F元素,则Y的离子半径比X的离子半径小,故A错误;B.化合物Na2S中只有离子键,故B错误;C.Y、W最高价氧化物对应水化物分别为NaOH、H2SO4,氧化铝为两性氧化物,能与强酸、强碱反应,故C正确;D.元素的非金属性越强,其氢化物越稳定,非金属性:F>Cl>S,所以简单气态氢化物的稳定性由强到弱的顺序:X、W、Z,故D错误。
故选C
考查方向
解题思路
X、Y、Z、W是原子序数依次增大的短周期主族元素,X原子最外层有7个电子,四种元素中原子序数X最小,所以X为F元素;Y原子最外层电子数是最内层电子数的一半,而且原子序数大于F,则Y为Na元素;Z最高正价是最低负价绝对值的3倍,则Z的最高正价为+6价,所以Z为S元素,W的原子序数大于S,W为Cl元素;结合元素周期律与元素化合物性质解答。
易错点
元素的推断出错会导致随后的解题过程完全错误;元素周期表规律混淆不清
知识点
X.Y.Z.Q.R是五种短周期元素,原子序数依次增大.X是原子半径最小的主族元素;Y元素最高正价与最低负价之和为0;Q与X同主族,;Z.R分别是地壳中含量最高的非金属元素和金属元素.请回答下列问题:
24.①五种元素中,原子半径最大的是 ,非金属性最强的是 .(写元素符号)
②X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)
③由以上某些元素组成的化合物A.B.C.D有如下转化关系:
25.工业合成氨时,合成塔中每产生
①工业合成氨的热化学方程式是 .
②已知:N≡N的键能为945.8kJ/mol,H﹣H的键能为436.0kJ/mol,则断开1mol N—H键所需的能量是 kJ.
26.氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料.电池的总反应为:

正确答案
① Na O .② C2H2 ③ 
解析
X.Y.Z.Q.R是五种短周期元素,原子序数依次增大.X是原子半径最小的主族元素,则X为H元素;Z.R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素.R为Al;Y元素最高正价与最低负价之和为0,由原子序数可知,只能处于第ⅣA族,而其原子序数又小于O元素,故Y为碳元素;Q与X同主族,结合原子序数可知Q为Na;
①所有元素中H原子半径最小,同周期自左而右原子半径减小.非金属增强,同主族自上而下原子半径增大.非金属性减弱,故上述五种元素中,Na的原子半径最大,O的非金属性最强,
故答案为:Na;O;
②H与C能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质为C2H2,
故答案为:C2H2;
③由以上某些元素组成的化合物A.B.C.D有如下转化关系:

故答案为:
考查方向
解题思路
X.Y.Z.Q.R是五种短周期元素,原子序数依次增大.X是原子半径最小的主族元素,则X为H元素;Z.R分别是地壳中含量最高的非金属元素和金属元素,则Z为O元素.R为Al;Y元素最高正价与最低负价之和为0,由原子序数可知,只能处于第ⅣA族,而其原子序数又小于O元素,故Y为碳元素;Q与X同主族,结合原子序数可知Q为Na;
易错点
不知道结构性质位置关系应用.热化学方程式书写.键能与反应热关系.原电池等,无法推断元素,需注意元素最高正价与最低负价之和均为0,可以为ⅣA族元素,也可以为H元素,中学中较少涉及H元素的负化合价。
正确答案
①N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.2kJ/mol
② 391 kJ.
解析
①生成2mol氨气放出的热量为46.1kJ×2=92.2kJ,反应热化学方程式为:N2(g)+3H2(g)⇌2NH3(g)△H=−92.2kJ/mol,
故答案为:N2(g)+3H2(g)⇌2NH3(g)△H=−92.2kJ/mol;
②设断开1mol N−H键所需的能量是xkJ,则945.8kJ/mol+3×436.0kJ/mol−6×xkJ/mol=−92.2kJ/mol,解得x=391,
故答案为:391;
考查方向
解题思路
①计算生成2mol氨气放出的热量,注明物质的聚集状态与反应热书写热化学方程式;②反应热=反应物总键能−生成物总键能;
易错点
不知道结构性质位置关系应用.热化学方程式书写.键能与反应热关系.原电池等,无法推断元素,需注意元素最高正价与最低负价之和均为0,可以为ⅣA族元素,也可以为H元素,中学中较少涉及H元素的负化合价。
正确答案
2NH3+6OH﹣﹣6e﹣=N2+6H2O
解析
原电池负极发生氧化反应,氨气在负极失去电子,碱性条件下生成氮气与水,负极电极反应式为:2NH3+6OH−−6e−=N2+6H2O,
故答案为:2NH3+6OH−−6e−=N2+6H2O。
考查方向
解题思路
原电池负极发生氧化反应,氨气在负极失去电子,碱性条件下生成氮气与水.
易错点
不知道结构性质位置关系应用.热化学方程式书写.键能与反应热关系.原电池等,无法推断元素,需注意元素最高正价与最低负价之和均为0,可以为ⅣA族元素,也可以为H元素,中学中较少涉及H元素的负化合价。
3. 短周期主族元素X、Y、Z、W的原子序数依次增大。X、Y、Z、W原子的最外层电子数之和为18,X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构。下列说法正确的是( )
正确答案
解析
A.Y的单质是氧气,Z的单质是金属镁,金属镁的沸点大于氧气的沸点,故A错误;
B.C、O、Mg三种元素可以形成离子化合物MgCO3,故B错误;
C.非金属性S>C,因此最高价氧化物对应的水化物的碳酸的酸性小于硫酸的酸性,故C错误;
D.Y分别与Z、W形成的化合物分别为MgO、SO2或SO3,MgO中含有离子键,SO2或SO3中含有共价键,化学键类型不同,D正确。
故选D。
考查方向
原子结构与元素周期律的关系。
解题思路
X原子的最外层电子数是其内层电子数的2倍,因此X是C,Y是地壳中含量最高的元素O,Z2+与O2-具有相同的电子层结构,因此Z为Mg。X、Y、Z、W原子的最外层电子数之和为18,W是S,据此解答。
易错点
本题考查了短周期元素种类推断,涉及元素周期律中非金属性的比较以及化合键的判定等知识,难度不大,熟悉短周期元素的原子结构是解题的必备知识。
知识点
14. X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是
正确答案
解析
X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,X、Y同周期,则X为S元素,
A.X、Y、Z分别为S、Na、F,原子最外层电子数分别为6、1、7,即原子最外层电子数:Z>X>Y,故A错误;
B.常温下Na、S为固体,F2为气体,Na的熔点较低,但钠的沸点高于硫,顺序应为Na>S>F2,故B错误;
C.Na+、F-具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为F->Na+,S2-电子层最多,离子半径最大,故离子半径S2->F->Na+,故C错误;
D.电子层数越大原子半径越大,电子层数相同,原子序数越大半径越小,则原子半径:Y>X>Z,故D正确
考查方向
原子结构与元素周期律的关系
解题思路
X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,X、Y同周期,则X为S元素,结合元素在周期表中的位置以及元素周期律知识解答该题
易错点
B项中单质沸点的比较
教师点评
本题考查原子结构与元素周期律的关系,侧重于学生的分析能力的考查,题目难度不大,本题的关键是根据原子结构特点正确推断元素的种类。
知识点
3.已知A、B、C、D、E是5种短周期元素,C、D、E是原子半径依次递减的同周期元素,A的L层电子数是其K层电子数的3倍,B是组成有机物的必要元素,元素C是海水中含量最高的金属元素,元素D与B的原子最外层电子数相同,E原子处于能量最低状态时只有1个未成对电子,下列说法正确的是
正确答案
解析
A.电子层数越多,原子半径越大,电子层数相同,核电荷数越大,原子半径越小,因此原子半径大小顺序是:C>D>E>B>A,A错误;
B.电解饱和NaCl溶液,阴极可以得到氢气,阳极可以得到氯气,B正确;
C.Na与O形成的两种化合物Na2O2和Na2O,Na2O2中含有非极性共价键和离子键,Na2O中含有离子键,C错误;
D.非金属性由强到弱:Cl>C>Si,最高价氧化物对应水化物是H2CO3、H2SiO3、HClO4,非金属性越强,最高价氧化物对应水化物的酸性越强,因此酸性由强到弱:HClO4>H2CO3>H2SiO3,D错误。
故选B。
考查方向
解题思路
A、B、C、D、E五种短周期元素,A的L层电子数是其K层电子数的3倍,即A为O;B是组成有机物的必要元素,即B为C;元素C是海水中含量最高的金属元素,即C为Na;元素D与B的原子最外层电子数相同,即D为Si;C、D、E是原子半径依次递减的同周期元素,则C、D、E是原子序数递增的同周期元素,E原子处于能量最低状态时只有1个未成对电子,即E为Cl;即A-O、B-C、C-Na、D-Si、E-Cl,据此分析:
A.电子层数越多,原子半径越大,电子层数相同,核电荷数越大,原子半径越小;
B.电解饱和NaCl溶液,阴极可以得到氢气,阳极可以得到氯气;
C.Na2O2中含有非极性共价键和离子键,Na2O中含有离子键;
D.非金属性越强,最高价氧化物对应水化物的酸性越强。
易错点
本题考查了位置、结构与性质关系的应用,题目难度中等,正确推断各元素名称为解答关键,注意明确常见元素的原子结构、元素周期表结构与元素周期律内容,熟练掌握常见化学用语的表示方法
知识点
12.X、Y、Z、W是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的金属性最强,W原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述正确的是( )
正确答案
解析
A.X.Y的氢化物分别为CH4.H2O,CH4的沸点在同族氢化物中最低,故A错误;
B.X.Y.Z分别是C.O.Na元素,含有三种元素的化合物有碳酸钠.醋酸钠.甲酸钠.醋酸钠等,故B正确;
C.同周期自左而右原子半径减小.同主族自上而下原子半径增大,一般电子层越多原子半径越大,故原子半径r(Na)>r(Cl)>r(C)>r(O),即原子半径r(Z)>r(W)>r(X)>r(Y),故C错误;
D.Y(O)与Z(Na)形成氧化钠.过氧化钠,过氧化钠含有共价键,Y(O)或W(Cl)形成的化合物含有共价键,故D错误.
故选:B.
考查方向
解题思路
X.Y.Z.W是短周期主族元素,X原子最外层电子数是次外层的两倍,最外层电子数不超过8个,则其K层为次外层,最外层电子数为4,则X是C元素;Y元素在地壳中的含量最多,则Y是O元素;Z元素的金属性最强,则Z是Na元素;W原子的核外电子数是X原子与Z原子的核外电子数之和,则W的核外电子数是17,所以W是Cl元素,据此解答.
知识点
15.如表所示的五种元素中,W.X.Y.Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是
正确答案
解析
W、X、Y、Z为短周期元素,由元素在周期表中位置可知,X、Y处于第二周期,W、Z处于第三周期,令W的最外层电子数为a,则X、Y、Z最外层电子数分别为a+1、a+2、a+3,故a+a+1+a+2+a+3=22,解得a=4,故W为Si、X为N、Y为O、Z为Cl、T为Ge.
A.Ge元素的单质具有半导体的特性,与Cl元素可形成化合物GeCl4,故A正确;
B.物质SiO2、Si3N4均为原子晶体,均有熔点高、硬度大的特性,而SiCl4为分子晶体不具有,故B错误;
C.N、O和H形成的化合物硝酸铵中既有离子键、又有共价键,故C错误;
D.X、Y、Z三种元素最低价氢化物分别为氨气、水、HCl,常温下水为液态,氨气、HCl为气体,故水的沸点最高,氨气分子之间都存在氢键,沸点比HCl的高,故D错误;
考查方向
原子结构与元素周期律的关系
解题思路
W、X、Y、Z为短周期元素,由元素在周期表中位置可知,X、Y处于第二周期,W、Z处于第三周期,令W的最外层电子数为a,则X、Y、Z最外层电子数分别为a+1、a+2、a+3,故a+a+1+a+2+a+3=22,解得a=4,故W为Si、X为N、Y为O、Z为Cl、T为Ge,以此来解答
易错点
氢键存在影响熔沸点
教师点评
本题考查原子结构与元素周期律的关系,为高频考点,把握短周期及最外层电子数的关系推断元素为解答的关键,涉及氢键、化学键、晶体类型及性质、元素周期律等,综合性较强,充分考查了学生灵活应用基础知识的能力,题目难度中等
知识点
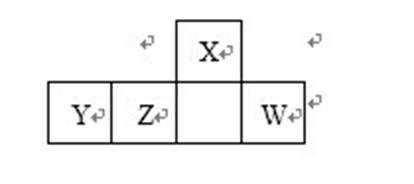
6.X、Y、Z、W是元素周期表中短周期元素,四种元素在元素周期表中的位置关系如下图。如果它们都属于中学化学重点研究的对象,则下列说法中不正确的是
正确答案
解析
X、Y、Z、W是元素周期表中短周期元素,由四种元素在周期表中的相对位置,可知X和Y处于第二周期、Z和W处于第三周期,它们都属于中学化学重点研究的对象,说明均为主族元素,X、Y、Z、W应分别为C、N、S、Cl.
A.均形成分子晶体,相对分子质量越大,分子间作用力越强,沸点越高,故A正确;
B.同周期自左而右非金属性增强,氯元素非金属性比硫的强,故氯气的氧化性比硫的强,故B正确;
C.Y和W可以同时存在于同一离子化合物中,如NH4Cl等,故C正确;
D.碳元素可以形成多种气态氢化物,如甲烷、正丁烷、异丁烷等,故D错误
考查方向
位置结构性质应用
解题思路
X、Y、Z、W是元素周期表中短周期元素,由四种元素在周期表中的相对位置,可知X和Y处于第二周期、Z和W处于第三周期,它们都属于中学化学重点研究的对象,说明均为主族元素,X、Y、Z、W应分别为C、N、S、Cl.
A.均形成分子晶体,相对分子质量越大,沸点越高;
B.同周期自左而右非金属性增强,单质的氧化性增强;
C.Y和W可以同时存在于同一离子化合物中,如NH4Cl等;
D.碳元素可以形成多种气态氢化物.
易错点
C项:符合条件的物质举例
教师点评
本题考查位置结构性质应用,熟练掌握元素周期表的结构,题目难度不大
知识点
4. 短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Y所处的周期数和族序数相等,下列判断错误的是
正确答案
解析
短周期元素X、Y、Z、W在周期表中的位置如图所示,结合元素周期表结构可知,X处于第二周期,Y、Z、W处于第三周期;Y所处的周期数和族序数相等,则Y处于ⅢA族,为Al元素;结合各元素的相对位置可知,Z为Si、X为N、W为S元素,
A.Z为Si、X为N,非金属性:N>Si,则最简单气态氢化物的热稳定性:X>Z,故A正确;
B.Z为Si、W为S元素,非金属性:Si<S,最高价氧化物对应水化物的酸性:Z<W,故B正确;
C.电子层越多,原子半径越大,电子层相同时核电荷数越大,原子半径越小,则原子半径大小为:Y>Z>X,故C正确;
D.Y为Al元素,偏铝酸钠为Al的盐溶液,但偏铝酸钠呈碱性,故D错误
考查方向
原子结构与元素周期律
解题思路
短周期元素X、Y、Z、W在周期表中的位置如图所示,结合元素周期表结构可知,X处于第二周期,Y、Z、W处于第三周期;Y所处的周期数和族序数相等,则Y处于ⅢA族,为Al元素;结合各元素的相对位置可知,Z为Si、X为N、W为S元素,结合元素周期律的知识进行判断
易错点
C项:原子半径比较
教师点评
本题考查了原子结构与元素周期律的关系,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,题目难度不大
知识点
扫码查看完整答案与解析