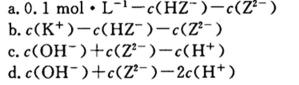- 盐类水解的应用
- 共21题
将足量CO2通入KOH和Ca(OH)2混合溶液,生成沉淀的物质的量和通入CO2体积(V)的关系正确的是
正确答案
解析
略
知识点
根据下列操作及现象,所得结论正确的是
正确答案
解析
略
知识点
23.25℃时,某浓度的NH4Cl溶液pH = 4,下列叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
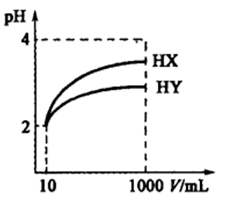
28.常温下,10 mL pH均为2的HX、HY两种一元酸溶液加水稀释过程中溶液的pH随溶液体积变化曲线如右图所示:
请回答下列问题:
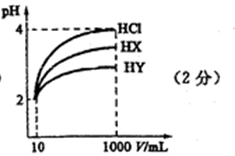
(1)在图中用曲线表示将10 mL pH=2的盐酸加水稀释到1000 mL的过程中溶液pH变化趋势。
(2)物质的量浓度均为
(3)常温下,
(4)若HX、HY均为非氧化性酸,在上述稀释后的HX、HY和盐酸三种溶液中加入足量相同规格的铁粉,则产生氢气的速率最快的是 ( ),产生氢气体积最少的是 ( )。
(5)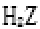

正确答案
(1)
(2)
(3)
(4)
(5)
解析
解析已在路上飞奔,马上就到!
知识点
6.下列过程或现象与盐类水解无关的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析