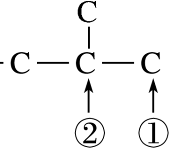
- 苯酚的用途
- 共16题
10.芳香族化合物A与
正确答案
解析
芳香族化合物A与
共计7种。
故选C。
考查方向
解题思路
芳香族化合物A与
共计7种,注意苯环上有2-4个取代基时的同分异构体。
易错点
本题考查同分异构体的书写,题目难度不大,注意苯环上有2-4个取代基时的同分异构体。
知识点
7.下列离子方程式与所述事实相符且书写正确的是
正确答案
解析
A.铁做电极,阳极Fe失去电子,阳极反应为Fe-2e-=Fe2+故A错误;
B.肥皂主要成份是高级脂肪酸的钠盐或钾盐:C17H35COONa ,C17H35COOK ,这两者都是弱酸强碱盐,肥皂溶于水中会发生水解:C17H35COONa +H2O —C17H35COOH + NaOH,C17H35COOK +H2O —C17H35COOH + KOH,因此肥皂水是碱性的,能使酚酞试液变红.
C. 4Fe2++O2+4H+=4Fe3++2H2O硫酸亚铁是酸性条件下才存在的
D.已知苯甲酸的酸性比碳酸强,苯酚的酸性比碳酸弱.可以将 

考查方向
本题主要考查了离子方程式的书写。
解题思路
本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意离子反应中保留化学式的物质,侧重氧化还原反应、电解反应的离子反应考查,题目难度不大
易错点
1、离子反应的书写方法
2、离子反应方程式书写的正误判断
知识点
9.1-乙氧基萘常用作香料,也可合成其他香料。实验室制备1-乙氧基萘的过程如下:
已知:1-萘酚的性质与苯酚相似,有难闻的苯酚气味。相关物质的物理常数:
(1)、将72g 1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是 。
(2)、装置中长玻璃管的作用是: 。
(3)、该反应能否用实验室制备乙酸乙酯的装置 (选填“能”或“不能”),简述理由 。
(4)、反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是 (选填编号)。a.③②④① b.①②③④ c.②①③④
(5)、实验测得1-乙氧基萘的产量与反应时间、温度的变化
如图所示,时间延长、温度升高,1-乙氧基萘的产量下降
可能的两个原因是 。
(6)、提纯的产品经测定为43g,本实验中1-乙氧基萘的产率为 。
正确答案
(1)、提高1-萘酚的转化率 (2)、冷凝回流
(3)、不能、产物沸点大大高于反应物乙醇,会降低产率 (4)、a
(5)、 1-萘酚被氧化,温度高乙醇大量挥发或温度高发生副反应 (6)、50%
解析
(1)首先,根据


(2)反应结束,烧瓶中液体含有













(3)由于酚类物质容易被空气中的氧气氧化,乙醇的沸点较低,因此反应时间延长,温度升高,

(4)根据反应方程式知,



考查方向
解题思路
(1)使用过量的乙醇可提高1-萘酚的转化率,
(2)结合题中的相关物质的物理常数,提纯产物的步骤为A,
(3)如果时间延长,温度升高1-萘酚被氧化(或:温度高乙醇大量挥发)(或:温度高发生副反应),
(4)结合化学方程式计算得1-乙氧基萘的产率为50%。
知识点
己二酸是一种工业上具有重要意义的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用,能够发生成盐反应、酯化反应等,并能与二元醇缩聚成高分子聚合物等,己二酸产量居所有二元羧酸中的第二位。实验室合成己二酸的反应原理和实验装置示意图如下:
可能用到的有关数据如下:
实验步骤如下;
I、在三口烧瓶中加入16 mL 50%的硝酸(密度为1.31g/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
II、水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
III、当环己醇全部加入后,将混合物用80℃~90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
IV、趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。V、粗产品经提纯后称重为5.7g。
请回答下列问题:
27.仪器b的名称为__________。
28.向三口烧瓶中滴加环己醇时,要控制好环己醇的滴入速率,防止反应过于剧烈导致温度迅速上升,否则.可能造成较严重的后果,试列举一条可能产生的后果:_________________________________________________________________。
29.已知用NaOH溶液吸收尾气时发生的相关反应方程式为:2NO2+2NaOH=NaNO2+NaNO3+H2O NO+NO2+2NaOH =2NaNO2+H2O ;如果改用纯碱溶液吸收尾气时也能发生类似反应,则相关反应方程式为:_____________________________、________________________________。
30.为了除去可能的杂质和减少产品损失,可分别用冰水和 洗涤晶体。
31.粗产品可用 法提纯(填实验操作名称)。本实验所得到的己二酸产率为 。
正确答案
球形冷凝管(或冷凝管)
解析
冷凝管主要用来冷凝蒸汽。
考查方向
解题思路
冷凝管的使用。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
反应液暴沸冲出冷凝管;放热过多可能引起爆炸;产生的二氧化氮气体来不及被碱液吸收而外逸到空气中。
解析
应液暴沸冲出冷凝管;放热过多可能引起爆炸;产生的二氧化氮气体来不及被碱液吸收而外逸到空气中。
考查方向
解题思路
当两种盐,它们的溶解度随着温度的变化,而不同时使用重结晶法。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
2NO2+Na2CO3=NaNO2+NaNO3+CO2 NO+NO2+Na2CO3=2NaNO2+CO2
解析
NO2与Na2CO3反应时,根据已知可以看出会发生歧化反应,所以有NaNO2和NaNO3生成,而碳的化合价不发生改变,以二氧化碳的形态出现。
考查方向
解题思路
当碰到不熟悉的方程式时,观察题干给出的反应物与生成物,再利用得失电子守恒配平。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
苯
解析
用溶解性更好的有机溶剂洗涤效果会更好。
考查方向
解题思路
洗涤产物时不能使之溶解。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
正确答案
重结晶 75%
解析
m(环己醇)=5.4 *0.962。再根据质量比进行计算。
考查方向
本题考查化学实验的基本操作及原理。认识仪器。对方程式的迁移。生成物的洗涤。产率的计算。
解题思路
反应液暴沸冲出冷凝管;放热过多可能引起爆炸。
易错点
重结晶法。歧化反应。实验仪器的再认。产率计算。根据条件书写方程式。
成环反应在有机合成中具有重要应用,某环状化合物G的合成过程如下:
40.A→B为加成反应,则B的结构简式是 ;
B→C的反应类型是 .
41.G中含有的官能团名称是 ;
F的化学式为 .
42.D→E的化学方程式是 .
43.H是F的同分异构体,具有下列结构特征:
①核磁共振氢谱除苯环吸收峰外仅有1个吸收峰;
②存在甲氧基(CH3O—).H的结构简式是 .
44.由C通过加聚反应合成高分子化合物M的化学方程式为 .
45.下列说法正确的是 .
正确答案
HC≡C—CH=CH2
解析
从C和E生成F的反应,属于C共轭烯烃的1、4加成。
考查方向
解题思路
质量分数计算可以用铜元素守恒法来计算。
易错点
同分异构体的种类。
正确答案
醚键、酯基 C10H14O3
解析
H的结构中除苯环外只有一个吸收峰且有—OCH3
考查方向
解题思路
熟悉各种官能团后不难识别出醚键和醛基。
易错点
有机官能团的确认
正确答案
CH3C≡C—COOH+CH3CH2OH 
解析
共有3个O,故有3个—OCH3结构
考查方向
解题思路
看到条件后可以判断这是酯化反应。
易错点
加成反应
正确答案
解析
有因为还有一个C,故三个—OCH3结构连在一个C上,得到该物质结构。
考查方向
解题思路
核磁共振氢谱除苯环吸收峰外仅有1个吸收峰,说明只有1种氢。
易错点
加聚反应。
正确答案
nCH2=CH—CH(OCH3)=CH2 

解析
nCH2=CH—CH(OCH3)=CH2
考查方向
本题考查有机物的结构性质同分异构体的书写,方程式的书写,加成反应,核磁共振氢谱图,聚合反应,有机推断。
解题思路
从C和E生成F的反应,属于C共轭烯烃的1、4加成。
易错点
消去反应
正确答案
考查方向
易错点
π键的判断
9.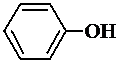
正确答案
解析
--C4H9可形成以下2*2种取代基,每一种取代基都可以在苯环上羟基的邻位、间位和对位形成三种异构体,共计是3*4=12种
考查方向
本题主要考查了同分异构体的判断种数计算。
解题思路
步骤1:写出-C4H9可能的碳骨架,有2种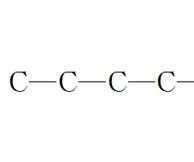
步骤2:根据“等效氢原子法”确定取代的位置,并标号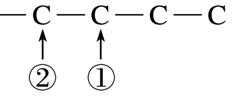
步骤3:计算数目--C4H9可形成以下2*2=4种取代基
易错点
1、
2、-C4H9同分异构体数量的判断
知识点
10. 2—氨基—5—硝基苯甲醚俗称红色基B,其结构简式如右所示。若化学式与红色基B相同,且氨基与硝基直接连在苯环上 并呈对位时的同分异构体数目(不包括红色基B)可能为
正确答案
解析
先考虑官能团异构有醚、醇、酚,属于醚时,根据位置异构有2种:


考查方向
解题思路
先考虑官能团异构有醚、醇、酚,属于醚时的位置异构数量:确定属于醇时位置异构数量;属于酚时位置异构数量;根据羟基的不同有2种,再考虑甲基的位置;总数=位置异构数量*甲基的位置数。
易错点
1、根据官能团不同造成的同分异构体及官能团的位置不同造成的同分异构体来判断苯环上并呈对位时的同分异构体数目;
2、同分异构体结构的关键是按“碳架结构→类别异构→官能团或取代基位置异构”顺序有序补举,同时要充分利用“对称性”防漏剔增;
知识点
3.青蒿素对治疗疟疾有很好的效果,下列说法正确的是()
正确答案
解析
A.青蒿素含有酯基,几乎不易溶于水,可溶解于乙醇,易溶于氯仿、丙酮、乙酸乙酯和苯,A错误;
B.青蒿素分子中共含有5个环,其中有3个六元环(1个六碳环、1个五碳一氧环、1个三碳三氧环)和2个七元环(1个六碳一氧环、1个五碳二氧环),B错误;
C.青蒿素中含过氧键,过氧键属于非极性共价键,C正确;
D.高分子化合物,是指那些由众多原子或原子团主要以共价键结合而成的相对分子量在一万以上的化合物。纤维素属于高分子化合物,青蒿素不是高分子化合物,D错误。
故选C。
考查方向
解题思路
A.青蒿素含有酯基,几乎不易溶于水,可溶解于乙醇,易溶于氯仿、丙酮、乙酸乙酯和苯;
B.青蒿素分子中共含有5个环,其中有3个六元环(1个六碳环、1个五碳一氧环、1个三碳三氧环)和2个七元环(1个六碳一氧环、1个五碳二氧环);
C.青蒿素中含过氧键,过氧键属于非极性共价键;
D.高分子化合物,是指那些由众多原子或原子团主要以共价键结合而成的相对分子量在一万以上的化合物。纤维素属于高分子化合物。
易错点
本题考查学生对相关有机官能团的理解及有机化合物结构的掌握与应用的能力。
知识点
6.2015年诺贝尔生理学、医学奖的一半授予我国药物化学家屠吆吆,以表彰她发明抗疟疾新药青蒿素和双氢青蒿素。以异胡薄荷醇为起始原料是人工全合成青蒿素的途径之一(如右图)。下列说法正确的是
正确答案
解析
B.青蒿素提取时可以通过加热或加碱溶解,酯基发生断裂。
C.青蒿素易溶于水,易溶于有机溶剂
D.异胡薄荷醇有羟基且相邻碳原子上有H可发生消去反应。
考查方向
本题主要考查了有机官能团的判定和化学性质。
解题思路
识别出有机官能团,判断化学性质。
易错点
1、异胡薄荷醇的分子式的判定。
2、消去反应发生的条件。
知识点
9. 下列说法正确的是
正确答案
解析
A.丙烷、丁烷、正戊烷的沸点随着碳数的增加、相对分子质量越大沸点应依次增大,错误;
B.乙二醇可与乙二酸发生缩聚反应、丙氨酸中含有氨基和羧基可发生缩聚反应,正确;
C.蔗糖水解的最终产物为葡萄糖和果糖,麦芽糖水解的最终产物是葡萄糖,错误;
D.饱和(NH4)2SO4溶液可导致蛋清液发生盐析而凝固,错误;故答案为B。
考查方向
解题思路
在某些物理因素或化学因素的影响下,蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性.物理因素有:加热、加压、搅拌、振荡、紫外线照射、超声波等;化学因素有:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等,饱和(NH4)2SO4溶液可导致蛋清液变性凝固;纤维素的性质和用途。
易错点
1、晶体熔沸点的比较。
2、蛋白质的变性
知识点
扫码查看完整答案与解析