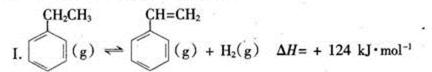- 苯酚的用途
- 共16题
11.
钴(Co)是人体必需的微量元素。含钴化合物作为颜料,具有悠久的历史,在机械制造、磁性材料等领域也具有广泛的应用。请回答下列问题:
(1)Co基态原子的电子排布式为 ;
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。
①酞菁钴中三种非金属原子的电负性由大到小的顺序为 ;
(用相应的元素符号作答);碳原子的杂化轨道类型为 ;
②与钴离子通过配位键结合的氮原子的编号是 ;
(3)CoCl2中结晶水数目不同呈现不同的颜色。
CoCl2可添加到硅胶(一种干燥剂,烘干后可再生反复使用)中制成变色硅胶。简述硅胶中添加CoCl2的作用: ;
(4)用KCN处理含Co2+的盐溶液,有红色的Co(CN)2析出,将它溶于过量的KCN溶液后,可生成紫色的[Co(CN)6]4-,该配离子具有强还原性,在加热时能与水反应生成淡黄色[Co(CN)6]3-,写出该反应的离子方程式: ;
(5)Co的一种氧化物的晶胞如右图所示,在该晶体中与一个钴原子等距离且最近的钴原子有_________个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如下图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是 ( )
正确答案
解析
(1)Co的原子序数为27,基态原子的电子排布式为
考查方向
对电子排布式、电负性、杂化方式、配位键的判断、配位数以及离子方程式等物质结构和性质进行考查。
解题思路
(1)Co的原子序数为27,基态原子的电子排布式为
易错点
由于不能有效掌握配位键的实质与题给信息的分析策略,所以不能准确判断出配
位键;空间想象能力薄弱,不能根据晶胞结构判断配位数。
正确答案
(2)①N>C>H sp2 ②2、4
解析
(2)①非金属性越强电负性越大;每个碳原子只含3个σ键且没有孤电子对,所以属于sp2杂化所以电负性由大到小的顺序为N>C>H,故答案为:N>C>H;
②配位键是中心离子(或原子)提供空轨道,配位体提供孤对电子,是一种特殊的共价键,4个氮原子中,2、4分别提供了孤电子对,钴离子提供了空轨道,故答案为:2、4;
考查方向
对电子排布式、电负性、杂化方式、配位键的判断、配位数以及离子方程式等物质结构和性质进行考查。
解题思路
(2)①非金属性越强电负性越大;每个碳原子只含3个σ键且没有孤电子对,所以属于sp2杂化;②配位键是中心离子(或原子)提供空轨道,配位体提供孤对电子,是一种特殊的共价键,4个氮原子中,2、4分别提供了孤电子对,钴离子提供了空轨道;
易错点
对电子排布式、电负性、杂化方式、配位键的判断、配位数以及离子方程式等物质结构和性质进行考查。
正确答案
(3)随着硅胶的吸湿和再次烘干,二氯化钴在结晶水合物和无水盐间转化,通过颜色的变化可以表征硅胶的吸湿程度
解析
(3)因为无水COCl2为蓝色,水合CoCl2·6H2O显红色。所以根据变色硅胶的颜色变化,可以判断硅胶吸水的程度,随着硅胶的吸湿和再次烘干,二氯化钴在结晶水合物和无水盐间转化,通过颜色的变化可以表征硅胶的吸湿程度,故答案为:随着硅胶的吸湿和再次烘干,二氯化钴在结晶水合物和无水盐间转化,通过颜色的变化可以表征硅胶的吸湿程度;
考查方向
对电子排布式、电负性、杂化方式、配位键的判断、配位数以及离子方程式等物质结构和性质进行考查。
解题思路
(3)因为无水COCl2为蓝色,水合CoCl2·6H2O显红色。所以根据变色硅胶的颜色变化,可以判断硅胶吸水的程度。
易错点
由于不能有效掌握配键位的实质与题给信息的分析策略,所以不能准确判断出配
位键;空间想象能力薄弱,不能根据晶胞结构判断配位数。
正确答案
(4)2[Co(CN) 6 ] 4- +2H 2 O 
解析
(4)[Co(CN)6]4-具有强还原性,能与水反应生成[Co(CN) 6 ] 3-与氢气,根据原子守恒与电荷守恒可知还有OH-生成,故反应的离子方程式为:2[Co(CN) 6 ] 4- +2H 2 O 
+H 2 ↑+2OH – ;
考查方向
对电子排布式、电负性、杂化方式、配位键的判断、配位数以及离子方程式等物质结构和性质进行考查。
解题思路
(4)[Co(CN)6]4-具有强还原性,能与水反应生成[Co(CN) 6 ] 3-与氢气,根据原子守恒与电荷守恒可知还有OH-生成。
易错点
由于不能有效掌握配键位的实质与题给信息的分析策略,所以不能准确判断出配
位键;空间想象能力薄弱,不能根据晶胞结构判断配位数。
正确答案
12 D
解析
(5)该晶胞为面心立方结构,每个钴原子周围与之距离最近的钴原子个数为(3×8)÷2=12,根据晶胞的结构可知,选项ABC的化学式均是符合CoO2的;选项D中Co原子的个数还是1个,但氧原子的个数是4×1/4=1,所以不符合化学组成,故答案为:12 、D
考查方向
对电子排布式、电负性、杂化方式、配位键的判断、配位数以及离子方程式等物质结构和性质进行考查。
解题思路
(5)该晶胞为面心立方结构,每个钴原子周围与之距离最近的钴原子个数为(3×8)÷2=12,根据晶胞的结构可知,选项ABC的化学式均是符合CoO2的;选项D中Co原子的个数还是1个,但氧原子的个数是4×1/4=1,所以不符合化学组成。
易错点
由于不能有效掌握配键位的实质与题给信息的分析策略,所以不能准确判断出配
位键;空间想象能力薄弱,不能根据晶胞结构判断配位数。
13.HO没食子酸丙酯简称PG,结构简式为见右图,是白色粉末,难溶于水,

i.含有苯环,且苯环上的一溴代物只有一种;ii.既能发生银镜反应,又能发生水解反应。
正确答案
⑴C10H12O5,羟基、酯基,4mol
⑵CH3CH2CH2OH; 3;
⑶ ③④
⑷ C
⑸ CH3CH2CHO+2Cu(OH)2
⑹、
解析
⑴根据物质的根据简式可知PG的分子式为C10H12O5;在PG分子中所含官能团有羟基、酯基;在一个PG中含有三个酚羟基和一个酯基,酯基水解得到一个羧基和一个醇羟基。酚羟基与羧基能与NaOH发生反应,而醇羟基不能发生反应。所以1mol没食子酸最多可与4mol NaOH发生反应。所以答案为:C10H12O5,羟基、酯基,4mol。
⑵PG在NaOH水溶液中加热水解,然后酸化得到丙醇A:CH3CH2CH2OH和B:没食子酸
⑶通过上述分析可知①是取代反应;②⑤是复分解反应;③④是氧化反应;所以答案为③④。
⑷因为在PG分子中含有三个酚羟基,能够与氧气发生反应而被氧化,从而对其它物质起到了保护作用。因此PG具有抗氧化作用。所以答案为C。
⑸反应④是:CH3CH2CHO与Cu(OH)2反应生成Cu2O砖红色沉淀和对应的羧酸,所以反应的化学方程式为:CH3CH2CHO+2Cu(OH)2
考查方向
解题思路
⑴根据物质的根据简式可知PG的分子式为C10H12O5;根据PG在转化关系图中发生反应的性质可以判断出PG分子中所含官能团有羟基、酯基;在一个PG中含有三个酚羟基和一个酯基,酯基水解得到一个羧基和一个醇羟基。酚羟基与羧基能与NaOH发生反应,而醇羟基不能发生反应。
⑵PG在NaOH水溶液中加热水解,然后酸化得到丙醇A:CH3CH2CH2OH和B:没食子酸
易错点
不注意有机物结构书写造成书写不规范;化学方程式书写缺项或缺少反应条件;
有机结构简式中原子间的连接方式表达不正确,写错位;同分异构体种类的判断不能准确把
握限定条件导致错误或者判断种类时思维无序导致判断结果错。
知识点
26.
X物质是 ( );Y物质是( ) 。
Z物质最适宜选择( )(选填编号)。
a.NaOH b.Na2CO3 c.NaHCO3 d.CaCO3
浓硫酸的作用是 ( 其优点是用量少,可能的进行,如图,产品T是(),
请说明理由 ( ) 。
废水中苯酚的含量,可根据苯酚与溴水的反应,用以下方法测定:
①把20.00mL废水、20mLKBrO3和KBr混合溶液[其中:
c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,
再加入10mL6mol/L的盐酸,迅速盖好盖子,摇动锥形瓶。
②充分反应后,稍松开瓶塞,从瓶塞和瓶壁间缝隙迅速加入10%KI溶液10mL(过量),迅速加盖,充分摇匀。加入少许淀粉溶液。
③用0.0250 mol/LNa2S2O3标准溶液滴定至终点。用去Na2S2O3溶液22.48mL。
已知:BrO3–+5Br–+6H+→3Br2 +3H2O ;写出苯酚与浓溴水反应的化学方程式 ( );第①步加盐酸、第②步加KI溶液,要迅速盖好盖子的原因是( )。
已知:I2 +2Na2S2O3→2NaI + Na2S4O6;滴定终点的现象是( );该废水中苯酚的浓度是 ( ) mol/L(保留4位小数)。
正确答案
氧气(或空气);异丙苯
解析
.由信息方程式得:X应该是氧气(要氧化异丙苯);Y是再“回炉氧化”的物质,故为异丙苯。
考查方向
有机合成与实验、有机物的性质
解题思路
信息优先,信息与已有知识点的整合迁移。
易错点
Z物质最适宜选择、及废水中苯酚的浓度的计算。
正确答案
c
解析
Z物质最适宜选择是NaHCO3,因其不与苯酚反应。
考查方向
有机合成与实验、有机物的性质。
解题思路
信息优先,信息与已有知识点的整合迁移。
易错点
Z物质最适宜选择、及废水中苯酚的浓度的计算。
正确答案
催化剂,浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等)
解析
浓硫酸的作用是催化剂。其优点是用量少,可能的缺点是浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等)
考查方向
有机合成与实验、有机物的性质。
解题思路
信息优先,信息与已有知识点的整合迁移。
易错点
Z物质最适宜选择、及废水中苯酚的浓度的计算。
正确答案
苯酚与溴水的反应方程式(略),防止溴挥发
解析
苯酚与浓溴水反应的化学方程式
要迅速盖好盖子的原因是因为溴易挥发,故盖好盖子防止溴挥发。
考查方向
有机合成与实验、有机物的性质。
解题思路
信息优先,信息与已有知识点的整合迁移。
易错点
Z物质最适宜选择、及废水中苯酚的浓度的计算。
正确答案
由蓝色变为无色(或白色浑浊)且半分钟内不变色;0.0053
解析
①依据KBrO3+5KBr+6HCl→3H2O+ 3Br2+6KCl
KBr过量,由KBrO3计算溶液中产生溴的总量:
n(Br2)=3 n(KBrO3)=3×0.0100mol·L-1×20×10-3L=0.6×10-3mol。
②依据I2 + 2Na2S2O3→2NaI + Na2S4O6
Br2+2I-(过量)→I2+2Br-
得关系式:Br2~I2~2Na2S2O3,
此时消耗n(Br2)= n(Na2S2O3)/2=22.48×10-3L×0.0250 mol/L÷2=0.281×10-3mol。
③与废水中苯酚反应的溴为:n(Br2)= 0.6×10-3 mol-0.281×10-3mol=0.319×10-3 mol,
则n(C6H5OH)= n(Br2)/3,故该废水中苯酚的浓度是:
c(C6H5OH)= n(Br2)/3÷V(废水)= 0.319×10-3mol÷3÷20×10-3L≈0.0053 mol/L(保留4位小数)。
考查方向
有机合成与实验、有机物的性质。
解题思路
信息优先,信息与已有知识点的整合迁移。
易错点
Z物质最适宜选择、及废水中苯酚的浓度的计算。
天然橡胶和香料柑青酸甲酯衍生物F的合成路线如下:
已知:①
②
(R、R’可以是氢原子、烃基或官能团)
14. F中所含官能团的名称是________。
15.试剂a的结构简式是________。
16.关于试剂b的下列说法正确是________(填字母序号)。
17.A与试剂b反应生成B的化学方程式是________。
18.C发生银镜反应的化学方程式是________。
19.E的结构简式是________。
20.分子中含有

正确答案
碳碳双键、酯基
解析
由A加聚生成

考查方向
解题思路
(1)根据官能团的转化可知转化的反应类型依次为;
(2)根据有机物的结构简式判断所含官能团;
(3)根据结合官能团的性质易知生成A的反应,以此可确定a结构简式;
(4)由合成路线可知此步为官能团的保护;
易错点
1、有机合成
2、推断醇烯烃
正确答案
HCHO
解析
由A加聚生成

考查方向
解题思路
(1)根据官能团的转化可知转化的反应类型依次为;
(2)根据有机物的结构简式判断所含官能团;
(3)根据结合官能团的性质易知生成A的反应,以此可确定a结构简式;
(4)由合成路线可知此步为官能团的保护;
易错点
1、有机合成
2、推断醇烯烃
正确答案
解析
由A加聚生成

考查方向
解题思路
(1)根据官能团的转化可知转化的反应类型依次为;
(2)根据有机物的结构简式判断所含官能团;
(3)根据结合官能团的性质易知生成A的反应,以此可确定a结构简式;
(4)由合成路线可知此步为官能团的保护;
易错点
1、有机合成
2、推断醇烯烃
正确答案
解析
由A加聚生成


故答案为
考查方向
解题思路
(1)根据官能团的转化可知转化的反应类型依次为;
(2)根据有机物的结构简式判断所含官能团;
(3)根据结合官能团的性质易知生成A的反应,以此可确定a结构简式;
(4)由合成路线可知此步为官能团的保护;
易错点
1、有机合成
2、推断醇烯烃
正确答案
解析
由A加聚生成

发生银镜反应的化学方程式是
故答案为
考查方向
解题思路
(1)根据官能团的转化可知转化的反应类型依次为;
(2)根据有机物的结构简式判断所含官能团;
(3)根据结合官能团的性质易知生成A的反应,以此可确定a结构简式;
(4)由合成路线可知此步为官能团的保护;
易错点
1、有机合成
2、推断醇烯烃
正确答案
解析
由A加聚生成
可知E的结构简式是为

故答案为

考查方向
解题思路
(1)根据官能团的转化可知转化的反应类型依次为;
(2)根据有机物的结构简式判断所含官能团;
(3)根据结合官能团的性质易知生成A的反应,以此可确定a结构简式;
(4)由合成路线可知此步为官能团的保护;
易错点
1、有机合成
2、推断醇烯烃
正确答案


解析
由A加聚生成
可知A为(CH3)2C=CHCH3,
根据已知②可推知,B与E生成F的反应原理,
可推知E为CH2=C(CH3)COOCH3,
则D为CH2=C(CH3)COOH,C为CH2=C(CH3)CHO,
根据以上信息可知,D为CH2=C(CH3)COOH,
分子中含有



CH2=CH-CH2-COOH,
CH3-CH=CH-OOCH,CH3-CH=CH-COOH,
CH3-CH=CH-OOCH,CH2=C(CH3)OOCH,共7种;
故答案为7种

考查方向
解题思路
(1)根据官能团的转化可知转化的反应类型依次为;
(2)根据有机物的结构简式判断所含官能团;
(3)根据结合官能团的性质易知生成A的反应,以此可确定a结构简式;
(4)由合成路线可知此步为官能团的保护;
易错点
1、有机合成
2、推断醇烯烃
乙苯是一种用途广泛的有机原料,可制备多种化工产品。
(一)制备苯乙烯(原理如反应I所示):
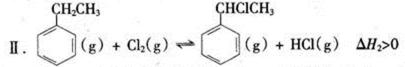
(二)制备α-氯乙基苯(原理如反应II所示):
26.部分化学键的键能如下表所示:
根据反应I的能量变化,计算x= ____。
27.工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气。用化学一平衡理论解释通入水蒸气的原因为____ 。
28.从体系自由能变化的角度分析,反应I在____(填“高温”或“低温”)下有利于其自发进行。
29.T℃时,向10 L恒容密闭容器中充人2mol乙苯(g)和2 mol Cl2(g)发生反应Ⅱ,5 min
时达到平衡,乙苯和Cl2、α-氯乙基苯和HC1的物质的量浓度(c)随时间(t)变化的
曲线如图l所示:
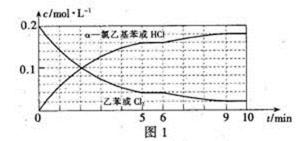
①0—5 min内,以HC1表示的该反应速率v(HCl)=____ 。
②T℃时,该反应的平衡常数K=____ 。
③6 min时,改变的外界条件为________。
④10 min时,保持其他条件不变,再向容器中充人1moI乙苯、1 mol Cl2、1 mol α-氯乙基苯
和l mol HCl,12 min时达到新平衡。在图2中画出10-12 min,Cl2和HC1的浓度变化
曲线(曲线上标明Cl2和HC1);0—5 min和0—12 min时间段,Cl2的转化率分别用α1、α2
表示,则αl α2(填“>”、“<”或“=”)。
正确答案
612
解析
由反应物总键能减去生成物总键能等于焓变可求得x=612;
考查方向
解题思路
反应总能量守恒
易错点
利用化学平衡移动的原理解决实际问题生产中的问题。
正确答案
该反应正向为气体分子数增大的反应,入水蒸气需增大容器容积,减小体系压强,平衡正向移动,增大反应物的转化率。
解析
在恒压设备中进行反应I时,反应正向为气体分子数增大的反应,入水蒸气需增大容器容积,减小体系压强,平衡正向移动,增大反应物的转化率,所以常在乙苯蒸气中通入一定量的水蒸气;
考查方向
解题思路
反应总能量守恒
易错点
利用化学平衡移动的原理解决实际问题生产中的问题。
正确答案
高温
解析
从体系自由能变化的角度分析,反应I在高温下有利于其自发进行;
考查方向
解题思路
反应总能量守恒
易错点
利用化学平衡移动的原理解决实际问题生产中的问题。
正确答案
①0.032 mol·L-1·min-1 ②16 ③升高温度
④<
解析
由图像可知,0—5 min内,v(HCl)=0.16mol·L-1/5min=0.032 mol·L-1·min-1 ;
由题意可得以下三段式:
C6H5CH2CH3 + Cl2 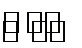
起始/mol 2 2 0 0
转化/mol 1.6 1.6 1.6 1.6
平衡/mol 0.4 0.4 1.6 1.6
所以K=16
由图像可知,6min时,改变的外界条件是升高温度。
考查方向
解题思路
反应总能量守恒
易错点
利用化学平衡移动的原理解决实际问题生产中的问题。
扫码查看完整答案与解析