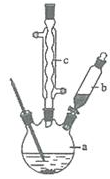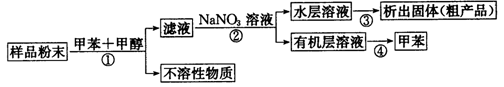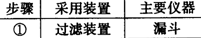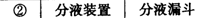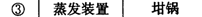- 过滤、分离与注入溶液的仪器
- 共16题
3.下列操作或装置能达到实验目的的是( )
正确答案
知识点
9.实验室从含溴化氢的废液中提取溴单质,下列说法中能达到实验目的的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
19.某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
(一)制取氧化铜
①称取2 g CuSO4·5H2O研细后倒入烧杯,加10 mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是_____________(填实验序号),步骤①③中研磨固体所用仪器的名称是_____________;
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,相关数据如下:
回答下列问题:
(2)上述实验中“待测数据”指______________________;
(3)本实验装置图中量气装置B由干燥管、乳胶管和50 mL滴定管改造后组装而成,此处所用滴定管是_____________(选填“酸式”或“碱式”)滴定管;读数时需要注意
①____________
②视线与刻度线相平
(4)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a.___________________________________________,
b.CuO的化学性质有没有改变。
正确答案
(1)①②③ 研钵
(2)KClO3完全反应所用的时间
(3)碱式 上下移动右管使两液面相平
(4)CuO的质量有没有改变
解析
解析已在路上飞奔,马上就到!
知识点
信息时代给人们的生活带来了极大的便利,但同时也产生了大量的电子垃圾。某化学兴趣小组将一批废弃的线路板简单处理后,得到了主要含Cu、Al及少量Fe、Au等金属的混合物,并设计了如下制备硫酸铜晶体和硫酸铝晶体的路线:
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)过滤操作中用到的玻璃仪器有 。
(2)Cu可溶于稀硫酸与H2O2的混合溶液,其离子方程式是 。
(3)滤渣a的主要成分是 。
(4)步骤③中X的取值范围是 。
(5)假设制得的CuSO4·5H2O中只含Na2SO4杂质,若用该样品进行“硫酸铜晶体结晶水含量的测定”实验,测得结晶水含量 (填“偏低”、“偏高”或“无影响”)。乙同学取1.280g该样品,加热至恒重称得质量变为0.830g,则此样品的纯度为 。(用小数表示,保留三位有效数字)
正确答案
(1) 烧杯、漏斗、玻璃棒
(2)Cu + H2O2+2H+ → Cu2++2 H2O
(3)Au
(4) 5.2≤X<5.4
(5) 偏低(2分),0.977
解析
略
知识点
下列有关实验的叙述正确的是
正确答案
解析
略。
知识点
利用实验器材(规格和数量不限),能完成相应实验的一项是
正确答案
解析
硫酸铜溶液的浓缩结晶需要用到酒精灯,A错;用盐酸出去BaSO4中的少量BaCO3需要进行过滤,需要用到漏斗,B错;用固体配制溶液需要用到托盘天平称量固体,C错;D中可以先进行置换反应,然后进行萃取、分液,D正确。
知识点
试管是最常用的化学仪器之一,下列清洗试管内壁吸附物质所用试剂错误的是
正确答案
解析
略
知识点
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是_______(1分)。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是_______(1分);仪器c的名称是_______(1分),其作用是_______(1分)。反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是_______(2分)。下列仪器中可用于分离苯乙酸粗品的是_______(填标号)(2分)。
A. 分液漏斗
B. 漏斗
C. 烧杯
D. 直形冷凝管
E. 玻璃棒
(3)提纯粗苯乙酸的方法是_______(1分),最终得到44 g纯品,则苯乙酸的产率是_______(2分)。
(4)用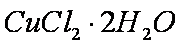
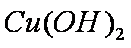
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是_______(2分)。
正确答案
(1)先加水、再加入浓硫酸
(2)滴加苯乙腈;球形冷凝管;回流(或使气化的反应液冷凝);便于苯乙酸析出;BCE
(3)重结晶;95﹪
(4)取少量洗涤液、加入稀硝酸、再加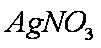
(5)增大苯乙酸溶解度,便于充分反应
解析
略。
知识点
实验室制取乙酸丁酯的实验装置有如
右下图所示两种装置供选用。其有关物质的物理性质
如下表:
(1)制取乙酸丁酯的装置应选用_______(填“甲” 或“乙”)。不选另一种装置的理由是
。
(2)该实验生成物中除了主产物乙酸丁酯外,还可能生成的有机副产物有(写出结构简 式): 、 。
(3)酯化反应是一个可逆反应,为提高1-丁醇的利用率,可采取的措施是 。
(4)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图 示的操作中,肯定需要的化学操作是________________(选填答案编号)。
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器。使用分液漏斗前必须 ;某同学在进行分液操作时, 若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还可能 。
正确答案
(1)(4分)乙(2分) 由于反应物(乙酸和1-丁醇)的沸点低于产物乙酸丁酯的沸点,
若采用甲装置会造成反应物的大量挥发降低了反应物转化率(1分),乙装置则
可以冷凝回流反应物,提高了反应物转化率(1分)。
(2)(4分)CH3CH2CH2CH2OCH2CH2CH2CH3(2分) CH3CH2CH=CH2(2分)
(3)(2分)增加乙酸浓度
(4)(2分)AC(选1个且正确1分,错一个扣0分)
(5)(4分)检查是否漏水或堵塞(2分) 分液漏斗上口玻璃塞上的凹槽未与漏斗口
上的小孔对准(或漏斗内部未与外界大气相通,或玻璃塞未打开。2分)。
解析
略
知识点
海洋动物海鞘中含有种类丰富、结构新颖的次生代谢产物,是海洋抗肿瘤活性物质的重要来源之一。一种从海鞘中提取具有抗肿瘤活性的天然产物的流程如下:
下列关于该流程中各步骤的说法中,错误的是
正确答案
解析
略
知识点
扫码查看完整答案与解析