- 氧化还原反应方程式的配平
- 共44题
某离子反应涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中NH4+的浓度随时间的变化曲线如图所示。下列判断错误的是
正确答案
解析
略。
知识点
一位同学在复习时遇到这样一道习题:某无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。
(1)加入铝粉产生H2,说明铝具有______(填“氧化性”或“还原性”)。
(2)该同学分析:若H+大量存在,则NO3-就不能大量存在。
设计实验证实如下:
① 盐酸溶解Al2O3薄膜的离子方程式是______。
② 根据现象ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
a. 浅棕色气体是______。
b. 实验1的目的是_______。
c. 实验1、2说明反应生成了NO,将生成NO的离子方程式补充完整:
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在。
重新设计实验证实如下:
为确认“刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
① 刺激性气味的气体是______。
② 产生该气体的离子方程式是______。
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是______。
(5)实验结果证实:NO3在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物。习题中的无色溶液一定能大量存在的是Na+和OH-。
正确答案
见解析。
解析
(1)还原性
(2)① 6H+ + Al2O3 == 2Al3+ + 3H2O
② a.NO2
b. 对比实验,排除氧气使湿润的淀粉KI试纸变蓝的可能
c. 1,1,4H+,1,1,2H2O
(3)① NH3
② 8Al +3NO3- + 5OH- + 2H2O == 3NH3↑+ 8AlO2-
(4)2Al +2NaOH + 2H2O == 2NaAlO2 + 3H2↑
知识点
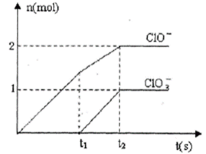
已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应。生成Cl-、ClO-、ClO3-三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
(1)t1时,开始有ClO3-生成的原因是___________________________。
(2)t2时,Ca(OH)2与Cl2发生反应的总的化学方程式为___________________________。
(3)该石灰乳中含有Ca(OH)2的物质的量是_________mol。
(4)若反应物的量不变,在某温度下恰好完全反应时,氧化产物比值为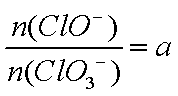
正确答案
(1)反应放热使温度升高,在较高温度下可生成ClO3-
(2)10Cl2 +10Ca(OH)2→Ca(ClO3)2+2Ca(ClO)2+7CaCl2+10H2O
(3)5
(4)(5a+25)/(a+3)
解析
略
知识点
铁屑可用于地下水脱氮,其实验室研究步骤如下:
Ⅰ、将铁屑浸泡在0.5 mol/L盐酸中进行预处理。
Ⅱ、30 min后,用去离子水反复冲洗,至冲洗后液体的pH为中性。在N2保护下烘干备用。
Ⅲ、在蒸馏水中加入硝酸钾配制硝酸钾溶液。
Ⅳ、将酸预处理后的铁屑加入硝酸钾溶液中。
请回答:
(1)盐酸溶解Fe2O3的离子方程式是 。
(2)烘干时需要在N2保护下进行的原因是 。
(3)将步骤Ⅱ中冲洗后的溶液在空气中加热蒸发灼烧,最终得到的固体是 。
(4)将酸性条件下,铁与NO3-反应的离子方程式补充完整:
(5)已知活性炭能吸附NH4+ 、OH-。步骤Ⅳ中操作时将铁屑和活性炭同时加入硝酸钾溶液中,可以提高脱氮的效果,其原因是 。
(6)研究表明溶液pH会影响铁屑脱氮的效果,反应体系的pH分别控制在4 和8. 5 时,NO3-的去除率分别为90% 和15%。正常地下水中含有CO32-,会影响脱氮的效果,用化学用语和文字简述其原因 。
正确答案
见解析。
解析
(1)Fe2O3+ 6H+= 2Fe3+ +3H2O
(2)防止铁屑在空气中被氧化
(3)Fe2O3
(4)4 Fe + NO3-+ 10H+=4 Fe2+ + NH4+ +3H2O
(5)活性炭的添加使其和铁构成了无数个微小的铁碳原电池加快反应速率,其次活性炭吸附生成物NH4+ 、OH-能降低出水中的NH4+的浓度。(并且能降低出水pH 值,这可能是因为活性炭能够吸附OH-。)
(6) CO32-+H2O 
知识点
27.(1)请将5种物质:




_________+__________→__________+__________+__________+ H2O
(2)反应物中发生氧化反应的物质是( ),被还原的元素是( )。
(3)反应中1 mol氧化剂( )(填“得到”或“失去”)( )mol电子。
正确答案
(1) 
(2)
(3)得到 ; 4
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析