- 原子结构与元素周期律的关系
- 共7题
6.设NA为阿伏加德罗常数,下列叙述中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
25.C、N、O、Al、Si、Cu是常见的六种元素。
(1)Si位于元素周期表第____周期第_____族。
(2)N的基态原子核外电子排布式为_____;Cu的基态原子最外层有___个电子。
(3)用“>”或“<”填空:

0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1时,原电池中电子流动方向发生改变,其原因是______。
正确答案
(1)三;IVA
(2)
(3)> < > <
(4)


解析
解析已在路上飞奔,马上就到!
知识点
元素的原子结构决定其性质和周期表中的位置。下列说法正确的是
正确答案
解析
有些元素的最高价不等于最外层电子数,如O、F等元素,故A错;根据核外电子排布规律,能量低的电子在离核较近的区域内运动,能量高的电子在离核较远的区域内运动,故B错;元素的得电子能力越强,其最高价氧化物对应的水化物的酸性越强,故C正确;周期表中位于金属和非金属分界线附近的元素通常既显一定的金属性,又显一定的非金属性,而过渡元素是指副族和第Ⅷ元素,故D错。
知识点
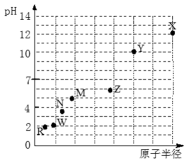
第三周期元素,浓度均为0.01 mol/L的最高价氧化物对应水化物的pH与原子半径的关系如下图所示。则下列说法正确的是
正确答案
解析
略
知识点
13、X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族的短周期元素可形成常见气体甲(甲有刺激性气味)。X、Y、Z 三种元素形成化合物乙。下列说法不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其电子层数的
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种主族元素组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是
正确答案
解析
A.Y为锂元素、Z为铍元素、R为氧元素、T为氟元素,位于同周期,元素的原子半径从左向右半径在减小,即原子半径:Y>Z>R>T,故A正确;
B.W为硅元素、R为氧元素、T为氟元素,非金属性F>O>Si,则气态氢化物的稳定性W<R<T,故B正确;
C.X为钙元素、Z为铍元素,金属性Ca>Be,则最高价氧化物对应的水化物碱性:氢氧化钙>氢氧化铍,故C正确;
D.XR2、WR2两化合物CaO2、SiO2,CaO2中O元素为-1价,SiO2中O元素化合价为-2,故D错误,
故选C
考查方向
解题思路
香花石化学式为X3Y2(ZWR4)3T2,由前20号元素中的6种组成,其中R原子最外层电子数为其次外层电子数的3倍,R原子只能有2个电子层,最外层电子数为6,则R为O元素;Y、Z、R、T位于同周期,即处于第二周期,T元素无正价,则T为F元素;Z的最外层电子数与次外层电子数相等,则Z为Be元素;Y为金属元素,则Y为Li;X、Z位于同主族,则X为Mg元素或Ca元素,若X为镁元素,则由X与R原子序数之和是W的2倍,则

易错点
本题推断元素是关键,各选项判断都不难,但气态氢化物的稳定性是容易出错的知识点
知识点
扫码查看完整答案与解析