- 化学实验
- 共767题
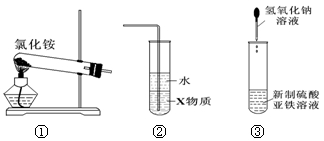
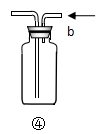
7.关于下列各装置图的叙述中,正确的是()
正确答案
解析
A.实验室用装置①制取氨气,缺少反应物石灰,故错误;
B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸,是一种重要的防倒吸装置,正确;
C.装置③制备氢氧化亚铁时,要观察其颜色,必须是用较长的滴管、且伸入到硫酸亚铁液面滴下。故错误;
D.装置④ b口进气,只能收集密度比空气小的气体,故可收集CO2等气体错误。
考查方向
解题思路
依据实验操作的规范(细节)、原理解题。
易错点
对某些实验基本操作细节的忽视或遗忘,就会错选C等。
知识点
下列根据实验及现象得出的结论不正确的是
正确答案
解析
略
知识点
煤是“工业的粮食”,石油是“工业的血液”。有关煤和石油加工的说法正确的是
正确答案
解析
略
知识点
30.在用FeSO4溶液与NaOH溶液反应制备白色的Fe(OH)2时,出现了“白色沉淀迅速转变为灰绿色,最后逐渐变成红褐色”的实验现象,如何解释出现灰绿色的现象,探究小组的同学产生了不同的观点:
①灰绿色物质就是红褐色的氢氧化铁跟白色的氢氧化亚铁的简单混合物;
②灰绿色物质是铁的一种新的氢氧化物,但其中不含Fe3+离子。
(1)验证观点①不正确的实验操作是:( ),验证观点②所需的试剂有:( )。
(2)某同学查阅资料后,得到Fe(OH)2如下信息:
阅读该资料后,你对上述实验中出现灰绿色的现象的解释是:( )。
探究小组的同学在研究由Fe2+制备Fe(OH)2的过程中,甲、乙、丙、丁四位同学分别设计了如下4个实验方案:
甲方案:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
乙方案:应用钢铁吸氧腐蚀的原理, 设计电池制备Fe(OH)2。
丙方案:按图实验,制备Fe(OH)2。
丁方案:按图实验,制备Fe(OH)2。
(苯的作用是使电解质溶液隔绝空气)
回答下列问题:
①在甲方案中,所用FeSO4样品通常部分被氧化,写出在配制FeSO4溶液时,其操作过程及反应的离子方程式:( )。
②在乙方案中,正极的电极反应式是:( )。你认为该方案是否可行?( ),若不可行请说明理由(若可行,则该空不需回答):( )。
③在丙方案中,当容器B、A中均加入试剂并塞好橡皮塞后,还需要进行的操作是( )。
④在丁方案中,在两电极之间的溶液中首先观察到白色沉淀。请写出b电极的电极反应式:( )。则其电解质溶液可以是下列三项中的( )
A.蒸馏水
B.NaCl溶液
C.NaOH溶液
正确答案
(1)取红色和白色固体粉末混合均匀后,若混合物的颜色不为灰绿色,则证明观点不正确。盐酸或稀硫酸、KSCN溶液。
(2)Fe(OH)2 易被氧化成灰绿色的Fe3(OH)8 ,其中含有Fe2+、Fe3+。
①向盛有蒸馏水的烧杯中加入一定量的硫酸,再将样品置于其中,搅拌溶解;然后加入过量的还原铁粉,反应为:2Fe3++Fe=3Fe3+,搅拌、静置,上层清液即为所要配置的FeSO4溶液。 ②O2+2H2O+4e-=4OH- 否产生的Fe(OH)2随即就被空气氧化为Fe(OH)3
③打开胶管夹C,使反应进行一段时间后关闭C④2H++2e-=H2↑ B
解析
解析已在路上飞奔,马上就到!
知识点
27.利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置(图15)如下:
(1)B装置有三种功能:①控制气流速度;②均匀混合气体;③( )。
(2)设
(3)D装置的石棉中均匀混有KI粉末,其作用是( )。
(4)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式( ) 。
(5)E装置中除盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为( )。
A.水洗分液法 B.蒸馏法 C.过滤法 D.结晶法
(6)工业上氯气采用电解饱和食盐水的方法来获得。若要获取标况下
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.铆在铜板上的铁铆钉(如图所示),处于酸性不强的水膜中。下列有关说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.化学与生产、生活、社会密切相关。下列有关说法中不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
7.下列有关物质分类或归纳的说法中,正确的一组是 ( )
①蔗糖和麦芽糖的化学式都可用C12H22O11表示,它们互为同分异构体
②聚乙烯、聚氯乙烯、纤维素都属于合成高分子
③明矾、石膏、冰醋酸、水都是电解质
④盐酸、漂白粉、水玻璃都是混合物
⑤分馏、干馏、裂化都是化学变化
⑥植物油、直馏汽油都可与溴水反应
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.用你所学有机化学知识判断下列表述,其中正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.在实验室进行下列实验,括号内的实验用品都要用到的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
【选做题】本题包括A、B两小题,请选定一中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A [物质结构与性质](请回答35-41题)
下列反应曾用于检测司机是否酒后驾驶:
2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
B实验化学](请回答38-42题)
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的沸点见附表)。其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。步骤4:减压蒸馏有机相,手机相应馏分。
35.Cr3+基态核外电子排布式为_________;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是________(填元素符号)。
36.CH3COOH中C原子轨道杂化类型为______________,1mol CH3COOH分子中含有σ键的数目为 。
37.与H2O互为等电子体的一种阳离子为________(填化学式);H2O与CH3CH3OH可以任意比例互溶,除因为它们都是极性分子外,还因为___________。
38.实验装置中冷凝管的主要作用是________,锥形瓶中的溶液应为________。
39.步骤1所加入的物质中,有一种物质是催化剂,其化学式为_________。
40.步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的______(填化学式)。
41.步骤3中加入无水MgSO4固体的作用是_________。
42.步骤4中采用减压蒸馏技术,是为了防止_____。
附表 相关物质的沸点(101kPa)
正确答案
1s22s22p63s23p63d3 O
解析
(1)Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,则离子的电子排布为1s22s22p63s23p63d3,配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体,O原子提供孤对电子,与Cr3+形成配位键,故答案为:1s22s22p63s23p63d3;O;
考查方向
解题思路
(1)Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体;
易错点
本题涉及核外电子排布、杂化类型等问题,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.
正确答案
sp3和sp2 7mol或7×6.02×1023
解析
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,分别为sp3杂化、sp2杂化,CH3CHOOH分子中含有1个C﹣C、3个C﹣H、1个C﹣O、1个C=O、1个O﹣H等化学键,则1mol CH3COOH分子中含有σ键的数目为7mol或7×6.02×1023,故答案为:sp3和sp2;7mol或7×6.02×1023;
考查方向
解题思路
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,CH3CHOOH分子中含有1个C﹣C、3个C﹣H、1个C﹣O、1个C=O、1个O﹣H等化学键;
易错点
本题涉及杂化类型,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.
正确答案
H2F+ H2O与CH3CH3OH之间可以形成氢键
解析
(3)与H2O互为等电子体的阳离子应含有3个原子、且电子数为10,应为H2F+,H2O与CH3CH3OH都含有氢键,且都为极性分子,二者互溶,故答案为:H2F+;H2O与CH3CH3OH之间可以形成氢键.
考查方向
解题思路
(3)与H2O互为等电子体的阳离子应含有3个原子、且电子数为10,H2O与CH3CH3OH都含有氢键,且都为极性分子,二者互溶.
易错点
本题考查等电子体等问题,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.
正确答案
冷凝回流 NaOH
解析
(1)因溴易挥发,为使溴充分反应,应进行冷凝回流,以增大产率,反应发生取代反应,生成间溴苯甲醛的同时生成HBr,用氢氧化钠溶液吸收,防止污染空气,故答案为:冷凝回流;NaOH;
考查方向
解题思路
苯甲醛与溴在氯化铝催化作用下在60℃时反应生成间溴苯甲醛,通式生成HBr,经冷凝回流可到间溴苯甲醛,生成的HBr用氢氧化钠溶液吸收,防止污染空气,有机相中含有Br2,加入HCl,可用碳酸氢钠除去,有机相加入无水MgSO4固体,可起到吸收水的作用,减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化,以此解答该题.
(1)因溴易挥发,为使溴充分反应,应进行冷凝回流,以增大产率,反应发生取代反应,生成间溴苯甲醛的同时生成HBr,用氢氧化钠溶液吸收,防止污染空气.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
AlCl3
解析
(2)将三颈瓶中的一定配比的无水AlCl3、1,2﹣二氯乙烷和苯甲醛充分混合,三种物质中无水AlCl3为催化剂,1,2﹣二氯乙烷为溶剂,苯甲醛为反应物,
故答案为:AlCl3;
考查方向
解题思路
(2)将三颈瓶中的一定配比的无水AlCl3、1,2﹣二氯乙烷和苯甲醛充分混合,三种物质中无水AlCl3为催化剂,1,2﹣二氯乙烷为溶剂,苯甲醛为反应物.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
Br2、HCl
解析
(3)将反应混合物含有溴,缓慢加入一定量的稀盐酸中,加入碳酸氢钠,可与Br2、HCl反应,故答案为:Br2、HCl;
考查方向
解题思路
(3)将反应混合物含有溴,缓慢加入一定量的稀盐酸中,加入碳酸氢钠,可与Br2、HCl反应.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
除去有机相的水
解析
(4)经洗涤的有机相含有水,加入适量无水MgSO4固体,可起到除去有机相的水的作用,故答案为:除去有机相的水;
考查方向
解题思路
(4)经洗涤的有机相含有水,加入适量无水MgSO4固体,可起到除去有机相的水的作用.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
间溴苯甲醛被氧化
解析
(5)减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化,故答案为:间溴苯甲醛被氧化.
考查方向
解题思路
(5)减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
下图是制备和研究乙炔的性质实验装置图。下列说法不正确的是
正确答案
解析
略
知识点
下图为实验室制取乙炔并验证其性质的装置图。下列说法不合理的是
正确答案
解析
略
知识点
29.请回答下列实验中的有关问题。
(1)实验室用浓硫酸与乙醇共热制取乙烯,以下是某同学设计的三套气体发生装置。
其中合理的是( )(填序号),该装置中,反应容器的名称是( ) 。
(2)利用如下实验装置制备氨气,并完成氨气的喷泉实验。
②实验时,组装好装置后,下列步骤的正确顺序是( )(填序号)。
a.加入试剂 b.检查装置的气密性 c.关闭K1、K2,打开K3 d.关闭K3、打开K1、K2
e.给A装置试管进行加热f.撤去酒精灯g.用热毛巾敷盖在烧瓶上
③实验中,说明D部分烧瓶中氨气已经收集满的现象是( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下图所示的实验装置不能够达到实验目的的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析