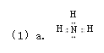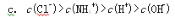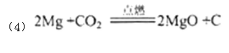- 无机物的性质实验
- 共35题
5.下列有关实验装置进行的相应实验,不能达到实验目的的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
下列说法正确的是
正确答案
解析
略。
知识点
利用下列装置分别完成相关实验,不能达到实验目的的是
正确答案
解析
略
知识点
利用下列实验装置能完成相应实验的是
正确答案
解析
略
知识点
下列叙述错误的是( )
正确答案
解析
生铁中含有碳,构成原电池加快了腐蚀速率,故A说法正确;用锡焊接的铁质器件,焊接处易生锈,是因为构成的原电池中Fe作负极,加快了腐蚀速率,故B正确;在铁制品上镀铜时,镀件应为阴极,故C错;铁管上镶嵌锌块,构成的原电池中Fe作正极,受到保护,故D正确。
知识点
下列叙述不正确的是
正确答案
解析
略
知识点
下列实验操作与预期实验目的或所得实验结论一致的是
正确答案
解析
略
知识点
为了探究二氧化硫的漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,某学习小组设计了如右装置来进行实验。请回答相关问题。
(1)为了探究干燥的SO2 能不能使品红褪色,请指出实验装置图设计中的不合理之处。
① _______; ② ________ 。
(2)按照修改后的装置,实验中控制二氧化硫以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。这说明品红褪色的原因不是二氧化硫直接导致。为此,SO2 通过品红水溶液后,引起品红褪色的微粒可能是___________ 。
(3)甲同学实验如下:取等量、相同浓度的品红水溶液于两支试管中,再分别加入少量亚硫酸钠固体和亚硫酸氢钠固体,两支试管中的品红都褪色,对此,他得出结论:使品红褪色的微粒是______________,不是H2SO3。你认为他的结论是否正确 __________, 其理由是 __________ 。
(4)为了进一步探究,乙组同学做了如下实验:分别取相同浓度的品红溶液各20mL于两只小烧杯中,两只烧杯中同时一次性各加入20mL0.1mol/L的亚硫酸钠,20mL0.1mol/L的亚硫酸氢钠溶液,发现加入亚硫酸钠溶液的品红褪色较快。
①微粒浓度与褪色快慢关系,请用“大”或“小”填写“______”内容
②根据实验和分析,得出的结论是 ___________ ;理由是 ___________ 。
正确答案
(1)二氧化硫没有干燥(或缺少二氧化硫的干燥装置);没有尾气吸收装置
(2)H2SO3、 HSO3-、SO32-
(3)HSO3-、SO32-
不正确,因为亚硫酸根离子和亚硫酸氢根离子都会水解生成亚硫酸。
(4)①
②结论:使品红褪色的微粒是亚硫酸根离子;
原因: SO32-离子浓度大,褪色快;而SO32- 浓度小时,褪色慢。
解析
略
知识点
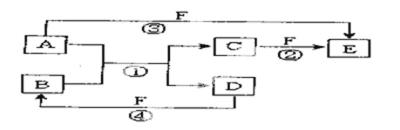
26.A—F有如图所示的转化关系(反应条件未标出),已知反应①是置换反应。请回答下列问题:
(1)若B是黄绿色气体,C、F是空气的主要成分,A、D相遇有白烟生成。
a.写出A的电子式 。
b.写出反应①中直接产生白烟的化学方程式为 。
c. A、D相遇形成的白烟所形成的水溶液中所有离子的浓度由大到小的顺序为
(用离子符号表示)。
d. 有同学模仿排饱和食盐水收集氯气的方法,想用排饱和白烟的水溶液的方法收集A气体。你认为能否达到目的? (填“能”或“否”),理由是 。
(2)若A、D、F都是非金属单质,A、D所含元素同主族,A、F所含元素同周期,则写出反应①的化学方程式为 ;说出B的一个重要用途 。
(3)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行。若C的溶液在空气中暴露一定时间后,要证明该溶液中的阳离子未被氧化完的实验方法是
。
(4)若A、D是常见单质, A的原子序数是D的2倍, D原子的最外层电子数是A的2倍,反应③④中都有红棕色气体生成。则反应①的化学方程式为 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.下列叙述不正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析