- 相对原子质量及其计算
- 共5题
1.中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于
正确答案
解析
A第116号元素Lv的原子序数为116,故A正确; B ,中子数=质量数﹣质子数=293﹣116=177,故B正确;C,原子序数=质子数=核外电子数=核电荷数,可知核外电子数为116,故C正确;D,293代表该原子的质量数,一种元素有多种核素,质量数指的是质子与中子质量的和,不同核素的质量数不同,即一种元素可以有多个质量数,相对原子质量为各核素的平均相对质量,所以同种元素的相对原子质量只有一个数值,两者近似相等,故D错误.故选D.
考查方向
解题思路
根据在原子中:原子序数=质子数=核外电子数=核电荷数,进行解答.
易错点
本题主要考查了原子符号的含义,掌握原子序数=核内质子数=核电荷数是解题的关键,题目难度不大.
知识点
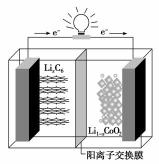
18.某种聚合物锂离子电池放电时的反应为Li1-xCoO2+LixC6=6C+LiCoO2,其电池如图所示。下列说法不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么

请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
①Cu0未完全起反应
② CuO不干燥
③Cu0中混有不反应的杂质
④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_____________,或_______________和_______________达到实验目的。
正确答案
(1)2NH3+3CuO
(2)a→e→b→e
(3)
(4)①③
(5)m(CuO)和m(Cu)、m(Cu)和m(H2O)
解析
本题主要考察氨气的制备、净化、干燥和利用方程式进行的计算以及有关误差分析。氨气具有弱还原性,在加入条件下可以被氧化铜氧化,反应的化学方程式为:
2NH3+3CuO




知识点
8.下列叙述不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数及物质的量分数。现有下列实验用品:中学化学实验常用仪器、1000 mL烧杯、100 mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19 g·cm-3)、水。
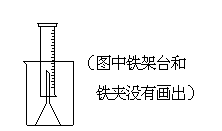
按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100 mL)
(1).补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在1000 mL烧杯底部,把短颈漏斗倒扣在样品上面。
②_________________________________▲________________________________________。
③_________________________________▲________________________________________。
④_________________________________▲________________________________________。
(2).合金样品用铜网包裹的目的是什么?
___________________________________▲_____________________________________。
(3).已知一定质量的铝锌合金的总物质的量为n,实验测得的气体体积为V1mL(已经换算为标准状况)。则铝锌合金中铝的物质的量分数为:_______▲__________。(用含n和V1的式子表示)
(4)本装置也可用于测定金属锌(或其它金属)的相对原子质量,若m g金属锌进行实验,测得的气体体积为V2mL(已经换算为标准状况)。则金属锌的相对原子质量为:________▲_________。(用含m和V2的式子表示)
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析