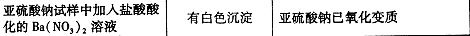- 电解质溶液
- 共721题
26.I.(1)室温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。则图中表示醋酸溶液中pH变化曲线的是____(填“A”或 “B”)设盐酸中加入Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1____m2(选填“<”、“=”、“>”)。
(2)若室温下pH=2的盐酸和醋酸溶液各100mL,分别加水稀释后使pH=4,设盐酸中加入水的体积为V1,醋酸溶液中加入的水的体积为V2,则:V1_______V2(选填“<”、“=”、“>”)。
II.已知常温下,Cu(OH)2 的溶度积常数为Ksp = 2×10 -20。又知常温下某CuSO4溶液里 Cu2+浓度为0.02 mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于____;
III.常温下,某纯碱(Na2CO3) 溶液中滴入酚酞,溶液呈红色,则该溶液呈____性。在分析该溶液遇酚酞呈红色的原因时,甲同学认为,是配制溶液时所用的纯碱样品中混有NaOH 所致;乙同学认为,是溶液中Na2CO3电离出的CO32-水解所致。请你设计一个简单的实验方案,以验证甲和乙的说法(包括操作、现象和结论)____。
正确答案
I (1)B <(2)<
II 5
III 碱
向红色溶液中加入足量BaCl2溶液,如果溶液还显红色说明甲正确,红色褪去说明乙正确
解析
解析已在路上飞奔,马上就到!
知识点
12.常温下向10 mL,0.1mol/L氨水中缓缓加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大 ②c(H+)增大 ③导电性增强
④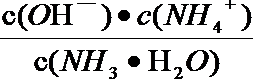
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列根据实验操作和现象所得出的解释或结论正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.室温下10mLpH=3的醋酸溶液作如下改变时,说法正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.25℃时,有关弱酸的电离平衡常数如下:下列有关说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.室温下,下列叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.对于常温下0.0lmol/L的氨水,下列叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.液态化合物AB会发生微弱的自身电离,电离方程式为,
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.分析下表,下列选项中错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.常温下,下列叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析