- 原子结构
- 共16题
9.短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
下列说法中正确的是
正确答案
解析
A光导纤维、棉花、油脂、ABS树脂来自高中化学课本体系的不同位置,但,都是所在部分的重点识记的知识内容。考察学生化学知识面的宽度,考察基础知识的巩固程度和重点知识的敏感度。光导纤维主要成分是SiO2。棉花是天然纤维,油脂是天然混甘油酯,棉花和油脂是天然有机高分子,ABS树脂是合成有机高分子。B、核能、太阳能、甲醇汽油、无磷洗涤剂分据不同章节,和社会生活热点息息相关。但低碳经济,低碳生活并不是书本知识。要了解低碳的含义,更要明确化学知识对低碳的实际意义。考察学生的应用化学知识解决生活问题或关注与化学有关的社会问题的应用积极性。其中无磷洗涤剂不能直接降低碳排放。C、红外光谱仪、核磁共振仪、质谱仪是研究有机物结构的基本实验仪器,课本集中在选修模块中。考察重点实验方法,体现重点知识与化学强调实验的特点。D、阴极射线、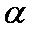
知识点
某同学为了验证碳和硅两种元素非金属性的相对强弱,用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验操作步骤:
Ⅰ. 打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ. A中看到白色沉淀时,…,关闭活塞a。
请回答:
(1)B中反应的离子方程式是________。
(2)通过步骤Ⅰ得知盐酸具有的性质是________(填字母)。
A.挥发性
B.还原性
C.氧化性
D.酸性
(3)C装置的作用是________,X是________(写化学式)。
(4)为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是________,D中反应的化学方程式是________。
(5)碳、硅的非金属性逐渐减弱的原因是________(从原子结构角度加以解释)。
正确答案
见解析。
解析
(1) CaCO3 + 2H+ = Ca2+ + CO2↑+ H2O
(2) A D
(3)除HCl气体 、 NaHCO3
(4)关闭弹簧夹1,打开弹簧夹2,当D中出现白色胶状沉淀后
Na2SiO3 + CO2 + H2O = H2SiO3(胶体)+ Na2CO3
(5)碳和硅位于同一主族,从上到下,原子半径逐渐增大,得电子的能力减弱,非金属性减弱。
知识点
二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H202相似,熔点为l93 K,沸点为41lK,遇水很容易水解,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得。下列有关说法正确的是
正确答案
解析
略
知识点
下列分子中所有原子都满足最外层为8电子结构的是 ( )
正确答案
解析
略
知识点
下列说法正确的是
正确答案
解析
略
知识点
锶(38Sr)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与20Ca和56Ba同属于第ⅡA族。
(1)碱性:Sr(OH)2 Ba(OH)2(填“>”或“<”);锶的化学性质与钙和钡类似,用原子结构的观点解释其原因是 。
(2)碳酸锶是最重要的锶化合物。用含SrSO4和少量BaSO4、BaCO3 、FeO 、Fe2O3、Al2O3 、SiO2的天青石制备SrCO3,工艺流程如下(部分操作和条件略):
Ⅰ.将天青石矿粉和Na2CO3溶液充分混合,过滤;
Ⅱ.将滤渣溶于盐酸,过滤;
Ⅲ.向Ⅱ所得滤液中加入浓硫酸,过滤;
Ⅳ.向Ⅲ所得滤液中先加入次氯酸,充分反应后再用氨水调pH约为7,过滤;
Ⅴ.向Ⅳ所得滤液中加入稍过量NH4HCO3,充分反应后,过滤,将沉淀洗净,烘干,得到SrCO3。
已知:ⅰ.相同温度时的溶解度: BaSO4<SrCO3<SrSO4<CaSO4
ⅱ.生成氢氧化物沉淀的pH
①Ⅰ中,反应的化学方程式是 。
②Ⅱ中,能与盐酸反应溶解的物质有 。
③Ⅳ的目的是 。
④下列关于该工艺流程的说法正确的是 。
a.该工艺产生的废液含较多的NH4+、Na+ 、Cl- 、SO42-
b.Ⅴ中反应时,升高温度一定可以提高SrCO3的生成速率
c.Ⅴ中反应时,加入溶液一定可以提高NH4HCO3的利用率
正确答案
见解析。
解析
(1)< 同一主族元素,原子最外层电子数相同
(2)①
②


③将



④a c
知识点
8. 韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。下列关于“暖冰”的说法正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。下列关于“暖冰”的说法中,正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。下列关于“暖冰”的说法中,正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析