- 铁的化学性质
- 共19题
14.利用右图所示装置进行下列实验,能得出相应实验结论的是
正确答案
C
解析
A. SO2使KMnO4溶液褪色是其还原性而不是漂白性,故A.错误;
B.通氯气到FeBr2溶液中,优先被氧化的是亚铁离子,生成的铁离子溶液呈黄色,后被氧化的才是溴离子,生成的溴单质(低浓度时)也是黄色,因此无法确定是否置换出溴,也就不能得出氧化性:Cl2 > Br2,故B.错误;C.正确;
D.浓硫酸与蔗糖所产生的气体使溴水褪色,是浓硫酸的强氧化性(被还原为SO2)的体现,还有脱水性,这里没有吸水性,故D.错误。
考查方向
解题思路
依据物质性质去判断实验现象。
易错点
FeBr2溶液变为黄色。
知识点
4.在铁的氧化物和氧化铝组成的混合物中,加入2mol/L硫酸溶液65mL,恰好完全反应.所得溶液中Fe2+能被标准状况下112mL氯气氧化.则原混合物中金属元素和氧元素的原子个数之比为( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
7.用下图装置(夹持、加热装置已略)进行试验,有②中现象,不能证实①中反应发生的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
治疗产褥期抑郁症心脾两虚证,应首选()
A.养心汤
B.归脾汤
C.甘麦大枣汤合归脾汤
D.炙甘草汤
E.桂枝加龙骨牡蛎汤
正确答案
C
解析
暂无解析
(NH4)2Fe(SO4)2•6H2O(M=392g•mol-1)又称莫尔盐,简称FAS,其俗名来源于德国化学家莫尔(Karl Friedrich Mohr).它是浅蓝绿色结晶或粉末,对光敏感,在空气中会逐渐风化及氧化,可溶于水,几乎不溶于乙醇.
FAS纯度测定
为测定FAS纯度,取m g样品配制成500 mL溶液,根据物质组成,甲、乙两位同学设计了如下两个实验方
11.甲方案:取20.00 mLFAS溶液,用0.1000 mol·L-1 的酸性K2Cr2O7 溶液进行滴定。i)写出此反应的离子方程式: 。ii) 滴定时必须选用的仪器是 。
12.乙方案:取20.00 mLFAS溶
列出计算FAS晶体纯度的代数式 (不用计算出结果)。
13.
正确答案
i)6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O(2分。化学式错0分。没配平给1分。)
ii)①④⑤⑥(2分。只要有错误即0分)
解析
i).取20.00mLFAS溶液,用0.1000mol•L-1的酸性K2Cr2O7溶液进行滴定,发生的氧化还原反应,亚铁离子被重铬酸钾氧化为铁离子,生成铬离子,反应的离子方程式为:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
ii)酸性K2Cr2O7溶液具有强氧化性,应该使用①酸式滴定管,盛装待测液需要使用④锥形瓶,滴定管需要固定,用到⑤铁架台及⑥铁夹
考查方向
氧化还原滴定
解题思路
i).取20.00mLFAS溶液,用0.1000mol•L-1的酸性K2Cr2O7溶液进行滴定,发生的氧化还原反应,亚铁离子被重铬酸钾氧化为铁离子,生成铬离子
ii).注意是滴定时选用的仪器,不是配制溶液需要仪器,所以应该选用酸式滴定管、锥形瓶、铁架台及铁夹
易错点
氧化还原离子方程式书写
教师点评
本题考查氧化还原滴定,题目难度中等
正确答案
392×25W/2×233m×100% 或196×25W/233m×100%(3分。没加100%不扣分)
解析
取m g样品配制成500mL溶液,取20.00mLFAS溶液进行实验,生成硫酸钡质量为wg,依据定量关系计算,
(NH4)2Fe(SO4)2•6H2O~2SO42-~2BaSO4 ,
1 2
n
解得:
则500ml溶液中为:
FAS晶体纯度的代数式:
考查方向
关系式法定量计算
解题思路
依据定量关系计算,(NH4)2Fe(SO4)2•6H2O~2SO42-~2BaSO4
易错点
关系式
教师点评
本题主要考查关系式法的定量计算,题目难度不大
正确答案
Fe2+被空气部分氧化,(1分)取少量FAS溶液,加入少量KSCN溶液,若溶液变为红色,说明Fe2+已被空气部分氧化(2分。只要有带“.”的关键词即可)
解析
已知实验操作都正确,却发现甲方案的测定结果总是小于乙方案,其可能的原因是Fe2+被空气部分氧化,设计简单的化学实验验证上述推测的实验过程为:取少量FAS溶液,加入少量KSCN溶液,若溶液变为红色,说明Fe2+已被空气部分氧化
考查方向
Fe3+的检验
解题思路
实验操作都正确,却发现甲方案的测定结果总是小于乙方案可能是亚铁离子被空气中氧气氧化,利用铁离子遇到KSCN溶液变红色设计实验检验是否被氧化
易错点
原因分析
教师点评
本题主要考查Fe3+的检验,题目难度不大
11.球墨铸铁中含有一种铁碳化合物X。实验小组为测定化合物X的组成设计实验如下:
下列说法不正确的是( )
正确答案
解析
铁碳化合物X,在足量空气中煅烧得固体1为铁的氧化物,可以有+2价或+3价的铁,溶于盐酸所得溶液中可能Fe2+和Fe3+,再能入足量的氯气,溶液中都为+3价的铁,加热蒸发,铁离子水解,生成氢氧化铁,灼烧后氢氧化铁分解得固体2为氧化铁,24g氧化铁中含有铁元素的质量为

A.固体2是氧化铁,故A正确;
B.X的化学式可以表示为Fe3C,故B错误;
C.溶液甲可以有+2价或+3价的铁,加热、蒸发、灼烧也生成氧化铁,因此可得到24.0g固体,故C正确;
D.X与足量的热浓硝酸反应有NO2和CO2生成,故D正确;
故选B。
考查方向
解题思路
铁碳化合物X,在足量空气中煅烧得固体1为铁的氧化物,可以有+2价或+3价的铁,溶于盐酸所得溶液中可能Fe2+和Fe3+,再能入足量的氯气,溶液中都为+3价的铁,加热蒸发,铁离子水解,生成氢氧化铁,灼烧后氢氧化铁分解得固体2为氧化铁,24g氧化铁中含有铁元素的质量为

易错点
本题主要考查了铁的相关知识,结合实验过程利用元素守恒分析和计算,中等难度,答题时注意元素化合物知识的灵活运用。
知识点
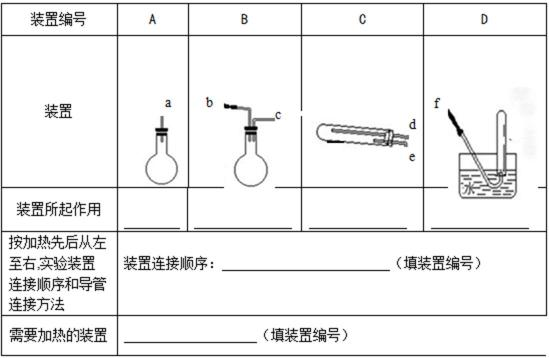
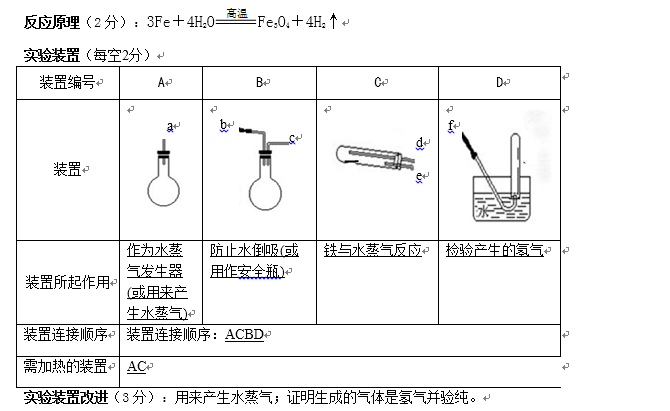
29.铁不能与冷水反应,但能与水蒸气反应,某化学兴趣小组为探究铁与水蒸气反应,请你为他们完成实验报告。
实验目的:探究铁与水蒸气的反应
反应原理:( )(用化学反应方程式表示)
实验装置:回答以下问题(加热装置略去)
实验装置改进:兴趣小组同学根据反应原理改进实验装置,

问:试管底部是蘸有水的湿棉花,其作用是( ),蒸发皿内加入的肥皂液的作用 ( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.下列说法正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.人血红蛋白由珠蛋白和血红素结合而成,一个珠蛋白分子包括两条α链和两条非α链。每个16号染色体上有2个基因控制α链的合成,如果出现有关基因缺失而使α链全部或者部分不能合成,则引起α海洋性贫血。
(1)上述实例表明,基因控制性状的方式之一是 ( ) 。
(2)决定α链的两对基因在传种接代过程中是否遵循孟德尔的遗传定律?请简要说明。
( )。
(2) 某学校研究性学习小组拟进行一项调查活动,用于记录调查结果的表格如下所示。
他们在调查α海洋性贫血的 ( ),你认为该如何减少误差(写出两点): ( ) 、( )。
(4)贫血的各种症状都与细胞缺氧有关,氧在细胞代谢中直接参与有氧呼吸的第( ) 阶段。镰刀型细胞贫血症是另一种先天性贫血症(基因用A、a表示)。某家庭,父亲患红绿色盲,母亲正常(基因用B、b表示),所生育的两个女儿中,一个患镰刀型细胞贫血症,另一个表现正常。正常女儿的基因型是 ( ),如果她与一个其父患红绿色盲、其母患镰刀型细胞贫血症的正常男子结婚,那么,他们生育患病子女的几率是( )。
正确答案
(1)基因通过控制蛋白质的结构而直接控制性状
(2)每对基因之间遵循基因分离定律,两对基因之间不遵循基因自由组合定律(或者遵循基因分离定律,但不遵循基因自由组合定律)
(3)发病率 应在人群中随机抽样调查 调查的人群数量应该足够多
(4)三 AAXBXb或AaXBXb 3/8
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析