- pH的简单计算
- 共20题
3.0.1mol下列气体分别与1L0.lmol·L-1的NaOH溶液反应,形成的溶液pH最小的是
正确答案
知识点
21. 高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:2K2FeO4+16HCl→4 KCl+2FeCl3+8 H2 O+3Q↑,下列说法不正确的是
正确答案
解析
A.Q为氯气,可用湿润的淀粉碘化钾试纸检验产物氯气,故A正确;
B.K2FeO4在水中的电离方程式为K2FeO4═2K++FeO42-,故B错误;
C.反应中16molHCl参加反应只有6mol被氧化,则反应中氧化剂与还原剂的物质的量之比为1:3,故C正确;
D.产物Q为氯气,氯气为单质不是电解质,所以反应中涉及的物质中有5种为电解质,故D正确;
考查方向
氧化还原反应
解题思路
已知2K2FeO4+16HCl═4KCl+2FeCl3+8H2O+3Q↑,根据元素守恒可知Q为氯气,Fe元素的化合价由+6价降低为+3价,Cl元素的化合价-1价升高为0价,以此来解答
易错点
C项中16molHCl参加反应只有6mol被氧化
教师点评
本题考查氧化还原反应、电解质的概念、物质的检验等,把握反应中元素的化合价变化为解答的关键,考查点较多,题目难度不大
知识点
12.
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.(1)用热水配制AlCl3溶液,会出现浑浊现象,原因是(用离子方程式和必要的文字说明):( )。要消除浑浊现象,又不污染药品,可加入适量的__________溶液。
(2)常温下,有①0.01 mol/L HCl溶液;②pH=12的氨水,其中水的电离程度①()②,(选填“>”、“<”或“=”);若将①、②混合后所得溶液pH=7,则消耗溶液的体积:①()②(选填“>”、“<”或“=”)。若用①来滴定未知浓度的氨水,通常选用____________作指示剂,达滴定终点时各离子浓度由大到小的顺序是_________________________________。
(3)某温度(T℃)时,测得0.01 mol·L-1NaOH溶液的pH=11,则在该温度下,将100 mL 0.2 mol·L-1的稀盐酸与100 mL 0.4 mol·L-1的NaOH溶液混合后,溶液的pH=( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.常温下,下列关于溶液pH的计算错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
7.某温度下,向PH=6的纯水中加入一定量的盐酸,保持温度不变,测得溶液的pH=2,对于该溶液,下列叙述中不正确的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.常温下,下列关于溶液pH的计算错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5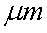
请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。
若测得该试样所含离子的化学组分及其浓度如下表:
根据表中数据判断试样的pH=( )。
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+1/2O2(g)=H20 (g) △H=-241.8kJ·mol-1
C(s)+1/2O2(g)=CO(g) △H=-110.5kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:( )。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是( ) 。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中有NOx和CO的生成及转化
① 若1mol空气含0.8molN2和0.2molO2,汽缸中的化学反应式为
1300℃时将1mol空气放在密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K=( ) 。
汽车启动后,汽缸温度越高,单位时间内NO排放量越大,其原因是 ( ) 。
②目前,在汽车尾气系统中装置催化转化器可减少CO和NOx的污染,其化学反应方程式为 ( ) 。
③ 汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO,
2CO(g)=2C(s)+O2(g)
已知该反应的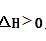
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.在新制的氯水中存在下列平衡:C12+H2O H++C1-+HC1O,若向氯水中加入少量Na2CO3粉末,溶液中发生的变化是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.常温下,电解某溶液x只生成H2和O2,下列有关电解过程的叙述正确的是( )(均在常温下讨论)①x溶液浓度可能增大 ②x溶液浓度可能减小 ③x溶液浓度可能不变 ④x溶液pH可能增大 ⑤x溶液pH可能减小 ⑥x溶液pH可能不变
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析











