- 常见阳离子的检验
- 共26题
28.某废水中仅含右表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。甲同学欲探究废水的组成,进行了如下实验:
I.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入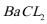
请推断:
(1)由I、Ⅱ判断,溶液中一定不含的阳离子是( )(写离子符号)。
(2)Ⅲ中加盐酸生成无色气体的的离子方程式是( ) .
(3)Ⅲ中所得红棕色气体是( ),该气体通入水中,气体变尤色,所发生反应的化学方程式为 ( ) .
(4)甲同学通过实验现象并结合计算,最终确定原溶液中所含阳离子是____(写
离子符号,下同),阴离子是________。
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为 ( )g。
(6)工业废水中常含有不同类型的污染物.可采用不同的方法处理。以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是____(填选项编号)。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
13.某溶液中可能含有以下6种离子中的几种:NH4+、A13+、Mg2+、CO32―、Cl一、SO42―,为确认溶液组成,现取100 mL分成三等份溶液进行如下实验:
(1)向第一份溶液中加入 AgNO3溶液有沉淀产生;
(2)向第二份溶液中加入足量NaOH溶液充分反应后,最终得到沉淀0.58 g,同时收集到气体0.03 mol(设气体全部从溶液中逸出);
(3)向第三份溶液中加入足量BaCl2溶液(盐酸酸化)充分反应后,得到沉淀6.99 g。由此可知,下列关于原溶液组成的正确结论是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.某混合物的水溶液,可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4(+)、Cl-、CO3(2-)、SO4(2-),现分别取100 mL的三等份溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加过量NaOH溶液加热后,只收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
③在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
④第三份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65 g。
根据上述实验回答:
(1)一定不存在的离子是,不能确定是否存在的离子是( )。
(2)试确定溶液中肯定存在的离子及其浓度(可不填满):离子符号,浓度( ) ; 离子符号,浓度 ; 离子符号,浓度( )。
(3)试确定K+是否存在,( )(填“是”或“否”),判断的理由是( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.某溶液中可能存在
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaC12溶液,无沉淀生成;
③向所得溶液中继续滴中淀粉溶液,溶液不变蓝色。
据此可推断:该溶液中肯定不存在的离子组是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、A13+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无须检验就可判断其中必有的两种物质是__________和______。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体。则X_________(填字母)。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.今有一混合物的水溶液,可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO


(1)第一份加入AgNO3溶液有沉淀产生;
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.图中X、Y、Z、 W是地壳含量前四位(不按顺序)的元素组成的单质,其它为化合物,A有磁性。它们之间存在如下转化关系(部分产物已略去)。
回答下列问题:
(1)组成单质Y的元素在周期表中的位置是( ), M的化学式是( );
(2)胶体的应用非常广泛,早在150年前的1862年,英国科学家格雷阿姆就提出了"胶体"的概念,R胶体中分散质直径大小范围为: ( ),可利用( )区分胶体和溶液;
(3)已知A与2.7g W反应转化为X时(所有物质均为固体),放出akJ热量,写出该反应的热化学方程式:(
);
(4)写出A和足量D的稀溶液反应生成G的离子方程式:( )
(5)简述检验G溶液中的金属阳离子的实验方法(操作、现象、结论)
(6)常温下,向物质的量浓度为0.04mol/L的G溶液中,加NaOH溶液调节pH,当
pH= ( )时,开始有沉淀生成。(已知25℃时,Ksp[Fe(OH)3]=4.0×10-38)
正确答案
(1)第二周期第ⅥA族; Na2SiO3
(2)1 nm~100 nm; 丁达尔效应
(5)取少量

解析
解析已在路上飞奔,马上就到!
知识点
13.有一未知的无色溶液.只可能含有以下离子中的若于种(忽略由水电离产生的H+、OH一):

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.取少量溶液,加入KSCN溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请回答:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是( )(写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是( )。
(3)将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为
( )。
(4)甲同学最终确定原溶液中所含阳离子是( ),阴离子是( )。(写离子符号)
(5)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为( ) g。
(6)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是( )
正确答案
(1)
(2)
(3)
(4)
(5)1.6
(6)D
解析
解析已在路上飞奔,马上就到!
知识点
12.有一瓶无色溶液,可能含有Na+、K+、Al3+、Mg2+、NH4+、Cl—、SO42—、HCO3—、MnO4—离子中的几种。为确定其成分,进行如下实验:
①取少许溶液,逐渐加入过量的Na2O2固体,产生无色无味的气体和白色沉淀且白色沉淀逐渐增多后又部分溶解;②另取部分溶液,加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀产生;③用洁净的铂丝蘸取原溶液在酒精灯火焰上灼烧,观察到黄色火焰。下列推断正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析





















