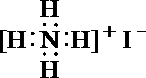- 氢键的存在对物质性质的影响
- 共39题
2.化学学
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.下列叙述正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
5. 2013年诺贝尔化学奖授予“为复杂化学系统创立了多尺度模型”的三位美国科学家,使化学家能通过计算机模拟,更快获得比传统实验更精准的预测结果。以下说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.三聚氰胺(结构如图)六元环中的碳氮键键长相等。与制酚醛树脂相似,甲醛与三聚氰胺缩聚也可制得三聚氰胺树脂。以下关于三聚氰胺的叙述肯定错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
7.描述硅原子核外电子运动说法错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
25.在下列各变化中,E为常温下无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。
回答下列问题:
(1)写出H的电子式:________________。
(2)若反应①在加热条件下进行,A为单质,C为无色有刺激性气味的气体,D为无色无味的气体,且C、D两种气体均能使澄清的石灰水变浑浊,则反应①的化学方程式是_______________。
①实验需要检验出C、D、E三种气体产物,三种气体检验的先后顺序是__________(用化学式填空),在检验D气体前,需除去C气体,所用试剂是_______,反应的离子方程式是_____________________________。
②已知:A(s)+O2(g) =AO2(g) △H=-393.5kJ·mol-1
2A(s)+O2(g) =2AO(g) △H=-221.0kJ·mol-1
则AO的燃烧热的热化学方程式________________.
③AO2在自然界循环时可与碳酸钙反应,碳酸钙是一种难溶物质,它的Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为_________。
(3)若反应①在溶液中进行,A是一种常见一元强碱,B是一种酸式盐,D是一种气体,且B遇盐酸产生能使品红溶液褪色的气体,在加热条件下,当A过量时,反应①的离子方程式是_____________。
(4)若反应①在溶液中进行,A是一种强酸,B是一种含有两种金属元素的盐,且B的水溶液显碱性,A、B均由短周期元素组成,当A过量时,C及D均易溶于水,则A过量时反应①的离子方程式是_______________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
4.在通常条件下,下列各组物质的性质排列正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
早期发现的一种天然二十面体准晶颗粒由AI.Cu.Fe 三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过 方法区分晶体.准晶体和非晶体。
(2)基态 Fe原子有 个未成对电子,Fe3+的电子排布式为 可用硫氰化钾检验Fe3+,形成的配合物的颜色为_ 。
(3)新制备的Cu(OH)2可将乙醛〔CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为_ ,1mol乙醛分子中含有的σ健的数目为_ 。乙酸的沸点明显高于乙醛,其主要原因是 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有_ 个铜原子。
(4)Al单质为面心立方晶体,,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为_ 。列式表示Al单质的密度_ g·cm-3〔不必计算出结果)。
正确答案
(1)X-射线衍射
(2)4 
(3)

6

16
(4) 12

解析
略
知识点
中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据。这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法。下列说法中正确的是
正确答案
解析
略
知识点
4.已知某种双子叶植物的阔叶和窄叶由一对等位基因控制,现对该植物的某个种群进行调查,发现有60%的植株表现为窄叶,余者表现为阔叶。从该种群中分别取两种性状的足够样本让其自交,发现约有30%阔叶植株的子代出现窄叶植株,而窄叶植株的子代未发现阔叶植株。以下结论错误的是 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析