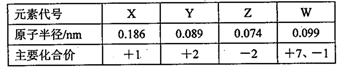- 元素周期律的应用
- 共230题
有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)X元素在周期表中的位置 ;其气态氢化物的电子式 ;
(2)工业上制取Y单质常用的方法是 ;
(3)Y离子半径比Z离子的半径 (填“小”或“大”);
(4)Z的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式 ;
(5) Z的某种盐是常用的净水剂,用离子方程式表示其净水原理 ;
(6)举出实例说明M的非金属性比X强(用化学方程式表示) 。
正确答案
见解析。
解析
(1)第二周期第ⅣA族;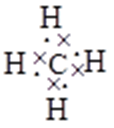
(2)电解法;
(3)大 ;
(4)
(5)Al3+ + 3H2O 
(6)Na2CO3 + 2HClO4 = 2 NaClO4 + CO2↑ + H2O 。
知识点
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素。其中Z是金属,W的单质是淡黄色固体,X、Y、W在周期表中的相对位置关系如右下图所示,下列说法一定正确的是
正确答案
解析
略。
知识点
下列说法正确的是
正确答案
解析
略。
知识点
A、B、C、D、E为原子序数相邻且依次递增的同一短周期元素,下列说法正确的是(m、n均为正整数)
正确答案
解析
略
知识点
短周期主族元素A、B、C、D的原子序数依次增大,它们的原子核外电子层数之和为7。B的化合物种类繁多,数目庞大。A与D能形成原子个数比为1︰1和2︰1的化合物。
(1)人类六大营养素中,只由A、B、D三种元素组成的有 (填其中一种营养素的名称);只由A、B、D三种元素组成的化合物中,相对分子质量最小的是 ;
由A、B、C三种元素按原子数目比5︰1︰1组成分子E,请写出E的电子式__________。
(2)由A、C两种元素组成的一种常见气态化合物,其分子的空间构型为________,工业上合成该气体的化学方程式为 。
(3)只由A、C、D组成的盐,发生水解反应的离子方程式为 。
(4)甲、乙两种化合物都只由A、B、C、D四种元素组成,它们既能与盐酸反应又能与烧碱溶液反应。其中,甲为无机酸式盐,甲与稀烧碱溶液反应的离子方程式为 ;乙为天然蛋白质水解的相对分子质量最小的产物,其结构简式为 。
正确答案
见解析。
解析
(1) 糖类(或:油脂); HCHO(或:甲醛) ; 
(2)三角锥型 ; 
(3)
(4)

知识点
几种短周期元素的原子半径及主要化合价如下表,由此可知
正确答案
解析
略。
知识点
前四周期原子序数依次增大的元素A,B,C,D中, A是电负性最大的元素,并且A-和B+的电子数相差为8;C和D原子序数相差为2,且都与B位于同一周期,C元素的次外层电子数是最外层电子数的7倍。
回答下列问题:
(1)D的价层电子排布式为_______。
(2)请用电子式表示A、B两元素形成化合物的过程。 。
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
①该化合物的化学式为_________;D的配位数为_______;
②列式计算该晶体的密度___ ____g·cm-3。
(4)A-、B+和C3+三种离子组成的化合物B3CA6,其中化学键的类型有_ ____;该化合物中存在一个复杂离子,该离子的化学式为___ ____,配位数是_ __。
正确答案
答案:
(1)3d84s2(该空1分,其余每空2分)

(3)①K2NiF4; 6 ②=3.4
(4)离子键、配位键; [FeF6]3-; 6
解析
略
知识点
O、W、X、Y、Z五种短周期元素在元素周期表中的相对位置如图所示,W是大气中含量最高的元素,由此可知
正确答案
解析
略。
知识点
已知短周期元素中,元素Q、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。W与Q可以形成一种新型的陶瓷材料。W的氯化物分子呈正四面体结构。下列推断中错误的是
正确答案
解析
略
知识点
A、B、C、D、E是原子序数依次增大的五种元素。B元素原子最外层电子数比内层多3个,C、D元素同主族且原子序数D为C的二倍,E元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,回答下列问题。
(1)E元素基态原子的外围电子排布图为_______。
(2)元素B、C、D的第一电离能由小到大排列顺序为_______(用元素符号表示)。
(3) DC3冷凝可形成一种D、C相间的六元环结构的三聚体,其中D原子的杂化方式为_______。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和1:2,两种化合物可任意比互溶,其主要原因是_______。
(5)A、B、C、D、E五种元素组成某配位化合物X,其原子个数比为18:6:4:1:1,该配位化合物X的化学式为_______。
(6) Sb的一种氧化物高于843K时会转化为长链的大分子,其结构片段如图,则该分子中Sb和O的原子个数比为_______。
正确答案
(1)
(2)S<O<N
(3)sp3
(4)H2O与H2O2之间形成氢键
(5)[Ni(NH3)6]SO4
(6)2∶3
解析
略。
知识点
扫码查看完整答案与解析