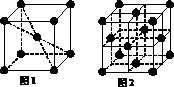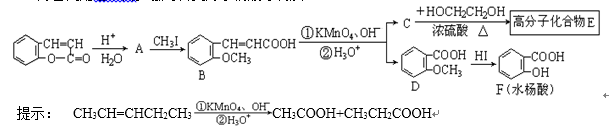- 化学键与物质的性质
- 共213题
20. X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)Y基态原子的电子排布式是 ;Z所在周期中第一电离能最大的元素是 。
(2)XY2- 离子的立体构型是 ;R2+的水合离子中,提供孤电子 对的原子是 。
(3)Z与某元素形成的化合物的晶胞如下图所示,晶胞中阴离子与阳离子的个数比是 。
(4)将R单质的粉末加入XH3的浓溶液中,通入Y2,充分反应后溶液呈深蓝色,该反应的离子方程式是 。
正确答案
(1)1s22s22p4 Cl
(2)V形 O
(3)2:1
(4)2Cu+8NH3·H2O+O2
解析
解析已在路上飞奔,马上就到!
知识点
原子序数依次增
回答下列问题:
(1)元素a为 ,c为 ;
(2)由这些元素形成的双原子分子为 ;
(3)由这些元素形成的三原子分子中,分子的空间结构属于直线型的是 ,非直线型的是 (写两种);[来源:学科网ZXXK]
(4)这些元素的单质或由它们形成的AB型化合物中,其晶体类型属于原子晶体的是 ,离子晶体的是 ,金属晶体的是 ,分子晶体的是 ;(每空填一种)
(5)元素a和b形成的一种化合物与c和d形成的一种化合物发生的反应常用于防毒面具,该反应的化学方程式为 。
正确答案
(1)碳,钠
(2)CO
(3)CO2、CS2;ClO2、SO2
(4)金刚石,NaCl,Na,S
(5)
解析
原子序数依次增大的短周期元素a、b、c、d和e中,a的最外层电子数为其周期数的二倍;b和d的A2B型氢化物均为V形分子,c的+1价离子比e的-1价离子少8个电子。可推出元素a为C; b为O; 元素c为钠,d为硫,e为氯。由这些元素形成的双原子分子为CO;由这些元素形成的三原子分子中,分子的空间结构属于直线形的是CO2 ,非直线形的是: H2O H2S。这些元素的单质或由他们形成的AB型化合物中,其晶体类型属于原子晶体的是_金刚石,离子晶体的是NaCl ,金属晶体的是Na ,分子晶体的是 S 或CO ;(每空填一种),元素a和b形成的一种化合物与c和b形成的一种化合物发生的反应常用于防毒面具中,该反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2
知识点
根据有关的概念,推断下列说法中正确的是( )
正确答案
解析
略
知识点
下面关于SiO2晶体网状结构的叙述正确的是
正确答案
解析
二氧化硅是原子晶体,结构为空间网状,存在硅氧四面体结构,硅处于中心,氧处于4个顶角所以A项错误;在SiO2晶体中,每6个Si和6个O形成一个12元环(最小环),所以D对,B、C都错误!
知识点
如图是某无机化合物的二聚分子,该分子中A、B两种元素都是第三周期的元素,分子中所有原子的最外层电子都达到8个电子的稳定结构。下列说法不正确的是
正确答案
解析
略
知识点
30. 【化学—物质结构与性质】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)请写出元素N的基态原子电子排布式( )。
(2)元素B、G形成的单质熔点更高的是_______(填化学式),原因是_____________________
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是__________(填“极性”或“非极性”)分子。根据等电子原理:NO2+ 中氮原子的杂化类型是( ), 1 mol O22+ 中含有π键的数目为 ( )。
(4)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有___________(填序号),CS2分子的空间构型是__________。
(5)元素N可以形成分子式为Co(NH3)5BrSO4,配位数均为6的两种配合物,若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为( ) 。
31.【化学—有机化学基础】
物质A有如下合成路线:
(1)A的分子式为( ),
(2)A→C的化学方程式为( ),
B和D反应的化学方程式为( ),
(3)B的同分异构体F、G能与浓溴水反应,且结构中均含有一个-CH3,已知1molF消耗3molBr2,1molG消耗2molBr2,则F、G的结构简式为F( ),G( )。
(4)我们把与醛基相连的碳原子上的氢原子称为α-H,含有α-H的醛自身可发生反应,如:
则通过一定的反应可以生成A的两种醛分别为( )和( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28、29题为物理题,第30、31题为化学题,考生从两道物理题、化学题中各任选一题作答。
30.[化学---物质结构与性质]
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)P、S、Cl三种元素中,第一电离能最小的是( ) 。
(2)PCl3和CH4中心原子的杂化类型相同,PCl3分子的空间构型是( ) 。
(3)钛原子的电子排布式为 ( ) 。在浓的TiCl3溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,将1 mol该物质溶于水,加入足量硝酸银溶液,立即产生1 mol氯化银沉淀,则该配合物阳离子的化学式为 ( ),形成该离子时提供孤电子对的分子或离子是( ) (填化学式)。
(4)铁元素在1183 K以下形成的晶体的基本结构
单元如图1所示,1183 K以上转变为图2所示结构的
基本结构单元。两种晶体的基本结构单元中的原子个
数之比为( ) 。
31.[化学---有机化学基础]
香豆素是广泛存在于植物中的一类芳香族化合物,具有抗菌和消炎作用。它的核心结构是芳香内酯,其结构简式为
(1)下列关于芳香内酯的叙述正确的是( ) 。
A.分子式为C9H8O2 B.可发生加聚反应
C.能与溴水发生反应 D.1mol芳香内酯最多能和5mol氢气发生加成反应
(2)写出芳香内酯在酸性条件下水解的化学方程式:( )。
(3)芳香内酯经下列步骤可转变为水杨酸等物质:
请回答下列问题:
① 指出D → F的反应类型为( ) 。
② 请写出反应C → E的化学方程式:( ) 。
③在一定条件下阿司匹林(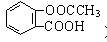
a.三氯化铁溶液 b.碳酸氢钠溶液 c.石蕊试液 d.氢氧化钠溶液
④水杨酸的同分异构体中含有酚羟基且属于酯类的共有3种,写出其中一种同分异构体的结构简式( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
第29、30题为物理题,第31、32题为化学题,考生从两道物理题、两道化学题中各任选一题作答。
31.[化学——物质结构与性质]
由Cu、N、B等元素组成的新型材料有着广泛用途。
(1)基态Cu+的核外电子排布式为___________。高温下CuO能转化为Cu2O,试从原子结构角度解释其原因:_______________________。
(2)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,它属于___________晶体。
(3)化合物A(H3BNH3)是一种潜在的储氢材料,它可由六元环状化合物(HB=NH)3通过
反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3而制得。
①与上述化学方程式有关的叙述不平碜的是——(填标号)。
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
②1 mol(HB=NH)3分子中有_________mol
(4)在硼酸盐中,阴离子有链状、立体状等多种结构形式。图(a)是一种长链结构的硼酸根,则该硼酸根离子的化学符号为_________。图(b)是硼砂晶体中阴离子的立体状结构,
其中硼原子采取的杂化轨道类型有__________________。
32.[化学一有机化学基础]
甲苯是一种重要的化工原料。以甲苯为原料通过以下转化可得多种化工产品。
(1)写出指定物质的结构简式:A______________,M______________。
(2)C中苯环上的侧链所含官能团的名称是_______________________。
(3)E→F的反应类型是______________。
(4)关于B的说法正确的是__________(填标号)。
a.能发生银镜反应 b.遇FeCl3溶液发生显色反应
c.能发生消去反应 d.能与H2发生加成反应
(5)写出D→E反应的化学方程式:_______________________。
(6)写出符合下列条件的A的同分异构体的结构简式:__________________。
a.苯环上一氯代物只有3种
b.不能与新制氢氧化铜悬浊液反应

甲苯是一种重要的化工原料。以甲苯为原料通过以下转化可得多种化工产品。

(2)C中苯环上的侧链所含官能团的名称是_______________________。
(3)E→F的反应类型是______________。
(4)关于B的说法正确的是__________(填标号)。
a.能发生银镜反应 b.遇FeCl3溶液发生显色反应
c.能发生消去反应 d.能与H2发生加成反应
(5)写出D→E反应的化学方程式:_______________________。
(6)写出符合下列条件的A的同分异构体的结构简式:__________________。
a.苯环上一氯代物只有3种
b.不能与新制氢氧化铜悬浊液反应
正确答案
第28、29题为物理题,第30、31题为化学题,考生从两道物理题、两道化学题中各任选一题作答。
30.【化学——物质结构与性质】
(1)下列分子中,属于平面型构型的有________。
A.CCl4 B.PH3 C.BBr3 D.COCl2
(2)H2O分子间因存在“氢键”的作用而彼此结合形成(H2O)n。在该分子形成的晶体中每个H2O分子被4个H2O分子包围形成变形的四面体,通过“氢键”相互连接成庞大的分子晶体,其结构示意图如图所示,试填空。
①含1molH2O的该晶体中有_____个“氢键”。
②请说明H2O比H2S的沸点高的原因___________________。
(3)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子的价电子排布式为________;一种铜金合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心、Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为________;该晶体中,原子之间的作用力是_______;
(4)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构相似,该晶体储氢后的化学式应为________。
31.【化学——有机化学基础】A、B、C、D、E均为有机物,它们具有下图的转化关系:
已知:C能与NaHCO3发生反应,C、D相对分子质量相等,E能发生银镜反应,相对分子质量为74。
请回答下列问题:
(1)写出C的名称:( ),E中含有的官能团名称( )、( );
写出有机物B可能发生的两种反应类型:( );
(2)写出反应②的化学方程式:( );
(3)A的结构简式为( );
(4)写出两种同时符合下列条件的B的同分异构体的结构简式:( ) 、( )。
①苯环上有二个间位取代基; ②属于芳香酸酯; ③能与FeCl3显色
30.【化学——物质结构与性质】
(1)下列分子中,属于平面型构型的有________。

已知:C能与NaHCO3发生反应,C、D相对分子质量相等,E能发生银镜反应,相对分子质量为74。
请回答下列问题:
(1)写出C的名称: ,E中含有的官能团名称 、 ;
写出有机物B可能发生的两种反应类型: ;
(2)写出反应②的化学方程式: ;
(3)A的结构简式为 ;
(4)写出两种同时符合下列条件的B的同分异构体的结构简式: 、 。
①苯环上有二个间位取代基; ②属于芳香酸酯; ③能与FeCl3显色
正确答案
正确答案
7. 下列说法中,正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析