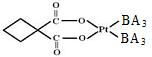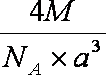- 化学方程式的书写
- 共78题
已知A、B为单质,C为化合物。能实现下述转化关系的是
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
正确答案
解析
略
知识点
前四周期的五种元素A、B、C、D、E原子序数逐渐变大,其中C、D元素同主族且原子序数D为C的二倍,B的第一电离能大于C,E原子的外围电子排布为(n-l)d (n+6)ns1。由它们组成的配位化合物X为深蓝色的结晶水合物,其原子个数比为14:4:5:1:1。回答下列问题。
(1)该配位化合物X的化学式为 。
(2)碳铂是一种含BA3分子的具有抗癌活性的金属配合物,碳铂的结构如图,其中碳原子的杂化方式有 。
(3)D元素原子的最外层电子轨道表式为 。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,两种化合物可任意比互溶,解释其主要原因为 。
(5) 元素B的单质可以和电石(CaC2)反应,生成氰氨化钙(CaCN2), 氰氨化钙和水反应可生成NH3。与CN22-互为等电子体的分子有 (填写一种化学式即可);写出CaCN2水解反应的化学方程式 。
(6)A元素与E元素可形成一种红色离子化合物Y,其原子个数比为1:1,该化合物Y可与稀硝酸反应,生成一种蓝色溶液和两种无色气体(其中一种为A元素的单质),写出该反应的化学方程式 。单质E的晶胞如图所示,若设该晶胞的边长为acm,阿伏加德罗常数为NA,单质E的摩尔质量为Mg/mol,则表示该晶胞密度的计算式为ρ= g/cm3。
正确答案
(1)Cu(NH3)4SO4`H2O (1分)
(2)sp3杂化和sp2杂化
(3)
(4)H2O与H2O2之间形成氢键
(5)CO2或N2O ; CaCN2+3H2O=CaCO3+2NH3↑
(6)6CuH+16HNO3=6Cu(NO3)2+3H2↑+4NO↑+8H2O;
解析
略
知识点
27.某回收废料中含Al2O3、Fe2O3、Co2O3·CoO多种金属氧化物,某实验室科技人员欲将之分离并制备有关物质,设计流程如下图所示:
(1)过程②的离子方程式为 。
(2)过程④会产生有毒气体,反应的化学方程式为 。
(3)过程⑥用于制备绿色水处理剂,反应的离子方程式为 。
(4)过程⑦中碳酸钠溶液起的作用是 。
(5)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。下表是粉红色的CoCl2·6H2O晶体受热分解时的情况:
认真分析以上数据,填写下列空白。③物质的化学式是____________。写出CoCl2·6H2O晶体受热分解生成②的化学反应方程式 。
正确答案
(1)AlO2-+2H2O +CO2 =Al(OH)3↓+HCO3-
(2)Co2O3·CoO+8HCl=3CoCl2+Cl2↑+ 4H2O
(3)2Fe(OH)3 +3ClO-+ 4OH-=2FeO42-+3Cl-+5H2O
(4)调整pH,提供碳酸根离子,使Co2+沉淀为CoCO3
(5)CoCl2·H2O CoCl2·6H2O
解析
略
知识点
解释下列事实的方程式正确的是
正确答案
解析
略。
知识点
著名化学家徐光宪获得2008年度“国家最高科学技术奖”,以表彰他在稀土串级萃取理论方面所作出的贡献。稀土铈(Ce)元素主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是
正确答案
解析
略
知识点
扫码查看完整答案与解析