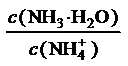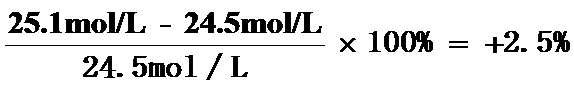- 有机化合物的异构现象
- 共52题
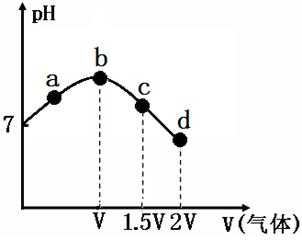
6.常温常压下,将NH3缓慢通入饱和食盐水中至饱和,然后向所得溶液中缓慢通入CO2,整个实验进程中溶液的pH随通入气体体积的变化曲线如图所示(实验中不考虑氨水的挥发)。下列叙述不正确的是()
正确答案
解析
A.a点到b点是向饱和氯化钠溶液中通入氨气达到饱和,溶液中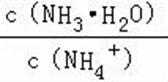
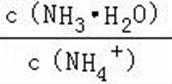
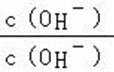
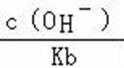
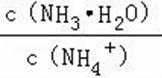
B.b到c点是一水合氨和通入的二氧化碳反应得到碳酸铵溶液,c到d点是碳酸铵和二氧化碳反应生成碳酸氢铵,在溶液中依据溶解度大小最后反应生成碳酸氢钠晶体和氯化铵溶液,由图可知(NH4)2CO3溶液显碱性、NH4Cl溶液显酸性,故B正确;
C.c点所示溶液是碳酸铵溶液,图象分析可知溶液显碱性,离子浓度大小为:c(NH4+)>c(CO32﹣)>c(OH﹣)>c(H+),故C正确;
D.d点是氯化铵溶液和碳酸氢钠饱和溶液,溶液中存在氮物料守恒,碳元素守恒,析出碳酸氢钠,则溶液中氯离子大于溶液中钠离子,c(NH4+)+c(NH3•H2O)>c(HCO3﹣)+c(CO32﹣)+c(H2CO3),故D错误。
故选D。
考查方向
解题思路
A.a点到b点是向饱和氯化钠溶液中通入氨气达到饱和,溶液中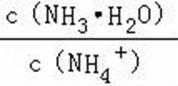
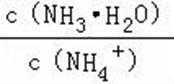
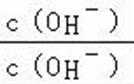
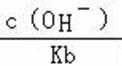
B.b到c点是一水合氨和通入的二氧化碳反应得到碳酸铵溶液,c到d点是碳酸铵和二氧化碳反应生成碳酸氢铵,在溶液中依据溶解度大小最后反应生成碳酸氢钠晶体和氯化铵溶液;
C.c点所示溶液是碳酸铵溶液,图象分析可知溶液显碱性;
D.d点是氯化铵溶液和碳酸氢钠饱和溶液,溶液中存在氮物料守恒,碳元素守恒,析出碳酸氢钠,则溶液中氯离子大于溶液中钠离子。
易错点
本题考查了侯氏制碱法的原理过程分析,盐类水解原理、图象变化和溶液酸碱性的判断等知识,注意产物的理解应用,题目难度中等。
知识点
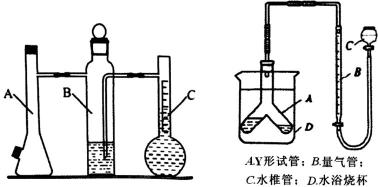
9.利用下左图所示实验装置可以测定常温常压下气体的摩尔体积。
甲同学利用如上左图装置,根据下列步骤完成实验:①装配好装置,作气密性检查。②用砂纸擦去镁带表面的氧化物,然后取0.108g的镁带。③取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口。④用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平。⑤用注射器吸取10mL3mol·L-1硫酸溶液,用针头扎进A瓶加料口橡皮塞,将硫酸注入A瓶,注入后迅速拔出针头。⑥当镁带完全反应后,读取C瓶中液体的体积,记录数据。⑦用注射器从A瓶加料口处抽出8.0mL气体,使B瓶中导管内外液面持平。⑧读出C瓶中液体体积是115.0mL。完成下列填空:
(1)常温常压下的压强为________,温度为_______。
(2)在常温常压下气体摩尔体积理论值约为24.5L/mol,甲同学测出此条件下lmol气体的体积为________,计算此次实验的相对误差为________%(保留2位有效数字)。引起该误差的可能原因是_________。
a.镁带中含铝;
b.没有除去镁带表面的氧化物;
c.反应放热;
d.所用硫酸的量不足
(3) 丙同学提出可用如上右图装置完成该实验。该装置气密性的检查方法是:_____________。
(4)与原方案装置相比,丙同学使用的装置实验精度更高。请说明理由(回答两条)____________________________________,_____________________________________。
正确答案
(1)101KPa ,25℃(298K)
(2)25.1L 2.5 ac
(3)快速上移或下移水准管,若量气管内液面最终与水准管液面存在稳定的液面差即气密性良好。(其它合理答案也给分下同)
(4)压强:该装置能更简便、更准确地控制气压不变;温度:借助水浴装置,实验温度更接近常温(水浴能减小反应放热带来的误差);精度:量气管由滴定管改制,读数更精确。
解析
(1)常温常压下的压强为101KPa,温度为25℃,
故答案为:101KPa;25℃;
(2)生成氢气的体积为115mL-10mL+8mL=113mL,0.108gMg完全反应得到氢气为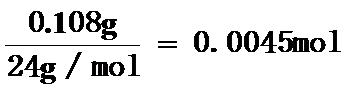
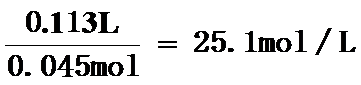
反应放热,气体体积热胀冷缩,Mg中含有Al时,生成氢气体积偏大,导致测定值偏大,没有除去镁带表面的氧化物、所用硫酸的量不足,导致生成氢气体积偏小,导致测定值偏小,故选ac,
故答案为:25.1L;+2.5;ac;
(3)该装置气密性的检查方法是:从水准管中加入水,快速上移或下移水准管,若量气管内液面最终与水准管液面存在稳定的液面差即气密性良好,
故答案为:从水准管中加入水,快速上移或下移水准管,若量气管内液面最终与水准管液面存在稳定的液面差即气密性良好;
(4)与图1相比,该装置能更简便、更准确地控制气压不变,借助水浴装置,实验温度更接近常温(水浴能减小反应放热带来的误差),量气管由滴定管改制,读数更精确,
故答案为:该装置能更简便、更准确地控制气压不变;量气管由滴定管改制,读数更精确等.
考查方向
解题思路
(1)常温常压是指25℃,101KPa;
(2)加入的硫酸溶液体积也计算在量气瓶中的液体体积,反应后抽出的气体体积调整液面平衡,所以需要在气体体积中加入抽出气体的体积,可得生成氢气的体积为,根据Mg的质量计算生成氢气物质的量,进而计算气体摩尔体积;
相对误差是指测量所造成的绝对误差与真值之比,再乘以100%所得的数值;
反应放热,气体体积热胀冷缩,Mg中含有Al时,生成氢气体积偏大,导致测定值偏大,没有除去镁带表面的氧化物、所用硫酸的量不足,导致生成氢气体积偏小,导致测定值偏小;
(3)利用液封气体,形成量气管内与水准管内液面存高度差,一定时间内液面差不变,说明气密性良好;
(4)与图1相比,该装置能更简便、更准确地控制气压不变;量气管由滴定管改制,读数更精确等.
易错点
本题中对于测定原理的理解会影响产生氢气的体积数据计算准确性,从而影响到下面的相对误差计算。
知识点
8.下列有关实验的说法正确的是( )
正确答案
解析
A选项容量瓶标有温度、规格、刻度线,量筒标有温度、规格,滴定管温度、规格,量筒、容量瓶无“0”刻度,滴定管有“0”刻度在最上面,使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗,故A正确;
B选项铝放在浓硝酸中会钝化,Al2O3与CuSO4不反应,所以放入硫酸铜中没有什么现象,B错误。
C选项若用浓盐酸配制1:1(体积比)的稀盐酸,通常使用量筒和烧杯即可,不需要使用容量瓶,故C错误
D选项固体碘单质受热易升华为其物理性质,不能说明碘单质的热稳定性较差,D错误。
本题正确答案是A
考查方向
解题思路
A选项容量瓶标有温度、规格、刻度线,量筒标有温度、规格,滴定管温度、规格,量筒、容量瓶无“0”刻度,滴定管有“0”刻度在最上面,使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗,故A正确;
B选项铝放在浓硝酸中会钝化,Al2O3与CuSO4不反应,所以放入硫酸铜中没有什么现象,B错误。
C选项若用浓盐酸配制1:1(体积比)的稀盐酸,通常使用量筒和烧杯即可,不需要使用容量瓶,故C错误。
D选项固体碘单质受热易升华为其物理性质,不能说明碘单质的热稳定性较差,D错误。
B选项不正确,C选项不正确,D选项不正确,所有选A选项。
易错点
实验仪器如计量仪器及使用方法和误差分析。
知识点
四氯化锡(SnCl4)是合成有机锡化合物的原料,其熔点为﹣33℃,沸点为114℃,在潮湿的空气中强烈水解产生有刺激性的白色烟雾,产物之一为SnO2。实验室制备四氯化锡的操作是:将金属锡熔融,然后泼入冷水,制成锡花,将干燥的锡花加入反应器中;再向反应器中缓慢地通入干燥的氯气。
图1 图2
I.图1是实验室制备干燥氯气的实验装置(夹持装置已略)
II.图2是蒸馏SnCl4的装置
17.a的仪器名称 该装置制备氯气选用的药品为漂粉精固体[主要成分Ca(ClO)2]和浓盐酸,B中发生反应的化学方程式为
18.装置C中饱和食盐水的作用 同时装置C亦是安全瓶,能检测实验进行时D中是否发生堵塞,请写出发生堵塞时C 中的现象
19.试剂X可能为 (填写字母)
20.四氯化锡在潮湿空气中水解的化学方程式
21.用锡花代替锡粒的目的是
22.①蒸馏前若发现烧瓶中液体呈黄色,可采取的措施是
②该装置尚有两处不当之处,它们分别是 ,
③写出III中发生反应的离子方程式
正确答案
分液漏斗Ca(ClO)2+4HCl(浓)= CaCl2+2Cl2↑+2H2O;(2分,无“浓”或“↑”扣1分)[来源:学科网]
解析
由仪器结构特征,可知仪器a为分液漏斗;Ca(ClO)2和浓盐酸反应生成氯化钙、氯气与水,反应方程式为:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O,
故答案为:分液漏斗;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
考查方向
解题思路
仪器a为分液漏斗;Ca(ClO)2和浓盐酸反应生成氯化钙、氯气与水;
易错点
四氯化锡遇水强烈水解;U形管中试剂X干燥氯气,不能为碱性干燥剂;若D中发生堵塞,装置内气压增大,c中长颈漏斗中液面上升。
正确答案
除去Cl2中的HCl ; 长颈漏斗中液面上升,形成水柱
解析
制备的氯气中含有HCl,饱和食盐水除去Cl2中的HCl;若D中发生堵塞,装置内气压增大,c中长颈漏斗中液面上升,形成水柱,
故答案为:除去Cl2中的HCl; 长颈漏斗中液面上升,形成水柱;
考查方向
解题思路
制备的氯气中含有HCl,饱和食盐水除去Cl2中的HCl;若D中发生堵塞,装置内气压增大,c中食盐水会被压入长颈漏斗中;
易错点
四氯化锡遇水强烈水解;U形管中试剂X干燥氯气,不能为碱性干燥剂;若D中发生堵塞,装置内气压增大,c中长颈漏斗中液面上升。
正确答案
解析
四氯化锡极易水解,通入的氯气应干燥,U形管中试剂X干燥氯气,不能为碱性干燥剂,可以吸收氯气,不能为液体干燥剂,否则气体不能通过,可以选择氯化钙、五氧化二磷,
故答案为:AD;
考查方向
解题思路
四氯化锡极易水解,通入的氯气应干燥,U形管中试剂X干燥氯气,不能为碱性干燥剂,可以吸收氯气,不能为液体干燥剂,否则气体不能通过;
易错点
四氯化锡遇水强烈水解;U形管中试剂X干燥氯气,不能为碱性干燥剂;若D中发生堵塞,装置内气压增大,c中长颈漏斗中液面上升。
正确答案
SnCl4+2H2O=SnO2+4HCl
解析
四氯化锡遇水强烈水解,根据水解原理可知,应生成Sn(OH)4、HCl,产物之一是固态二氧化锡,说明Sn(OH)4分解生成SnO2与H2O,故水解生成SnO2、HCl,反应方程式为:SnCl4+2H2O=SnO2+4HCl,
故答案为:SnCl4+2H2O=SnO2+4HCl;
考查方向
解题思路
四氯化锡遇水强烈水解,根据水解原理可知,应生成Sn(OH)4、HCl,产物之一是固态二氧化锡,说明Sn(OH)4分解生成SnO2与H2O,故水解生成SnO2、HCl;
易错点
四氯化锡遇水强烈水解;U形管中试剂X干燥氯气,不能为碱性干燥剂;若D中发生堵塞,装置内气压增大,c中长颈漏斗中液面上升。
正确答案
增大与氯气的接触面积,加快反应速率
解析
用锡花代替锡粒的目的是:增大与氯气的接触面积,加快反应速率,故答案为:增大与氯气的接触面积,加快反应速率;
考查方向
解题思路
增大与氯气的接触面积,加快反应速率;
易错点
四氯化锡遇水强烈水解;U形管中试剂X干燥氯气,不能为碱性干燥剂;若D中发生堵塞,装置内气压增大,c中长颈漏斗中液面上升。
正确答案
① 加入锡花
② 温度计水银球位置不对 , Ⅱ和Ⅲ之间缺少干燥装置.
③ Cl2+2OH—=Cl—+ClO—+H2O
解析
①蒸馏前若发现烧瓶中液体呈黄色,说明还有氯气未反应,可采取的措施是加入锡花继续反应,
故答案为:加入锡花;
②温度计水银球位置不对,应再蒸馏烧瓶支管口处;四氯化锡遇水强烈水解,而装置Ⅲ中的水蒸气易进入Ⅱ中,使其发生水解,二者之间缺少干燥装置;
故答案为:温度计水银球位置不对;Ⅱ和Ⅲ之间缺少干燥装置;
③III中主要吸收未反应的氯气,防止污染空气,反应离子方程式为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,
故答案为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O.
考查方向
解题思路
①蒸馏前若发现烧瓶中液体呈黄色,说明还有氯气未反应,加入锡花继续反应;
②温度计水银球位置不对;四氯化锡遇水强烈水解,而装置Ⅲ中的水蒸气易进入Ⅱ中,使其发生水解;
③III中主要吸收未反应的氯气,防止污染空气.
易错点
四氯化锡遇水强烈水解;U形管中试剂X干燥氯气,不能为碱性干燥剂;若D中发生堵塞,装置内气压增大,c中长颈漏斗中液面上升。
5.过量的下列溶液与水杨酸(
正确答案
解析
A.水杨酸与NaHCO3溶液反应时只是-COOH作用转化为-COONa,产物的分子式为C7H5O3Na,A正确;
B.水杨酸与Na2CO3溶液反应时-COOH、-OH均反应,生成产物的分子式为C7H4O3Na2,B错误;
C.水杨酸与NaOH溶液反应时-COOH、-OH均反应,生成产物的分子式为C7H4O3Na2,C错误;
D.与NaCl溶液不反应,D错误;
故选A。
考查方向
解题思路
A.水杨酸与NaHCO3溶液反应时只是-COOH作用转化为-COONa,产物的分子式为C7H5O3Na;
B.水杨酸与Na2CO3溶液反应时-COOH、-OH均反应,生成产物的分子式为C7H4O3Na2;
C.水杨酸与NaOH溶液反应时-COOH、-OH均反应,生成产物的分子式为C7H4O3Na2;
D.与NaCl溶液不反应;
易错点
本题考查有机物的结构和性质,题目难度不大,注意酚羟基、羧基与碳酸酸性的强弱比较,为解答该题的关键。
知识点
扫码查看完整答案与解析