- 有机化合物的异构现象
- 共52题
4.下列实验现象与实验解释正确的是
正确答案
C
解析
分离碘的CCl4溶液,是利用CCl4沸点低、易挥发,A错误。KMnO4具有强氧化性,能氧化乙醇,葡萄糖为多羟基的醛也能被氧化,B错误。蔗糖与浓硫酸的反应中,使蔗糖脱水碳化、与脱水生成的C反应体现了其强氧化性,C正确。加入盐酸酸化的Ba(NO3)2因有H+与NO3- 构成了强氧化性环境,如原溶液中混有SO32-等也能被氧化成硫酸根离子,D错误。
考查方向
解题思路
理清实验操作中相关的反应,弄清原理。
易错点
实验原理把握不准,导致对实验现象无法解释。
知识点
11.已知咖啡酸的结构如图所示.关于咖啡酸的描述正确的是( )
正确答案
解析
A.分子中含8个H,分子式为C9H8O4,故A错误;
B.含双键与溴水发生加成反应,含酚−OH,酚−OH的邻对位与溴水发生取代反应,故B正确;
C.苯环与双键与氢气发生加成反应,则1mol咖啡酸最多可与4mol氢气发生加成反应,故C错误;
D.含−COOH,与Na2CO3溶液.NaHCO3溶液均反应,故D错误;
故选B。
考查方向
解题思路
由结构可知,分子中含酚−OH.碳碳双键.−COOH,结合酚.烯烃.羧酸的性质来解答。
易错点
不能熟练掌握有机物的结构与性质,不能把握官能团与性质的关系,不能分辨酚.羧酸.烯烃性质,没注意D中酚与羧酸性质的差别.
知识点
7. 某学习小组按如下实验过程测量海带中碘的含量
上述实验过程对仪器选择不合理的是
正确答案
知识点
选考题:请考生从给出的3道化学题中任选一题做答,并用2B铅笔将答题卡上所选题目对应的题号右侧方框涂黑,按所涂题号进行评分;多涂、多答,按所涂的首题进行评分;不涂,按本选考题的首题进行评分。
【化学—选修2:化学与技术】
我国磷矿储量占世界第二位,主要矿物为磷灰石[(Ca3(PO4)2)]。下图是生产化肥磷铵[(NH4)3PO4]并联产水泥的工艺流程。
(请回答21-26题)
【化学—选修3:物质结构与性质】A、B、C、D、E、F为前四周期元素。A、B最外层电子排布可表
示为asa、bsbbpb。(a≠b);B、C、D是位于P区的同一周期的元素, B与D原子核外的未成对电子数相等;ED2与CD2-为等电子体;F为过渡金属元素,其原子核外没有未成对电子。请回答下列问题:27-32题
【化学—选修5:有机化学基础】
高分子化合物在日常生活中具有重要应用,以有机物A设计合成尼龙-66和聚碳酸酯的流程如下,
其中:A的分子式为C6H6O,遇FeCl3溶液显出紫色。
请回答: 33-38题
21.操作a的名称 ,实验室中进行此操作时用到的玻璃仪器有 。
22.在实验室中操作b包括 、冷却结晶。
23.干燥机中发生反应的化学方程式为 。
24.水泥常用做建筑材料,是利用了水泥的 性质。
25.SO2的催化氧化反应为2SO2(g)十O2(g) 

是:K(400℃ ) K(500℃ )(填“>”、“<”或“=” )。② 催化氧化时使用热交换器的原因是 。
26.制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。下列能用于测定硫酸尾气
中SO2含量的试剂组是 。(填写相应字母)A.NaOH溶液、酚酞试液 B.KMnO4溶液、
稀H2SO4 C.碘水、淀粉溶液 D.氨水、酚酞试液
27.与F同区、同周期的元素是 (填元素符号),其原子的外围电子排布式是 。
28.元素B、C、D的第一电离能由大到小的顺序是 (用元素符号表示)。
29.B、C、D的最简单氢化物中,键角由大到小的顺序是 (用分子式表示),ED2的分子立体构型名称是 。
30.BD与C2互为等电子体,BD的结构式为(若有配位键,请用“→”表示) 。
31.CA3分子可以与A+离子结合成CA4+离子,这个过程中发生改变的是____(填序号)。 a. 微粒的空间构型 b. C原子的杂化类型 c. A-C-A的键角 d. 微粒的电子数
32.FE在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方FE晶体结构如右图所示,该晶体的密度为ρ g·cm—3。如果FE的摩尔质量为M g·mol—1,阿伏加德罗常数为NA mol—1,则a、b之间的距离为 cm。
33.B的名称为 ,其核磁共振氢谱显示峰的数目为 个。
34.C中官能团的结构简式为 。
35.由D到E的化学方程式为 。
36.写出F的结构简式 。
37.对于该流程所涉及物质来说,下列说法正确的是 。①检验产物F中A是否含过量,可用FeCl3溶液作试剂②尼龙-66与羊毛的成分中,均含有—CO—NH—结构③聚碳酸酯是良好的耐酸耐碱高分子材料④已知聚碳酸酯可以溶于有机溶剂,则其属于线型分子,具有热塑性
38.D的同分异构体中,满足下列条件的同分异构体的数目(不含立体异构)为 个。①能与NaHCO3溶液反应生成气体②能发生银镜反应和水解反应
正确答案
过滤(1分),漏斗、玻璃棒、烧杯(2分。填对2个给1分,全对给2分)
正确答案
蒸发浓缩
正确答案
正确答案
水硬性
正确答案
①常压下SO2的转化率已经很高,且增大压强时SO2的转化率提高不多,但成本增加较多(2分);>(1分)②移去反应中放出的热量,使反应后的气体降温并预热未反应的气体(2分)
正确答案
BC(2分。只填一个正确给1分,填错或多填0分)
正确答案
Cu(1分),
正确答案
N>O>C或N、O、C
正确答案
CH4>NH3>H2O或 CH4、NH3、H2O(2分);V形或角形(2分)。
正确答案
正确答案
ac 。(2分。只填一个正确给1分,填错或多填0分。)
正确答案
正确答案
环己醇(2分),5(2分)。
正确答案
正确答案
正确答案
正确答案
②④(2分。只填一个正确给1分,填错或多填0分。)
正确答案
12
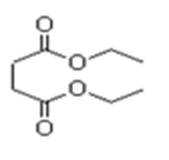
2.琥珀酸与乙醇反应生成琥珀酸二乙酯(结构如图所示),下列有关说法正确的是( )
正确答案
解析
A.1mol琥珀酸二乙酯含有2mol酯基,能与2mol的NaOH反应,故A错误;
B.琥珀酸二乙酯含有酯基,可发生取代反应,在一定条件下,羰基可发生加成,且有机物可燃烧,属于氧化反应,故B正确;
C.琥珀酸为1,4-丁二酸,分子式为C4H6O4,故C错误;
D.为链状化合物,不含环,故D错误.
本题正确答案是B
考查方向
解题思路
该有机物含有酯基,可发生取代、水解反应,结合分子的结构和官能团的性质解答该题
易错点
官能团的性质即酯的性质。
知识点
9.EDTA是一种重要的络合剂。4 mol 一氯乙酸和1 mol乙二胺(
正确答案
解析
一氯乙酸的分子式为C2H3ClO2,乙二胺分子为C2H8N2,根据题目信息利用原子守恒,列式4

考查方向
解题思路
利用反应中原子守恒进行分子式的推断。
易错点
分子式书写
知识点
(1)电渗析法淡化海水时阴极室可获得的重要化工原料有______。
(2)海水中含有大量的NaCl,盐田法仍是目前海水制盐的主要方法。盐田分为贮水池、____ 池和结晶池,建盐田必须在_________处建立(填序号)。
A.选在离江河入海口比较近的地方
B.多风少雨
C.潮汐落差大且又平坦空旷的海滩
(3)盐田中所得为粗盐,若想用粗盐制烧碱,需对所用食盐水进行两次精制。第一次精制主要是用沉淀法除去粗盐水中的Ca2+、Mg2+、Fe2+、SO42-等离子,流程如下:
①检测Fe3+是否除尽的方法是______________________;
②运用表中数据解释过程I选用BaCl2而不选用CaCl2的原因__________。
(4)工业上通常以NaCl、CO2和NH3为原料制取纯碱,请写出第一步制取NaHCO3的化学方程式___________________________。

样品中NaCl质量分数的数学表达式为______________________。
正确答案
解析
(1)在电渗析法淡化海水示意图中阴离子移向阳极,阳离子移向阴极,则水中的氢离子在阴极放电,则阴极生成氢气,同时生成NaOH,故答案为:氢气、氢氧化钠;(2)海水晒盐需要浓缩、蒸发、结晶,则盐田分为贮水池、蒸发池和结晶池;建盐田必须在阳光充足、平坦空旷的地方,则选B.多风少雨、C.潮汐落差大且又平坦空旷的海滩,与A无关,故答案为:蒸发;BC;
(3)①检测Fe3+是否除尽的方法为取过程Ⅳ的滤液于试管中,向其中滴加KSCN溶液,若溶液不变色证明Fe3+已经沉淀干净,反之没除净,故答案为:取过程Ⅳ的滤液于试管中,向其中滴加KSCN溶液,若溶液不变色证明Fe3+已经沉淀干净,反之没除净;②过程I除去钡离子,由表格数据可知硫酸钡比碳酸钡更难溶,则选用BaCl2而不选用CaCl2的原因为BaSO4的溶解度比CaSO4的更小,可将SO42-沉淀的更完全,故答案为:BaSO4的溶解度比CaSO4的更小,可将SO42-沉淀的更完全;
(4)制取纯碱,第一步中NaCl、CO2 和 NH3 为原料反应生成碳酸氢钠和氯化铵,该反应为NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,因此答案应为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl;
(5)测定样品中NaCl的质量分数,由流程可知,固体ng为碳酸钡的质量,由BaCO3~Na2CO3可知碳酸钠的质量为106n/197 g,则样品中NaCl质量分数为[m−(106n/197)]/m ×100%。
考查方向
解题思路
(1)在电渗析法淡化海水示意图中阴离子移向阳极,阳离子移向阴极,则水中的氢离子在阴极放电;
(2)海水晒盐需要浓缩、蒸发、结晶;建盐田必须在阳光充足、平坦空旷的地方;
(3)①检测Fe3+是否除尽,选择KSCN试剂观察是否出现血红色;②过程I除去钡离子,由表格数据可知硫酸钡比碳酸钡更难溶;
(4)制取纯碱,第一步中NaCl、CO2 和 NH3 为原料反应生成碳酸氢钠和氯化铵;
(5)测定样品中NaCl的质量分数,由流程可知,固体ng为碳酸钡的质量,由ngBaCO3~Na2CO3计算碳酸钠的质量,再计算NaCl质量分数.
易错点
化学方程式的掌握
知识点
9.三分子甲醛在一定条件下反应可生成三聚甲醛
正确答案
解析
A.高分子化合物相对分子质量在10000以上,该分子相对分子质量较小,所以不属于高分子化合物,故A错误;
B.分子式相同结构不同的有机物互为同分异构体,丙三醇分子式为C3H8O3,三聚甲醛分子式为C3H6O3,所以不是同分异构体,故B错误;
C.该反应符合加成反应特点,所以属于加成反应,故C正确;
D.三聚甲醛的分子式为C3H6O3,根据原子守恒知,如果完全燃烧生成二氧化碳和水的物质的量相等,如果生成CO,则生成的二氧化碳和水的物质的量不等,故D错误;
故选C。
考查方向
解题思路
清楚高分子化合物的特点,写出甘油好三聚甲醛的化学式,根据三聚甲醛的化学式计算出燃烧产物的物质的量
易错点
加成反应特点不清楚,同分异构体特点不了解
知识点
10.继屠呦呦从青蒿中成功提取出青蒿素后,中国科学院上海有机化学研究所又在1982年人工合成了青蒿素,其部分合成路线如下所示:
下列说法不正确的是
正确答案
解析
A.香茅醛含有碳碳双键,能发生加聚反应,含有醛基,能与酚发生缩聚反应,故A正确;
B.甲→乙是羟基中H原子被甲基取代,属于取代反应,故B正确;
C.-CH2OH氧化能得到-COOH,而环上的羟基不能氧化得到羧基,化学性质体现不同性,故C正确;
D.碳碳双键中其中1个不饱和碳原子连接2个甲基,不存在顺反异构,故D错误。
考查方向
有机物的结构和性质
解题思路
A.香茅醛含有碳碳双键,能发生加聚反应,含有醛基,能与酚发生缩聚反应;
B.甲→乙是羟基中H原子被甲基取代;
C.-CH2OH氧化能得到-COOH,而环上的羟基不能氧化得到羧基;
D.碳碳双键中其中1个不饱和碳原子连接2个甲基。
易错点
A中醛发生的缩聚反应为易错点
教师点评
本题考查有机物的结构与性质,熟练掌握官能团的性质、有机反应类型。
知识点
11.一种香豆素的衍生物结构如图所示,关于该有机物说法正确的是( )
正确答案
解析
A.该有机物分子式为 C10H8O4,故A错误;
B.只有苯环与双键与氢气发生加成反应,则1mol该有机物与 H2发生加成时最多消耗H2 4mol,故B错误;
C.酚-OH的邻对位与溴水发生取代反应,碳碳双键与溴水发生加成反应,则1mol该有机物与足量溴水反应时最多消耗Br23 mol,故C正确;
D.2个酚-OH、-COOC-及水解生成的酚-OH均与NaOH反应,则1mol该有机物与 NaOH 溶液反应是最多消耗NaOH 4 mol,故D错误;
考查方向
有机物的结构和性质
解题思路
由结构可知分子式,分子中含2个酚-OH、-COOC-及碳碳双键,结合酚、酯基、烯烃的性质来解答
易错点
酚、酯、烯烃的性质
教师点评
本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大
知识点
扫码查看完整答案与解析