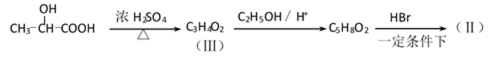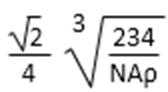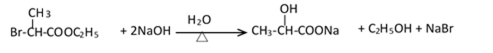- 原子核外电子排布
- 共93题
请考生从给出的3道化学题中任选一题做答。
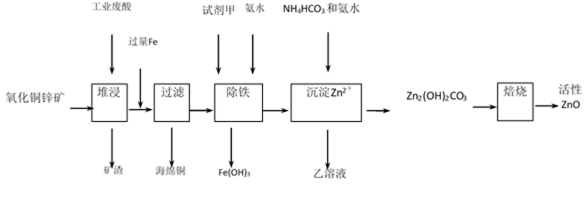
36.某工厂利用工业废酸(10%H2SO4)堆浸某废弃的氧化铜锌矿制取活性ZnO, 方案如下:
已知:298K时各离子开始沉淀及完全沉淀时的pH:
(1) 氧化铜锌矿中含有少量CuS和ZnS,在稀H2SO4作用下ZnS可溶而CuS不溶,这是由于同温下Ksp (ZnS) _________Ksp (CuS)(">" “<”,或“=”)。
(2) 在除铁过程中选用下列试剂中的_________作为试剂甲最合适:
A. Cl2
B. HNO3
C. KMnO4
D. H2O2
(3) 除铁过程中加入氨水的目的 ___________ ,实验中PH应控制的范围 ___________ ;
(4) 加试剂甲后,Fe3+,与氨水生成Fe(OH)3的离子方程式 ___________ ;
(5) 298K时,检验乙溶液中是否残留较多Fe3+的方法 ___________ ;
(6)乙的溶液可直接用作氮肥,乙的化学式 ___________;
(7) Zn2(OH)2CO3焙烧的化学方程式 ___________。
37.已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子云相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。试回答下列有关的问题:
(1)写出F元素的电子排布式_______。
(2)己知A元素扣一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为______。
(3)己知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子空间构型是______。
(4)B、C、D、E的第一电离能由大到小的顺序是______ (写元素符号)。
四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______(写化学式)。
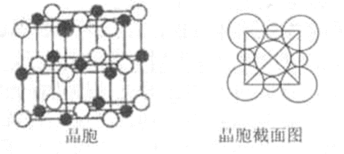
(5)由B、E两元素形成的化合物组成的晶体中,阴、阳离子都有球型对称结构, 它们都可以看作刚性圆球,并彼此“相切”。如下图所示为B、E形成化合物的晶胞结构图以及晶胞的剖面图:
晶胞中距离一个Na+最近的Na+有____________个。
若晶体密度为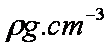
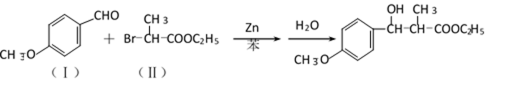
38.有机合成中增长碳链是一个重要环节。如下列反应:
用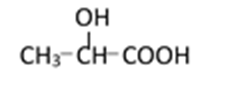
(1)(Ⅰ)的分子式为___________;(Ⅲ)的结构简式为___________ 。
(2)(Ⅱ)与足量的热NaOH溶液反应的化学方程式为___________ 。
(3)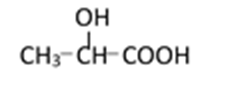
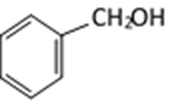
(4)(Ⅰ)的一种同分异构体能发生银镜反应,还能水解生成不含甲基的芳香化合物(Ⅳ)。(Ⅳ)的结构简式为 ___________。
正确答案
见解析。
解析
36.(1)>
(2) D
(3)调节溶液的pH,使Fe3+沉淀完全, 3.2~6.2
(4)Fe3++3NH3·H2O === Fe(OH)3↓+3 NH4+
(5)取少量乙溶液于试管中,滴入几滴KSCN溶液,若出现红色,说明还有较多Fe3+,若无红色出现,说明Fe3+沉淀完全 ,
(6)(NH4)2SO4
(7)Zn2(OH)2CO3 == 2ZnO+CO2↑ + H2O
37.(1)[Ar]3ds1
(2)sp3
(3)三角锥形
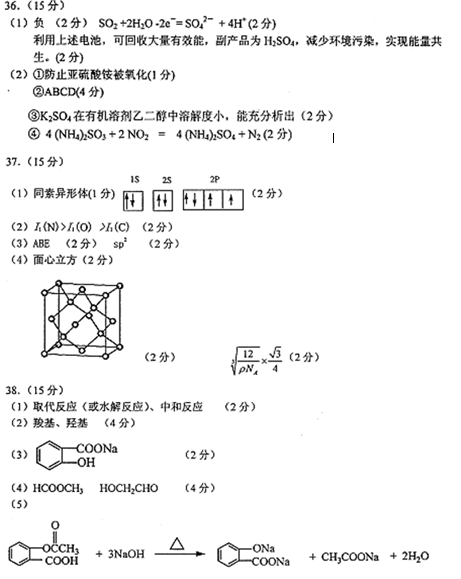
(4)Cl> P> S>Na,NaOH > H3PO4 >HClO4>H2SO4
(5)12;
38.(1)C8H8O2 ;CH2=CH-COOH
(2)
或
(3) 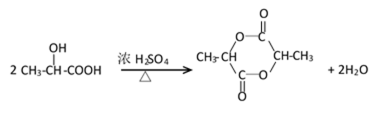
取代反应(或酯化反应)
(4) 
知识点
符号“3px”没有给出的信息是()
正确答案
解析
略
知识点
请从36~38题中任选一题作答
36.[化学—选修:化学与技术]
SO2.NO是大气污染物。吸收SO2 和NO,获得

(1)装置Ⅰ中生成
(2)含硫各微粒(


①下列说法正确的是( )(填字母序号)。
a.pH=8时,溶液中
b.pH=7时,溶液中
c.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:( )。
(3)装置Ⅱ中,酸性条件下,NO被

(4)装置Ⅲ的作用之一是再生
①生成
②生成
(5)已知进入装置Ⅳ的溶液中,


37.[化学—选修:物质结构与性质]
在5-氨基四唑(
(1)基态Ga原子的电子排布式可表示为( );
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为( );在1mol 5-氨基四唑中含有的σ键的数目为( )
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂.
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的 空间构型为( )。
②以四氯化钛.碳化钙.叠氮酸盐作原料,可以生成碳氮化钛化合物.其 结 构是用碳原子取代氮化钛晶胞(结构如上图示)顶点的氮原子,这种碳氮化钛化合物的化学式为( )。
③与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有 ( )。(填写元素符号)
④ [Ti(OH)2(H2O)4]2+中的化学键有( )。
a.σ键 b.π键 c.离子键 d.配位键
38.[化学—选修:有机化学基础]
苯酚是一种重要的化工原料。以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N(部分产物及反应条件已略去)。
(1)生成M、N的反应类型分别是( ),( ); D的结构简式是 ( )。
(2)已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种。C的结构简式是( )。
(3)由苯酚生成A的化学方程式是 ( ) 。B与C反应的化学方程式是( )。
(4)以苯酚为基础原料也可以合成芳香族化合物F。经质谱分析F的相对分子质量为152,其中氧元素的质量分数为31.6%,F完全燃烧只生成

已知:①芳香族化合物F能发生银镜反应,且还能发生水解反应;
②F的核磁共振氢谱显示其分子中含有4种氢原子;
③分子结构中不存在“-O-O- ”的连接方式。F的结构简式是( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
36.“C1化学”是指以研究分子中只含一个碳原子的化合物为原料来合成一系列化工原料和燃料的化学。
(1)煤的气化是获得合成气的一种方法,写出煤气化的主要化学反应方程式:( );
(2)天然气的重整的化学反应方程式为 ( );
(3)最近科学家提出一种“绿色自由’’构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为甲醇。其技术流程如下:
①碳酸钾溶液所起的作用是( );
②写出上述流程中分解池中发生反应的化学方程 ( );
③写出合成塔中发生的化学反应方程式( );
④“绿色自由”构想技术流程中常包括物质和能量的循环利用,上述流程中能体现循环利用的物质有 ( ) 。
37.在电解炼铝过程中加入冰晶石(用“A”代替),起到降低Al2O3的熔点等诸多作用,冰晶石的生产原理如下:
根据题意完成下列填空:
(1)冰晶石的化学式为 ( ),含有离子键、( )化学键;
(2)生成物中含有10个电子的分子是( )(写分子式),该分子的空间构型为 ( ),中心原子的杂化方式为( );
(3)反应物中电负性最大的元素为( ),写出其原子最外层的电子排布图:( )
(4)冰晶石由两种微粒构成,冰晶石晶胞结构如图丁所示,位于大立方体顶点和面心,位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的体心处▽所代表的微粒是( )(填具体的微粒符号)
(5)Al单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,请回答:
一个晶胞中Al原子的数目为( );Al晶体的密度为( )(用字母表示)
38.酒石酸(tartaric acid),即,2,3-二羟基丁二酸,是一种羧酸﹐存在于多种植物中﹐也是葡萄酒中主要的有机酸之一。作为食品中添加的抗氧化剂﹐可以使食物具有酸味。酒石酸最大的用途是饮料添加剂。也是药物工业原料,以烃A为原料合成酒石酸的流程如下:
已知:① 烃A中碳氢质量比为8:1
②
③ D的分子组成是C4H8O2Cl2,核磁共振氢谱显示其有三个峰。
(1)A的名称为: ( ),分子中最多有( )原子共面;
(2)B中所含官能团的名称是( ),B存在顺反异构,它的顺式结构为( );
(3)C转化为D的反应类型是( ),
F转化为G的化学反应方程式是 ( );
(4)F与乙二醇在一定条件下可以发生缩聚反应,该反应的化学方程式是___________
(5)C的同分异构体有多种,其中含有“—COO—”结构的有( )种;
(6)欲得到较纯净的酒石酸,需将G从其溶液中分离提纯,查阅相关资料得知G的溶解度受温度影响较大,则分离提纯G的方法是( )。
36.请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。“C1化学”是指以研究分子中只含一个碳原子的化合物为原料来合成一系列化工原料和燃料的化学。
(1)煤的气化是获得合成气的一种方法,写出煤气化的主要化学反应方程式:
;
(2)天然气的重整的化学反应方程式为 ;

①碳酸钾溶液所起的作用是 ;
②写出上述流程中分解池中发生反应的化学方程 ;
③写出合成塔中发生的化学反应方程式 ;
④“绿色自由”构想技术流程中常包括物质和能量的循环利用,上述流程中能体现循环利用的物质有 。
37.在电解炼铝过程中加入冰晶石(用“A”代替),起到降低Al2O3的熔点等诸多作用,冰晶石的生产原理如下:
2Al(OH)3+ 12HF+ 3 Na2CO3 = 2A+ 3CO2↑+ 9H2O
根据题意完成下列填空:
(1)冰晶石的化学式为 ,含有离子键、 等化学键;
(2)生成物中含有10个电子的分子是 (写分子式),该分子的空间构型为 ,中心原子的杂化方式为 ;
(3)反应物中电负性最大的元素为 ,写出其原子最外层的电子排布图:



体心处▽所代表的微粒是 (填具体的微粒符号)

下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,请回答:
一个晶胞中Al原子的数目为 ;Al晶体的密度为 (用字母表示)
38.酒石酸(tartaric acid),即,2,3-二羟基丁二酸,是一种羧酸﹐存在于多种植物中﹐也是葡萄酒中主要的有机酸之一。作为食品中添加的抗氧化剂﹐可以使食物具有酸味。酒石酸最大的用途是饮料添加剂。也是药物工业原料,以烃A为原料合成酒石酸的流程如下:
已知:① 烃A中碳氢质量比为8:1
②
③ D的分子组成是C4H8O2Cl2 ,核磁共振氢谱显示其有三个峰。
(1)A的名称为: ,分子中最多有 个原子共面;
(2)B中所含官能团的名称是 ,B存在顺反异构,它的顺式结构为 ;
(3)C转化为D的反应类型是 ,
正确答案
正确答案
正确答案
其中第29、30题为物理题,第31、32题为化学题,考生从两道物理题、两道化学题中各任选一题作答。
31.[化学----物质结构与性质]
(1)铬的外围电子排布式是( ) ,与铬同周期,最外层有3个未成对电子数的元素名称是( ),该元素对应的最低价氢化物分子的中心原子采取了( )杂化方式,分子的空间构型是( ) 。
(2)富勒烯
(3)氟化氢水溶液中存在氢键有( )种。
(4)2011年诺贝尔化学奖授予了因发现准晶体材料的以色列科学家。某准晶体是锰与另一个短周期元素X形成的凝固态。已知:金属的电负性一般小于1.8。元素X与同周期相邻元素Y、Z的性质如下表:则X元素符号是( ),锰与X在准晶体中的结合力为 ( )。
32.[化学—有机化学基础]
莽草酸(C7H10O5)可有效对付致命的H5N1型禽流感病毒的药物“达菲”的重要成分,它可从中药八角茴香中提取得到。右图是以莽草酸为原料合成某些物质的路线:
根据上图回答下列问题:
(1)A中含有的两种含氧官能团分别是_____________________
(2)已知烯醇式结构(C=C-OH)不能稳定存在、则莽草酸的结构简式为( ) 。
(3)莽草酸→C的反应类型是( ) 。
(4)写出C→D的化学反应方程式( )。
(5)与C具有相同官能团的同分异构体(含C)共有( )种。
31.[化学----物质结构与性质]
(1)铬的外围电子排布式是 ,与铬同周期,最外层有3个未成对电子数的元素名称是 ,该元素对应的最低价氢化物分子的中心原子采取

(2)富勒烯(


(3)氟化氢水溶液中存在氢键有 种。
(4)2011年诺贝尔化学奖授予了因发现准晶体材料的以色列科学家。某准晶体是锰与另一个短周期元素X形成的凝固态。已知:金属的电负性一般小于1.8。元素X与同周期相邻元素Y、Z的性质如下表:则X元素符号是 ,锰与X在准晶体中的结合力为 。
32.[化学—有机化学基础]
莽草酸(C7H10O5)可有效对付致命的H5N1型禽流感病毒的药物“达菲”的重要成分,它可从中药八角茴香中提取得到。右图是以莽草酸为原料合成某些物质的路线:
根据上图回答下列问题:
(1)A中含有的两种含氧官能团分别是_____________________
(2)已知烯醇式结构(C=C-OH)不能稳定存在、则莽草酸的结构简式为 。
(3)莽草酸→C的反应类型是 。
(4)写出C→D的化学反应方程式 。
(5)与C具有相同官能团的同分异构体(含C)共有 种。
正确答案
正确答案
请考生从给出的3道化学题中任选一题做答。
36.水处理技术在生产、生活中应用广泛。
(1)含有较多________离子的水称为硬水。硬水加热后产生碳酸盐沉淀的离子方程式为________________________(写出一个即可)
(2)将RH型阳离子交换树脂和ROH型阴离子交换树脂串接来软化天然硬水,应先使硬水通过_______(填“RH”或“ROH”)型离子交换树脂,原因是_______________________。
(3)通过施加一定压力使水分子通过半透膜而将大分子或离子截留,从而获得纯净水的方法称为________。电渗析法净化水时,使离子通过半透膜的推动力是________。
(4)检验蒸馏水的纯度时,最简单易行的方法是测定水的________。水处理技术在生产、生活中应用广泛。
37.下面是C60、金刚石和二氧化碳的分子模型。
请回答下列问题:
(1)硅与碳同主族,写出硅原子基态时的核外电子排布式:_________________
(2)从晶体类型来看,C60属于_________晶体。
(3)二氧化硅结构跟金刚石结构相似,即二氧化硅的结构相当于在硅晶体结构中每个硅与硅的化学键之间插入一个O原子。观察图乙中金刚石的结构,分析二氧化硅的空间网状结构中,Si、O原子形成的最小环上O原子的数目是__________________________;晶体硅中硅原子与共价键的个数比为
(4)图丙是二氧化碳的晶胞模型,图中显示出的二氧化碳分子数为14个。实际上一个二氧化碳晶胞中含有________个二氧化碳分子,二氧化碳分子中

(5)有机化合物中碳原子的成键方式有多种,这也是有机化合物种类繁多的原因之一。丙烷分子中2号碳原子的杂化方式是_______,丙烯分子中2号碳原子的杂化方式是_______,丙烯分子中最多有 个原子共平面。
38.一种分子式为C11H12O2的芳香酯(H)是一种香精的调香剂,可由下列路线合成:
回答下列问题:
(1)A中含有的官能团是( )(写名称)。G的结构简式是( ) 。反应⑤的反应类型是( ) 。
(2)X是F的同分异构体,X分子中含有一个苯环,且核磁共振氢谱有3个峰,则X可能的结构简式是( ) 。
(3)写出有关化学方程式:
②( );
③( );
⑧ ( ) 。
(4)E与甲醇发生酯化反应后,通过加聚反应能生成一种高分子化合物(俗称有机玻璃),写出此有机玻璃的结构简式是 ( ) 。
正确答案
(2)RH;先通过阴离子交换树脂可能产生Mg(OH)2等沉淀而影响树脂交换效果
(3)反渗透法;电势差(或电场力)
(4)电导率(或电阻率)
37.(1)
(2)分子
(3)6; 1:2
(4)4; 1:1
(5)sp3; sp2; 7
38.(1)碳碳双键;
解析
解析已在路上飞奔,马上就到!
知识点
请从36~38题中任选一题作答
36.【化学—选修2:化学与技术】
化学是人类进步的关键,化学为人类的生产、生活提供了物质保证。
Ⅰ.氮的化合物是重要的化工产品。其生产方法也在逐渐改进中,各国科学家均在为提高其产量,降低能耗做各种有益的探究。
(1)25℃时合成氨反应热化学方程式为:

(2)近年有人将电磁场直接加在氮气与氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较好的产率。从化学反应本质角度分析,电磁场对合成氨反应的作用是( );与传统的合成氨的方法比较,该方法的优点是( )。
Ⅱ.(3)卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品。从卤水中提取镁的步骤为:
a.将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
b.将石灰乳加入到海水沉淀池中经过滤得到
c.在

d.将
e.电解熔融的氯化镁可得到Mg。
①步骤d中的“一定条件”指的是( ) 。
②有同学认为:步骤b后可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,你同意该同学的想法吗?为什么?
(4)铀是核反应最重要的燃料,已经研制成功一种螫合型离子交换树脂,它专门吸附海水中 ( )的U4+,而不吸附其他元素。其反应原理为( )(树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为:( ) 。
37.【化学—物质结构与性质】
许多金属及它们的化合物在科学研究和工业生产中具有许多用途.回答下列有关问题:
(1)基态Ni核外电子排布式为( ), 第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是( );
(2)



(3)另一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为( ),若该晶胞的边长为a pm,则合金的密度为( ) 
38.【化学——选修5:有机化学基础】
苯酚是一种重要的化工原料。以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N。(部分产物及反应条件已略去)
(1)苯酚的俗名是( )。B的官能团名称( )。
(2) 已知C的分子式为C5H12O,C能与金属Na反应,C的一氯代物有2种。B与C反应的化学方程式是( ) 。
(3)生成N的反应方程式( ) 。
(4)以苯酚为基础原料也可以合成有机物E。已知E的相对分子质量为122,其中氧元素的质
量分数为26.23%,E完全燃烧只生成

(5)已知E具有如下结构特征:


(6)物质F如图,则符合下列条件F的同分异构体有( )种。
①能发生银镜反应②能与

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
36.以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
(1)写出反应Ⅰ的化学方程式 ( ) 。
(2)生产中,向反应II中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是( )。
(3)下列有关说法正确的是( ) 。
a.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
b.反应III中氧化剂与还原剂的物质的量之比为4︰1
c.反应IV需控制在60~
d.反应V中的副产物氯化铵可用作氮肥
(4)反应Ⅴ在25℃、40%乙二醇溶液中进行,不断有硫酸钾晶体从溶液中析出,硫酸钾的产率会超过90%,选用40%乙二醇溶液的原因是( )。
(5)(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,写出二氧化氮与亚硫酸铵反应的化学方程式( ) 。37.[Cu(NH3)4]SO4·H2O是一种杀虫剂。
(1)Cu元素基态原子的电子排布式为___ ____。
(2)元素N、O、S的第一电离能由大到小排列的顺序为___ __。
(3)H元素可与O元素形成H2O和H2O2,H2O2易溶于H2O,其主要原因为___ ___。
(4)H元素与N元素可组成化合物N2H4,其中N原子的轨道杂化方式为___ ___。
(5)与SO互为等电子体的一种分子的化学式为 ___ ___。
(6)Cu元素与H元素可形成一种红色晶体,其结构如图8,则该化合物的化学式为__ __。38.菠萝酯是一种具有菠萝香气的食用香料,是化合物甲与苯氧乙酸
(1)甲一定含有的官能团的名称是( ) 。
(2)5.8g甲完全燃烧可产生0.3mol CO2和0.3 mol H2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是( )。
(3)苯氧乙酸有多种酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且有2种一硝基取代物的同分异构体是(写
(4)已知:R-C

R-ONa
菠萝酯的合成路线如下:
①试剂X不可选用的是(选填字母)( ) 。
a. CH3COONa溶液
b. NaOH溶液
c. NaHCO3溶液
d.Na
②丙的结构简式是 ( ),反应II的反应类型是 ( ) 。
③反应IV的化学方程式是( ) 。
37.[Cu(NH3)4]SO4·H2O是一种杀虫剂。
(1)Cu元素基态原子的电子排布式为___ ____。
(2)元素N、O、S的第一电离能由大到小排列的顺序为___ __。
(3)H元素可与O元素形成H2O和H2O2,H2O2易溶于H2O,其主要原因为______。
(4)H元素与N元素可组成化合物N2H4,其中N原子的轨道杂化方式为___ ___。
(5)与SO互为等电子体的一种分子的化学式为___ ___。
(6)Cu元素与H元素可形成一种红色晶体,其结构如图8,则该化合物的化学式为____。
38.菠萝酯是一种具有菠萝香气的食用香料,是化合物甲与苯氧乙酸
(1)甲一定含有的官能团的名称是( )。
(2)5.8g甲完全燃烧可产生0.3mol CO2和0.3 mol H2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是 ( )。
(3)苯氧乙酸有多种酯类的同分异构体,其中能与FeCl3溶液发生显色反应,且有2种一硝基取代物的同分异构体是(写出任意2种的结构简式)( ) 。
(4)已知:
菠萝酯的合成路线如下:
①试剂X不可选用的是(选填字母)( ) 。
a. CH3COONa溶液
b. NaOH溶液
c. NaHCO3溶液
d.Na
②丙的结构简式是( ),反应II的反应类型是( ) 。
③反应IV的化学方程式是( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
36.请从36~38题中任选一题作答
36.【化学——选修2:化学与技术】
近年来,为提高能源利用率,西方提出共生系统。特指为提高经济效益,人类生产活动尽可能多功能化。共生工程将会大大促进化学工业的发展。
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V。实际过程中,将SO2通入电池的( )极(填“正”或“负”),负极反应式为( )。用这种方法处理SO2废气的优点是____
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
①生产中,向反应II的溶液中加入适量还原性很强的对苯二酚等物质,其目的是( )。
②下列有关说法正确的是( )。
A.反应I中需鼓人足量空气,以保证二氧化硫充分氧化生成硫酸钙。
B.反应Ⅲ中发生反应的化学方程式为
C.反应,IV需控制温度在60~70℃,目的之一是减少碳酸氢铵的分解。
D.反应V中的副产物氯化铵可用作氮肥。
③反应V中选用了40%的乙二醇溶液,温度控制在25℃,此时硫酸钾的产率超过90%,选用40%的乙二醇溶液原因是( )。
④(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式:( )。
37.【化学——选修3:物质结构与性质】
下图分别是金刚石、石墨、足球烯和碳纳米管的结构示意图。图中小黑点或小黑圈均代表碳原子。
(1)四种物质互称为 ( )。写出碳原子的基态电子排布图 ( )。
(2)试比较:第一电离能I1(C)、I1(N)、I1(O)由大到小的顺序为( ) 。
(3)石墨中存在的作用力有( )。A:σ键 B:π键 C:氢键 D:配位键 E:分子间作用力石墨中碳原子采取的杂化方式是 ( )。
(4)仔细观察图A金刚石结构,有人从中找出它的晶胞结构是碳原子位于立方体的所有顶点及面心处,将立方体切割成8个小立方体,在其中4个互不相邻的立方体体心各有一个碳原子。请写出金刚石属于晶胞,在方框中画出一个晶胞结构示意图:
若金刚石的密度为ρg·cm-3,试计算碳原子的半径为( )cm。
38.【化学——选修5:有机化学基础】
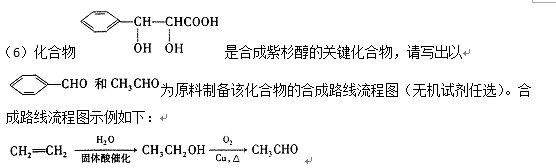
A为药用有机物,从A出发可发生下图所示的一系列反应。已知A在一定条件下能跟醇发生酯化反应,A分子中苯环上的两个取代基连在相邻的碳原子上;D不能跟NaHCO3溶液反应,但能跟NaOH溶液反应。
请回答:
(1)A转化为B、C时,涉及到的反应类型有( ) 、( ) 。
(2)F中所含官能团的名称是 ( )、( );
(3)D的结构简式为 ( )。
(4)E的两种同分异构体Q、R都能在一定条件下发生银镜反应,在核磁共振氢谱中,Q有两组峰,R有三组峰,Q、R的结构简式为Q ( )、R ( ) 。
(5)A在加热条件下与NaOH溶液反应的化学方程式为( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
36. 硫酸铁铵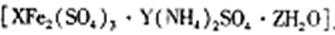
请回答下列问题:
(1)操作甲名称:( );操作乙名称:( )。
(2)硫酸亚铁溶液加硫酸酸化主要目的是 ( );滤渣A主要成分是();
(3)①试剂B最适宜的是()(填序号)
A.NaClO B.H2O2 C.酸化的KMnO4 D.K2Cr2O7
②除杂原理是( )(用离子方程式表示)
③若要检测Fe2+是否氧化完全,方法是( );能否用酸化的KMnO4溶液 ( ) (填“能”或“不能”),理由是 ( ) 。
(4)称取14.0g样品,配成100ml溶液,分成二等份,向一份加入足量NaOH溶液,过滤,洗涤,干燥得2.14g沉淀;另一份加入0.05mol Ba(NO3)2,恰好完全反应,则该产品化学式为 ( )。
37.A、B、C、D为原子序数依次增大的短周期元素。已知:
①A原子核外电子有5种运动状态;
②B是地壳中含量最多元素;
③A、C、D未成对电子数之比为1:3:1:
④E有生物金属之称,E4+与氩原子核外电子排布相同;
请回答下列问题:
(1)D原子价电子层结构为 ( ) ;基态E原子的核外电子排布式:( );
(2)5种元素所形成XY3型化合物化学式可能为( )、( );其中心原子杂化方式为 ( );
(3)与C周期相同的金属元素分别处于( )区;
(4)由B、D构成的以D为中心三原子分子的空间构型为 ( ) ;
(5)下列晶体的堆积方式与E单质晶体堆积方式相同的是( );
A.Po B.Zn C.Ag D.K
(6)B形成的两种同素异形体中在水中溶解度更大的是( )(填化学式);原因是( )。
38.我国科研人员从天然姜属植物分离出一种具有显著杀菌、消炎、解毒作用的化合物H,H的合成路线如下:
(1)A→B的反应类型是 ( )。
(2)化合物B中的含氧官能团为 ( ) 和( )(填官能团名称)。
(3)写出同时满足下列条件的B的一种同分异构体的结构简式:( ) 。
I.苯环上有两个取代基 II,分子中有6种不同化学环境的氢
Ⅲ.既能与FeCl3溶液发生显色反应,又能发生银镜反应,水解产物之一也能发生银镜反应
(4)实现F→G的转化中,加入的化合物X( C12H14O3)的结构简式为 ( ) 。
(5)写出F与新制氢氧化铜悬浊液反应的化学方程式: ( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析