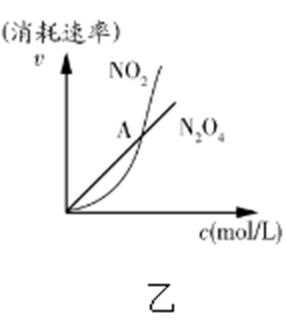- 溶液中溶质的质量分数及相关计算
- 共12题
9.下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.下述实验能达到预期目的的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.若需通过导电实验证明NaCl是离子化合物,可以选择的实验对象是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.试运用所学知识,回答下列问题:
(1)已知某反应的平衡表达式为:
(2)已知在400℃时,
欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是__________(填序号)
A.缩小体积增大压强
B.升高温度
C.加催化剂
D.使氨气液化移走
(3)在一定体积的密闭容器中,进行如下化学反应:
请完成下列问题:
①判断该反应的ΔH__________0(填“>”或“<”)
②在一定条件下,能判断该反应一定达化学平衡状态的是___________(填序号)
A.3v(B)(正)=2v(C)(逆)
B.A和B的转化率相等
C.容器内压强保持不变
D.混合气体的密度保持不变
(2)以天然气(假设杂质不参与反应)
①放电时,负极的电极反应式为:_________________________。
②假设装置中盛装100.0 mL 3.0 mol·L—1 KOH溶液,放电时参与反应的氧气在标准状况下体积为8 960 mL。放电完毕后,电解质溶液中各离子浓度的大小关系为_________________________。
正确答案
(1)C(s)+H2O(g) 
(2) = ; A
(3)① >; ② CD
(4)
①CH4-8e—+10OH—= CO32—+7H2O
②c(K+)>c(HCO3—)>c(CO32—)>c(OH—)>c(H+)
解析
解析已在路上飞奔,马上就到!
知识点
11.下列关于有机化合物的说法中,正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见图。下列说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
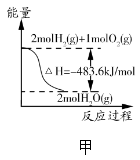
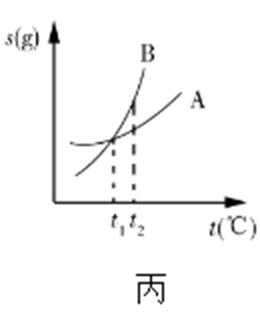
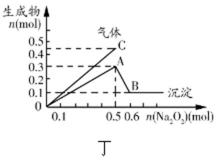
关于下列各图的叙述,正确的是
正确答案
解析
略
知识点
恒温下使某盐溶液蒸发掉ag水,有bg不含结晶水的晶体析出,再蒸发掉ag水后,又有cg不含结晶水的晶体析出,则原溶液中溶质的质量分数为
正确答案
解析
略
知识点
将amol钠和amol铝一同放入mg水(足量)中,所得溶液的密度为dg/mL,该溶液的质量百分比浓度为
正确答案
解析
略
知识点

正确答案
解析
略
知识点
扫码查看完整答案与解析