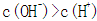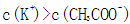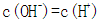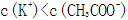- 酸碱混合时的定性判断及有关pH的计算
- 共38题
常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判断一定错误的是
正确答案
解析
本题考查电解质溶液的知识,意在考查考生思维的缜密性。若a=b,恰好反应生成弱酸强碱盐CH3COOK,溶液呈碱性,A项正确;若a>b,反应后溶液中溶质为CH3COOK和CH3COOH,该溶液可能呈中性,则C项正确;若该溶液含CH3COOH很少,CH3COOH的电离程度小于CH3COO-的水解程度,溶液呈碱性,则溶液中c(K+)>c(CH3COO-),B项正确;若溶液中c(K+)<c(CH3COO-),利用电荷守恒知溶液中一定存在c(H+)>c(OH-),溶液显酸性,而a<b,溶液一定呈碱性,二者矛盾,D项一定错误。
知识点
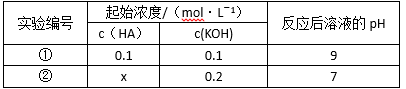
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断不正确的是
正确答案
解析
由表中①的HA为弱酸且酸碱物质的量相等,因此得A正确;由①中电荷守恒得[OH-]=[K+]-[A-]+[H+]=Kw/1X10-9 mol/L,故B错误;C中由②得X>0.2mol/L,故C正确;由电荷守恒得D正确
知识点
对于常温下pH为2的盐酸,叙述正确的是
正确答案
解析
电荷守恒A对。B 氨水过量,显碱性。D,反应后生成乙酸和氯化钠,水溶液为酸性。
知识点
25℃时,a mol·L-1一元酸HA与b mol·L-1NaOH等体积混合后,pH为7,则下列关系一定正确的是( )
正确答案
解析
pH为7,说明混合后的溶液显中性,根据溶液中的电荷守恒c(Na+)+c(H+)=c(OH-)+c(A-),可知c(Na+)=c(A-),故C正确。若HA为强酸,则a=b,若HA为弱酸,则应是a>b,现在不知是强酸还是弱酸,故无法确定a和b的关系。
知识点
常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是
正确答案
解析
a溶液分为四种情况①若酸为强酸,则反应后氨水有剩余,溶液呈碱性;②若酸为弱酸且酸的电离程度比氨水还弱,则溶液呈酸性;③若酸为弱酸且酸的电离程度比氨水强,则溶液呈碱性;④若酸为弱酸且酸的电离程度与氨水相同,则溶液呈中性。b溶液分为两种情况:①若酸为强酸,则二者恰好反应生成强酸强碱盐,溶液呈中性;②若酸为弱酸,则反应后酸有剩余,溶液呈酸性。
知识点
扫码查看完整答案与解析