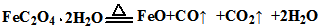- 物质检验实验方案的设计
- 共27题
13.下列设计的实验方案能达到实验目的的是( )
正确答案
解析
A.NaOH过量,反应生成偏铝酸钠,不能制备Al(OH)3悬浊液,故A错误;B.乙酸与碳酸钠反应后,与乙酸乙酯分层,振荡后静置分液,并除去有机相的水可除杂,故B正确;C.加入少量新制氯水氧化了亚铁离子,检验亚铁离子,应先加KSCN溶液,再加氯水,故C错误;D.相同条件下,试管中加入2mL5%H2O2和1mLFeCl3溶液反应速率快,则可探究催化剂对H2O2解速率的影响,故D正确;故选BD.
考查方向
解题思路
A.NaOH过量,反应生成偏铝酸钠;B.乙酸与碳酸钠反应后,与乙酸乙酯分层;C.加入少量新制氯水了氧化亚铁离子;D.可探究催化剂对H2O2解速率的影响.
易错点
本题考查化学实验方案的评价,为高频考点,涉及物质的性质、混合物分离提纯、离子检验及影响反应速率的因素等,把握物质的性质及反应原理为解答的关键,注意实验的评价性分析,题目难度不大.
知识点
28. 某化学兴趣小组的同学进行草酸亚铁晶体(FeC2O4·nH2O)分解的实验探究。经小组讨论,他们设计了如下装置进行实验。烧瓶B中盛有饱和NH4Cl和饱和NaNO2混合液(常用于实验室制N2),干燥管C1、C4中装有碱石灰,试管E1、E3、E4中装有澄清石灰水。
(1)充分反应后,将D1中的固体残余物投入足量经煮沸的稀硫酸中,固体完全溶解且无气体放出,取反应液加入KSCN溶液无血红色,证明固体产物为( )。
(2)该实验装置中有3个酒精灯,至少应该点 次酒精灯,最先点燃的酒精灯是( ),最后点燃的是( )。
(3)该实验装置中有4个直立的试管,它们与盛放试剂体现不同的作用,其中E2的作用是: ( )。
(4)该实验装置中有4个干燥管,C3中盛装的试剂是( )。
(5)取7.2 g样品充分反应后,测得D1中的固体残余物为2.88 g,D2中固体质量减轻0.64 g,则草酸亚铁晶体(FeC2O4·nH2O)分解的方程式为( )。
正确答案
(1)FeO
(2)4、 A1、 A1
(3)除尽气体中的CO2
(4)P2O5或CaCl2
(5)
解析
解析已在路上飞奔,马上就到!
知识点
28.过氧化钙(CaO2)常用作种子消毒剂、药物制造、油脂漂白及高温氧化剂,还可以作为鱼池增氧剂。有人提出:CO2、SO2与过氧化钙的反应原理相同;但也有人提出:SO2具有较强的还原性,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
(1) 装置B中所装试剂是( ),装置D的作用是( )。
(2)装置E用于测定氧气的体积,读数时,除应上下移动装置E中右侧量气管使两侧液面相平外,还要( ),再准确读数。
(3)实验测得装置C增重m1 g,装置D增重m2 g,装置E中收集到V L气体(已换算成标准状况下),用上述有关测量数据判断,若SO2未氧化,V与m1或m2的关系式为( );若SO2完全氧化,写出反应的化学方程式( )。
为进一步探究过氧化物与SO2反应的原理,向一定量的过氧化钠固体中通入足量SO2,取反应后的固体进行实验探究:
提出假设:( )
假设1:反应后固体中只有Na2SO3,SO2未氧化;
假设2:反应后固体中只有Na2SO4,SO2完全氧化;
假设3:( ) 。
实验探究:
(4)设计实验证明假设3是正确的,简要回答实验过程、现象和结论:( )。
实验评价:
(5)实验过程中若SO2的量不足,则直接影响探究实验结果的科学性,请简要说明原因:
( )。
正确答案
28.
(1)浓硫酸(1分) 吸收未反应的SO2(2分)
(2)待气体温度恢复到室温后,(2分)
(3)V=7m1/30,(3分)CaO2+SO2=CaSO4(2分)反应后固体为Na2SO3、Na2SO4的混合物,SO2部分氧化(2分)
(4)取少量反应后的固体放入试管中,加适量水溶解,加入BaCl2溶液有白色沉淀产生。再加入稀盐酸,沉淀部分溶解,证明原固体中既有亚硫酸钠也有硫酸钠,即Na2O2将SO2部分氧化。(2分)
(5)若Na2O2剩余,固体加水溶解,过氧化钠能将SO3(2-)氧化成SO4(2-)。(2分)
解析
解析已在路上飞奔,马上就到!
知识点
27.某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究氯气与碳酸钠反应得到的固体物质。
(1)写出装置A中发生反应的化学方程式:( )
(2)写出试剂Y的名称:( )
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为氯氧化物。可以确定的是C中含有的氯盐只有一种,且含有碳酸氢钠,现对C成分进行猜想和探究。①提出合理假设。
假设1:存在两种成分:Na HCO3和( );
假设2:存在三种成分:Na HCO3和 ( ) 、( );
②设计方案,进行实验。请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:蒸馏水、稀硝酸、氯化钡溶液、澄清石灰水、硝酸银溶液、试管、小烧杯
(4)根据上述实验现象,有同学得出“干燥的氯气能和碳酸钠固体反应”的结论。该结论严密吗?为什么?
(5)若C中有0.1molCl 2恰好与装置中Na 2CO3完全反应,且假设1成立,可推知C中反应的化学方程式为:( )
正确答案
(1)实验室制备氯气的化学方程式
(2)饱和的氯化钠
(3)氯化钠 氯化钠和碳酸钠 步骤2:在A中加入氯化钡溶液 若有沉淀生成,说明有碳酸钠;若没有沉淀说明没有碳酸钠 在B中加入稀硝酸酸化硝酸银溶液 若有白色沉淀说明有氯化钠,若无沉淀就没有氯化钠
(4)不严密,因为有碳酸氢钠生成,氢元素就应来源于水,故是潮湿的氯气与碳酸钠反应
(5)
解析
解析已在路上飞奔,马上就到!
知识点
27.工业上用黄铜矿冶炼铜及对炉渣综合利用的一种工艺流程如下:
(1)冶炼过程中得到Cu2O和Cu的混合物称为“泡铜”,其与金属A1在高温条件下混合反
应可得粗铜,反应化学方程式为________。
粗铜精炼时应将粗铜连接在直流电源的____极,可在____极得到纯度较高的精铜。
(2)传统炼铜的方法主要是火法炼铜,其主要反应为:
每生成1 mol Cu,共消耗____mol O2。反应③中的氧化剂是____。
(3)炼铜产生的炉渣(含
①加入适量NaClO溶液的目的是_______ (用离子方程式表示)。
②除去Al3+的离子方程式是____。
③选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂有:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水。
所选试剂是____。实验设计:________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.研究性学习小组进行溴乙烷的制备的相关探究实验。
探究一:实验室制取少量溴乙烷的装置如图。
(1)圆底烧瓶中的反应物是溴化钠、( )和1:1的硫酸。
配制体积比1:1的硫酸所用的定量仪器为( ) 。
a.天平 b.量筒 c.容量瓶 d.滴定管
(2)烧瓶中发生的主要化学反应( ) 。
(3)将生成物导入盛有冰水混合物的试管A中,冰水混合物的
作用是 ( )。试管A中的物质分为三层(如图所示),产物在第( ) 层。
(4)用浓硫酸进行实验,若A中获得的有机物呈棕黄色,除杂的正确方法是( )。
a.蒸馏 b.氢氧化钠溶液洗涤 c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
探究二:探究试管B中使酸性高锰酸钾溶液褪色的物质。
假设1,该物质为乙烯。假设2,该物质为( ) 。设计实验验证你的两种假设。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
25.某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。
(1)写出装置A中发生反应的化学方程式:( )。
(2)写出试剂Y的名称:( ) 。
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。可以确定的是C中含氯元素的盐只有一种,且含有NaHCO3,现对C成分进行猜想和探究。
①提出合理假设。
假设1:存在两种成分:NaHCO3和 ( );
假设2:存在三种成分:NaHCO3和 ( ) 、( ) 。
②设计方案,进行实验。请写出实验步骤以及预期现象和结论(可不填满)。
限选实验试剂和仪器:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
(4)已知C中有0.1mol Cl2参加反应。若假设l成立,可推知C中反应的化学方程式为:( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析