- 金属及其化合物
- 共561题
20.已知NaOH+Al(OH)3→Na[Al(OH)4]。向集满CO2的铝制易拉罐中加入过量NaOH浓溶液,立即封闭罐口,易拉罐渐渐凹瘪;再过一段时间,罐壁又重新凸起。上述实验过程中没有发生的离子反应是
正确答案
解析
向集满CO2的铝罐中加入过量氢氧化钠,首先CO2与氢氧化钠反应,表现为铝罐变瘪,接着过量的氢氧化钠再与铝罐反应,因铝罐表面有氧化膜Al2O3,故可发生A、B、C的反应。故选D。
考查方向
解题思路
铝及表面有氧化膜Al2O3和氢氧化钠溶液反应过程中不会有Al3+产生。
易错点
未熟练掌握Al、Al2O3的性质。
知识点
29.(15分)无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:

步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 常温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160 ℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5
请回答:
(1)仪器A的名称是____________。
实验中不能用干燥空气代替干燥N2,原因是___________。
(2)如将装置B改为装置C(图2),可能会导致的后果是___________。
(3)步骤3中,第一次过滤除去的物质是___________。
(4)有关步骤4的说法,正确的是___________。A.可用95%的乙醇代替苯溶解粗品 B.洗涤晶体可选用0℃的苯C.加热至160℃的主要目的是除去苯 D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++ Y4-====Mg Y2-
①滴定前润洗滴定管的操作方法是__________。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol·L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50 mL,则测得无水MgBr2产品的纯度是________________________(以质量分数表示)。
正确答案
(1)干燥管 防止镁屑与氧气反应,生成的MgO阻碍Mg和Br2的反应
(2)会将液溴快速压入三颈瓶,反应过快大量放热而存在安全隐患
(3)镁屑
(4)BD
(5)①从滴定管上口加入少量待测液,倾斜着转动滴定管,使液体润湿内壁,然后从下部放出,重复2-3次
②97.5%
知识点
4.下列离子方程式正确的是
正确答案
解析
A.烧碱溶液与铝片反应生成偏铝酸钠和氢气,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,所以A错误;B.将磁性氧化铁溶于盐酸的离子反应为Fe3O4+8H+=2Fe3++Fe2++4H2O,所以B错误;C.用惰性电极电解氯化钠时,在两极上分别产生氢气和氯气,而用铁做电极,则阳极上是铁放电,故而没有氯气生成,反应的离子方程式为:Fe+2H2O
考查方向
解题思路
A.烧碱溶液与铝片反应生成偏铝酸钠和氢气,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑B.将磁性氧化铁溶于盐酸的离子反应为Fe3O4+8H+=2Fe3++Fe2++4H2O,C.用惰性电极电解氯化钠时,在两极上分别产生氢气和氯气,而用铁做电极,则阳极上是铁放电,故而没有氯气生成;D.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合,反应生成了碳酸钡、一水合氨和水。
易错点
盐酸没有强氧化性,不能将Fe2+氧化为Fe3+电解过程中活泼金属做阳极要比阴离子优先放电;
知识点
16.室温下,在0.2 mol·L-1 Al2(SO4)3溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
2.下列物质的转化在给定条件下能实现的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.某同学将光亮的镁条放入盛有NH4Cl溶液的试管中,有大量气泡产生。为探究该反应原理,该同学做了以下试验并观察到相关现象,由此得出的结论不合理的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
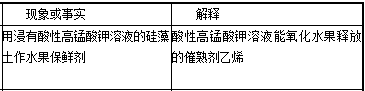
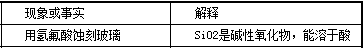
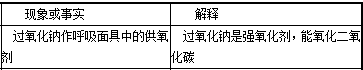
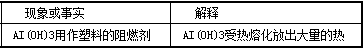
8.化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
类比归纳是学习化学的重要方法,对如下类比的说法正确的是
正确答案
解析
略
知识点
工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:
对上述流程中的判断正确的是
正确答案
解析
略
知识点
12.用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是 ( )
①加盐酸溶解
②加烧碱溶液溶解
③过滤
④通入过量CO2生成Al(OH)3 沉淀
⑤加入盐酸生成Al(OH)3 沉淀
⑥加入过量烧碱溶液
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析