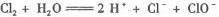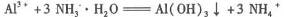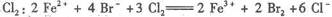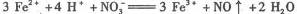- 化学用语
- 共784题
26、欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。已知:碳酸不能溶解Al(OH)3沉淀。
(1)Si在周期表中的位置是( )。
(2)下列说法正确的是( )。
(3)该矿石的组成是 ,滤渣和NaOH溶液反应的离子方程式是( )。
(4)该矿石和1 mol L-1HNO3反应的离子方程式( )。
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,目的是( );若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg,理论上至少需要1 mol L-1 HNO3的体积为( )L。
正确答案
(1)(1分)第三周期、ⅣA族
(2)(2分)ac
(3)(2分)FeCO3和SiO2 (2分)SiO2+2OH— = SiO32—+H2O
(4)(2分)3FeCO3+10H++NO3— = 3Fe3+ +3CO2↑+NO↑+5H2O
(5)(2分)NO循环使用能减少环境污染,NO跟H2O、O2反应后又得到硝酸提高原料利用率 (2分)3×104
解析
解析已在路上飞奔,马上就到!
知识点
2.下列解释事实的化学方程式或离子方程式,不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.(14分)重铬酸钾(K2Cr2O7)是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3)为原料生产重铬酸钾。实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下图所示。反应器中涉及的主要反应是
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应的原理相同均转变为可溶性盐。写出氧化铝与碳酸钠反应的化学方程式:( ) 。
(2)操作⑤中加酸酸化后

(3)步骤③中测定pH值的操作为:_________。
(4)某同学设计的检验上述工艺流程④的滤渣中Fe、Al、Si元素成分的探究实验如下,请帮助完成该实验,并填写表中空格:
(5)称取重铬酸钾(其式量为294)试样2.5000 g配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol/LH2SO4和足量碘化钾(铬的还原产物为Cr 3+),放置于暗处5 min,然后加入100 mL水,加入3 mL淀粉指示剂,用0.1200 mol/LNa2S2O3标准溶液滴定(
①配制溶液时所需的玻璃仪器除烧杯、玻璃棒外,还需( )和 ( )。
②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为(设整个过程中其他杂质不参与反应)( ) 。(保留2位小数)
27.重铬酸钾(K2Cr2O7)是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3)为原料生产重铬酸钾。实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下图所示。反应器中涉及的主要反应是:
6FeO·Cr2O3 + 24NaOH + 7KClO3 = 12Na2CrO4 + 3Fe2O3 + 7KCl + 12H2O
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应的原理相同均转变为可溶性盐。写出氧化铝与碳酸钠反应的化学方程式: 。
(2)操作⑤中加酸酸化后CrO

(3)步骤③中测定pH值的操作为:_________。
(4)某同学设计的检验上述工艺流程④的滤渣中Fe、Al、Si元素成分的探究实验如下,请帮助完成该实验,并填写表中空格:
(5)称取重铬酸钾(其式量为294)试样2.5000 g配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol/L H2SO4和足量碘化钾(铬的还原产物为Cr 3+),放置于暗处5 min,然后加入100 mL水,加入3 mL淀粉指示剂,用0.1200 mol/L Na2S2O3标准溶液滴定(I2 + 2S2O


①配制溶液时所需的玻璃仪器除烧杯、玻璃棒外,还需 和 。
②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为(设整个过程中其他杂质不参与反应) 。(保留2位小数)
正确答案
9.已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.下列离子方程式书写正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.下列离子方程式正确的是()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10、下列离子方程式表达正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
27.亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用。②ClO2气体在中性和碱性溶液中不能稳定存在。
(1)在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,请写出阳极的电极反应方程式( ) 。
(2)反应生成ClO2气体需要X酸酸化,X酸可以为( )。
A.盐酸 B.稀硫酸 C.硝酸 D.H2C2O4溶液
(3)吸收塔内的温度不能过高的原因为 ( )。
(4)ClO2被S2– 还原为ClO–2 、Cl–转化率与pH关系如图。写出pH≤2时ClO2与S2– 反应的离子方程式:( ) 。
(5)ClO2对污水中Fe2+、Mn2+、S2-和CN–等有明显的去除效果。某工厂污水中含CN– amg/L,现用ClO2将CN–氧化,生成了两种无毒无害的气体,其离子反应方程式为_______________________;处理100 m3这种污水,至少需要ClO2_____________ mol。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10. 下列离子方程式中,不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析