- 理想气体的状态方程
- 共154题
18.如图为水平放置的刚性圆柱形气缸,气缸内被重力不可忽略的A、B两活塞封有一定质量的气体,活塞之间用硬杆相
正确答案
解析
气体的压强为P,以整体为研究对象,受力平衡,可以得到P0(SA﹣SB)=P(SA﹣SB),所以可以得到气体的压强始终与大气的压强相等,即做等压变化,根据盖吕萨克定律可得

考查方向
解题思路
以气体和活塞的整体为研究对象,根据受力平衡得出大气压力和气体压力之间的关系,根据气体的状态方程分析气体的体积的变化
易错点
本题的关键是得到气体做的是等压变化,得出等压变化之后,根据等压变化的盖吕萨克定律分析就比较简单了
知识点
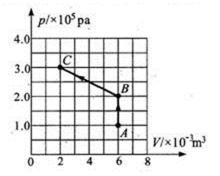
一定质量的理想气体从状态A变化到状态B再变化到状态C,其p-V图象如图所示。已知该气体在状态A时的温度为27℃,求:
20.该气体在状态B和C时的温度分别为多少K?
21.该气体从状态A经B再到C的全过程中是吸热还是放热?传递的热量是多少?
正确答案
300K
解析
对一定质量的理想气体由图象可知,A→B为等容变化,
由查理定律得= (2分)
即代入数据得TB=600 K (1分)
A→C由理想气体状态方程得= (2分)
代入数据得 TC=300 K (1分)
考查方向
解题思路
首先根据理想气体状态方程求出温度,然后利用热力学第一定律求出释放热量
易错点
理想气体状态方程的应用
正确答案
放热 1000J
解析
②从A到C气体体积减小,外界对气体做正功,由p-V图线与横轴所围成的面积可得
W==1000 J (2分)
由于TA=TC,该气体在状态A和状态C内能相等,ΔU=0
由热力学第一定律ΔU=W+Q (1分)
可得Q=-1000J,即气体向外界放出热量,传递的热量为1000 J (1分)
考查方向
解题思路
首先根据理想气体状态方程求出温度,然后利用热力学第一定律求出释放热量
易错点
理想气体状态方程的应用
竖直平面内有一直角形内径相同的细玻璃管,A端封闭,C端开口,最初AB段处于水平状态,中间有一段水银将气体封闭在A端,各部分尺寸如图所示,外界大气压强p0=75cmHg 。
36.若从右侧缓慢注入一定量的水银,可使封闭气体的长度减小为20cm,需要注入水银的总长度为多少?
37.若将玻璃管绕经过A点的水平轴顺时针转动90°,当AB
正确答案
30cm
解析
由玻意耳定律


考查方向
解题思路
通过理想气体状态方程求解,在列方程求解注意取舍
易错点
理想气体的状态方程列式求解中的压强的计算过程
正确答案
39.04cm
解析
设顺时针转动90°后,水银未溢出,且AB部分留有x长度的水银,玻意耳定律:



考查方向
解题思路
通过理想气体状态方程求解,在列方程求解注意取舍
易错点
理想气体的状态方程列式求解中的压强的计算过程
15.如图所示,竖直放置的弯曲玻璃管a端封闭,b端开口,水银将两段空气封闭在管内,管内各液面间高度差为h1、h2、h3且h1=h2=h3;K1、K2为两个阀门,K2位置与b管水银面等高,打开阀门后可与外界大气相通。打开K1或K2,下列判断正确的是( )
正确答案
解析
设h1=h2=h3=h,由图示可知,中间封闭气体的压强p=p0﹣h2=p0﹣h<p0,左边气体压强
pa=p﹣h3=p﹣h=p0﹣2h<p0;
A、打开K1,中间部分气体压强等于大气压p0,则h2和h3均变为零,左边气体压强变大,气体体积减小,h3增大,故AB错误;
C、打开K2,各部分气体压强均不变,则h1、h2、h3均不变,故C错误,D正确;
考查方向
解题思路
根据图示判断各部分气体压强与大气压的关系,然后分析打开阀门后各部分气体压强如何变化,然后根据压强的变化分析答题.
易错点
本题有两个结论可以直接应用①同一气体的压强处处相等 ②同一液体内部不同点间的压强差由高度差决定.分析清楚气体压强如何变化是正确解题的关键.
知识点
如图所示,固定的绝热汽缸内有一质量为m的“T”型绝热活塞(体积可忽略),距汽缸底部h0处连接一U形管(管内气体的体积忽略不计)。初始时,封闭气体温度为T0,活塞距离汽缸底部为1.5h0,两边水银柱存在高度差,左边低于右边。已知水银的密度为ρ,大气压强为p0,汽缸横截面积为S,活塞竖直部分长为1.2h0,重力加速度为g。
36.初始时,水银柱两液面高度差?
37.通过制冷装置缓慢降低气体温度,当温度为多少时两水银面相平?
正确答案
解析

考查方向
解题思路
利用理想气体状态方程建立等式求解。
易错点
在求解压强大小是要注意考虑活塞质量
正确答案
解析
在活塞竖直部分没有碰到气缸低前气体作等压变化,水银面高度差不改变。只有当竖直部分碰到气缸底部时,继续降低温度水银面高度差发生变化。所以当水银面相平时,活塞竖直部分已经触底,故




考查方向
解题思路
利用理想气体状态方程建立等式求解。
易错点
在求解压强大小是要注意考虑活塞质量
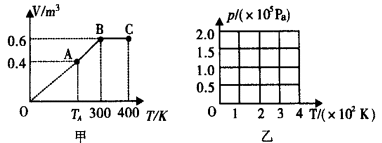
如图甲是一定质量的气体由状态A经过状态B变为状态C的V-T图象。已知气体在状态A时的压强是1.5×105Pa。
20.说出A→B过程中压强变化的情形,并根据图象提供的信息,计算图甲中TA的温度值.
21.请在图乙坐标系中,作出该气体由状态A经过状态B变为状态C的P—T图象,并在图线相应位置上标出字母A、B、C.如果需要计算才能确定的有关坐标值,请写出计算过程.
正确答案
200K
解析
①从题图甲可以看出,A与B连线的延长线过原点,所以A→B是一个等压变化,即pA=pB
根据盖—吕萨克定律可得=
所以TA
考查方向
解题思路
由图示图象求出气体各状态的状态参量、判断出气体状态变化过程,然后应用气体状态方程求出气体状态参量,再作出图象
易错点
理想气体状态方程的应用
正确答案
见参考答案
解析
②
由题图甲可知,由B→C是等容变化,根据查理定律得=
所以pC=pB=pB=pB=×1.5×105 Pa=2.0×105 Pa
则可画出由状态A→B→C的p-T图象如图所示.
考查方向
解题思路
由图示图象求出气体各状态的状态参量、判断出气体状态变化过程,然后应用气体状态方程求出气体状态参量,再作出图象
易错点
理想气体状态方程的应用
19.如图,在大气中有一水平放置的固定圆筒,它由a、b和c三个粗细不同的部分连接而成,各部分的横截面积分别为2S、S/2和S。已知大气压强为p0,温度为T0.两活塞A和B用一根长为4l的不可伸长的轻线相连,把温度为T0的空气密封在两活塞之间,此时两活塞的位置如图所示。现对被密封的气体加热,使其温度缓慢上升到T。若活塞与圆筒壁之间的摩擦可忽略,此时两活塞之间气体的压强可能为多少?
正确答案
解析
设加热前,被密封气体的压强为p1,轻线的张力为f,根据平衡条件有: 对活塞A:
对活塞B:
即被密封气体的压强与大气压强相等,轻线处在拉直的松弛状态,这时气体的体积为:
对气体加热时,被密封气体温度缓慢升高,两活塞一起向左缓慢移动,气体体积增大,压强保持p1不变,若持续加热,此过程会一直持续到活塞向左移动的距离等于l为止,这时气体的体积为:
根据盖·吕萨克定律得:


当T>T2时,活塞已无法移动,被密封气体的体积保持V2不变,由查理定律得:
解得:

考查方向
解题思路
根据平衡关系求出改变前后的气体压强,利用气体状态方程求解。
易错点
利用平衡条件求压强要考虑大气压强产生的作用力
知识点
19.如图所示,气缸分上、下两部分,下部分的横截面积大于上部

正确答案
解析
开始时,对两活塞受力分析:受到重力、钢球的压力、大气对上活塞的压力F大上,大气对下活塞的压力F大下、缸内气体对上和下活塞的压力F内上、F内下.根据平衡特点得到:mg+F钢+F大上+F内下=F大下+F内上;F大上=P大S上,F大下=P大S下,F内上=P内S上,F内下=P内S下;给气缸内气体缓慢加热,根据气体状态方程得到缸内气体压强增大,由于S上<S下;所以F内下﹣F内上的差值在增大,所以两活塞相对气缸向下移动,故A错误;取走几个钢球,F钢在减小,所以两活塞相对气缸向上移动,故B正确;大气压变小,F大上﹣F大下差值在变小,所以两活塞相对气缸向下移动,故C错误;让整个装置自由下落,处于完全失重状态,两活塞相对气缸静止,因此向上移动,故D正确。
考查方向
解题思路
要注意研究过程中哪些量不变,哪些量变化。根据气体状态方程和已知的变化量去判断其它的物理量。对活塞进行受力分析,运用平衡知识解决问题。
易错点
能够对活塞进行受力分析,运用平衡知识解决问题。从选项中找出变化的物理量,再引起哪些量发生改变。
知识点
如图所示,一敞口圆筒形气缸竖直放置在水平桌面上,导热良好的活塞可沿气缸壁无摩擦滑动且不漏气。气缸的顶部放有一密封性能良好的缸盖,缸盖和活塞的质量均为m,活塞横截面积为s,气缸周围的大气压强恒为

22. 继续缓慢加热,对气缸恰好无压力时,求缸内气体的温度。
正确答案
解析
当缸内气温为T时,B中
则A中 
当缸盖对气缸恰好无压力时,A中
B中 

对A:

带入解得 
考查方向
解题思路
先根据理想气体的等温变化解得此时气体的压强,然后根据
易错点
正确应用理想气体状态方程的前提是:判断此变化过程是属于等压、等容、还是等温变化,受力分析时研究对象的确定
17.如图,固定的导热气缸内用活塞密封一定质量的理想气体。现用力使活塞缓慢地向上移动。用p、V、E和
正确答案
解析
A、气缸和活塞导热性能良好,气缸内气体温度与环境温度相同,所以气体发生等温变化,所以p﹣V图象是双曲线,故A正确.B、气缸内气体温度与环境温度相同,保持环境温度不变,则气体的内能保持不变,故B正确.C、温度是分子平均动能变化的标志,温度不变,所以该气体分子的平均动能不变,故C错误.D、一定质量的理想气体,所以n=
考查方向
解题思路
气缸和活塞导热性能良好,气缸内气体的温度与环境温度相同,保持环境温度不变,气体发生等温变化.一定质量的理想的内能只跟温度有关.现用力使活塞缓慢地向上移动,气体对外界做功,根据热力学第一定律分析吸放热情况.根据气体状态方程和已知的变化量去判断其它的物理量.
易错点
关键要判断气体状态过程,知道等温变化遵守玻意耳定律,掌握温度的微观意义,能运用数学知识研究物理图象的形状和物理意义.
知识点
扫码查看完整答案与解析