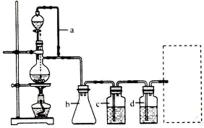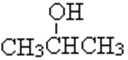- 蒸发、蒸馏与结晶的仪器
- 共19题
在实验室进行下列实验,括号内的实验用品都能用到的是
正确答案
解析
本题考查化学基本实验原理、化学仪器的使用等知识,A选项,在硫酸铜结晶水含量的测定实验中不使用温度计;B选项,醋酸铅是重金属盐,会使蛋白质变性,在蛋白质的盐析实验中不会用到;D选项,肥皂的制备中用到的药品是氢氧化钠不是甘油。
知识点
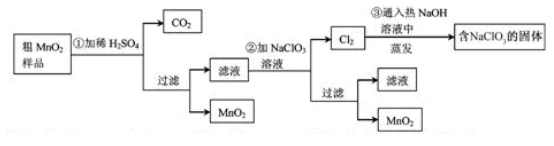
MnO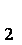
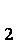
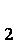
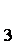

(1)第①步加稀H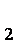
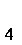
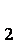
(2)第②步反应的离子方程式是__ _______+__ClO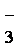

(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、_______、_______、_______,已知蒸发得到的固体中有NaClO
(4)若粗MnO
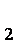
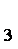
正确答案
(1)MnO2和MnCO3
(2)5Mn2++2ClO3-+4H2O=5MnO2↓+Cl2↑+8H+
(3)蒸发皿、酒精灯、玻璃棒;NaCl
(4)0.02
解析
本题综合考查离子反应方程式书写、氧化还原反应配平、化学计算以及化学实验的相关知识。情景简单,工艺流程清晰。
知识点
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了__________气体。继续滴加至液溴滴完。装置d的作用是____________________________________;
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用l0 mL水、8 mL l0%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是除去HBr和未反应的Br2;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是______;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母);
正确答案
解析
此题为基础题但是学生易出错。苯与液溴的实验产物为溴苯和HBr,HBr属于极易溶于水的。故有白雾。D装置的作用应该是吸收HBr和Br2这里学生易答成防止倒吸。(3)(4)很简单学生都熟悉。
知识点
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
CH3CH=CH2+CO+H2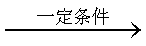
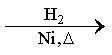
CO的制备原理:HCOOH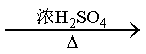
请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备氢气、丙烯,写出化学反应方程式:_________,_________。
(2)若用以上装置制备干燥纯净的CO,装置中a和b的作用分别是_________,_________。c和d中盛装的试剂分别是_________,_________。若用以上装置制备H2,气体发生装置中必需的玻璃仪器名称是_________;在虚线框内画出收集干燥H2的装置图。
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是_________(填序号)。
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4 ⑤品红溶液
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是_________。
a.低温、高压、催化剂 b.适当的温度、高压、催化剂
c.常温、常压、催化剂 d.适当的温度、常压、催化剂
(5)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品。为纯化1-丁醇,该小组查阅文献得知:①R-CHO+NaHSO3(饱和)
粗品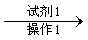


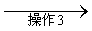
试剂1为_________,操作1为_________,操作2为_________,操作3为_________。
正确答案
(1)Zn+2HCl
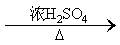
(2)恒压;防倒吸;NaOH溶液;浓H2SO4;分液漏斗、蒸馏烧瓶;
(3)④⑤①②③(或④⑤①③②)
(4)b
(5)饱和NaHSO3溶液;过滤;萃取;蒸馏
解析
(1)实验室用锌粒和稀盐酸制备氢气;用2-丙醇和浓硫酸共热,消去反应制备丙烯;
(2)在题给装置中,a的作用保持分液漏斗和烧瓶内的气压相等,以保证分液漏斗内的液体能顺利加入烧瓶中;b主要是起安全瓶的作用,以防止倒吸;c为除去CO中的酸性气体,选用NaOH溶液,d为除去CO中的H2O,试剂选用浓硫酸;若用题给装置制备H2,则不需要酒精灯,必须得是反应容器和滴加盐酸的仪器,氢气用向下排空气法收集,注意导气管伸入底部;
(3)检验丙烯和少量SO2、CO2及水蒸气组成的混合气体各成分时,应首先选④无水CuSO4检验水蒸气,然后用⑤品红溶液检验SO2,并用①饱和Na2SO3溶液除去SO2;然后用③石灰水检验CO2,用②酸性KMnO4溶液检验丙烯,特别注意不能用酸性高锰酸钾溶液除去二氧化硫;
(4)题给合成正丁醛的反应为气体体积减小的放热反应,为增大反应速率和提高原料气的转化率,选b;(5)由操作1后得到“滤液”和信息①可知,试剂1应为NaHSO3饱和溶液,操作为过滤;加入乙醚时1-丁醇易溶解于其中,故操作2为萃取分液;根据两种有机物沸点的不同,操作3应为蒸馏。
知识点
利用实验器材(规格和数量不限),能完成相应实验的一项是
正确答案
解析
硫酸铜溶液的浓缩结晶需要用到酒精灯,A错;用盐酸出去BaSO4中的少量BaCO3需要进行过滤,需要用到漏斗,B错;用固体配制溶液需要用到托盘天平称量固体,C错;D中可以先进行置换反应,然后进行萃取、分液,D正确。
知识点
扫码查看完整答案与解析