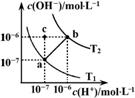- 水的电离
- 共35题
1
题型:
单选题
|
在常温下,纯水中存在电离平衡H2O


正确答案
A
解析
略
知识点
水的电离
1
题型:
单选题
|
如图表示水溶液中c(H+)和c(OH-)的关系,下列说法正确的是
正确答案
A
解析
略。
知识点
水的电离
1
题型:
单选题
|
下列说法正确的是
正确答案
C
解析
略
知识点
水的电离离子浓度大小的比较
1
题型:
单选题
|
W、X、Y、Z四种元素均为短周期元素且原子序数依次增大,其简单离子都能促进水的电离的是
正确答案
D
解析
略
知识点
元素周期律的应用水的电离
1
题型:
多选题
|
水是极弱的电解质,改变外界条件对水的电离有促进或抑制作用,下列说法错误的是
正确答案
A
解析
略
知识点
水的电离
下一知识点 : 离子积常数
扫码查看完整答案与解析