- 氧化还原反应的计算
- 共67题
13.室温下,取m克铝镁合金与一定浓度的稀硝酸恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加b mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中正确的有( )
①沉淀中氢氧根的质量为(
②恰好溶解后溶液中的NO3—离子的物质的量为
③反应过程中转移的电子数为
④生成NO气体的体积为
⑤发生反应的硝酸的物质的量为(
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
26.铜及其化合物在生产、生活中有广泛的应用。
Ⅰ、铜可采用如下方法制备:
方法一:火法炼铜:Cu2S + O2 2Cu + SO2
方法二:湿法炼铜: CuSO4 + Fe FeSO4 + Cu
上述两种方法中,你认为哪种方法更好 _____,原因是 _____(写出1条原因即可)。分别用火法炼铜与湿法炼铜生产640gCu,则转移的电子数之比为 ______。
Ⅱ、印刷电路板上使用的铜需要回收利用。
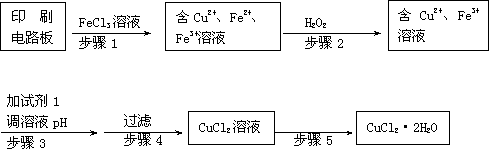
用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O晶体,实验室模拟回收过程如下:
①步骤2中反应的离子方程式是________ 。
②步骤5中蒸发浓缩CuCl2溶液时,要滴加浓盐酸,目的是________________ (用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl2·2H2O晶体。
③步骤4中洗涤沉淀的操作为_______
④步骤3中可选用的“试剂1”是________ (写出一种即可),目的是使溶液的pH升高到4,此时Fe3+浓度为 ________ [Ksp(Fe(OH)3)=4×10-38]。
正确答案
Ⅰ
湿法炼铜(或方法二) 不会产生污染空气的气体(或湿法炼铜不需要外界提供能量) 3:2
Ⅱ
① 2Fe2++ H2O2 + 2 H+ = 2Fe3+ + 2H2O
②CuCl2在溶液中可以发生水解反应: CuCl2+2H2O 
③ 向漏斗中加少量蒸馏水(水)至没过沉淀,静置滤干后重复操作2~3次。
④ CuO[或Cu(OH)2] 4×10-8mol/L
解析
解析已在路上飞奔,马上就到!
知识点
9.据悉,奥运会上使用的发令枪所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾。撞击时发生的化学反应方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
8.有一混合溶液,其中只含有Fe2+、Cl—、Br—、I—(忽略水的电离)其中Cl—、Br—、I—的个数比为2:3:4,向该溶液中通入氯气使溶液中Cl—和Br—的个数比为3:1,则通入氯气的物质的量与溶液中剩余Fe2+的物质的量之比为(还原性I—> Fe2+> Br—> Cl—)( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
12.已知硫化亚铜与一定浓度的硝酸共热,所得溶液中只有硝酸铜和硫酸铜,放出一氧化氮和二氧化氮两种气体,且两种气体的物质的量之比为3:7,则参加反应的硫化亚铜和作氧化剂的硝酸的物质的量之比为( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析