- 电极反应和电池反应方程式
- 共352题
复方过氧化氢消毒剂具有高效、环保、无刺激无残留,其主要成分H2O2。
(1)H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了甲、乙两种实验装置。
若利用甲实验,可通过观察________现象,从而定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是________;若利用乙实验可进行定量分析,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是________。
(2)在含有表面活性剂的酸性水溶液中,以碳为电极,通直流电进行电解可制取氢气和过氧化氢,过氧化氢在________(填“阴极”、“阳极”)产生。
以H2O2和硼氢化合物NaBH4(B的化合价为+3价)作原料的燃料电池,可用作通信卫星电源。其工作原理如图所示,写出a极上的电极反应式:________,正极材料采用MnO2,MnO2除了作电极材料之外还可能具有的作用为________。
(3)锗(Ge)与碳是同主族元素,最新研究表明有机锗具有明显的抗肿瘤活性,锗不与NaOH 溶液反应,但在有H2O2存在时可与NaOH 溶液反应生成锗酸盐,其化学方程式为________。
正确答案
(1)产生气泡的快慢;可以消除阴离子不同对实验的干扰;产生40mL气体所需的时间
(2)阳极;BH4- + 8OH- - 8e- = BO2- + 6H2O;MnO2对电极反应可能具有催化作用
(3) Ge+2 H2O2+2NaOH=Na2GeO3 +3H2O
解析
略。
知识点
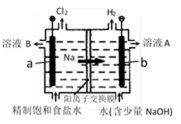
(1)A为用惰性电极电解饱和食盐水(含少量Ca2+、Mg2+)的装置。
①电解一段时间后,B中出现浑浊现象,请用离子方程式表示原因 。
此时电极a附近的现象为 ,因此工业上电解所用的食盐水需精制。
②随反应的进行,C中溶液红色褪去,主要原因有两种可能。请按要求填写表格。
(2)电解饱和食盐水所得气体X,可应用于提取溴单质。现有流程图如下:
请回答:
① 气体X的化学式为 ,反应II的化学方程式为 。
② 在母液苦卤中含有较多的NaCl、KCl、MgCl2、MgSO4等物质。用沉淀法测定苦卤中镁元素的含量(g/L),实验过程中应测定的数据有 。
③ 电解200kg 质量分数为25%的饱和食盐水,当浓度下降到20%时,收集到氯气的物质的量为 (溶于溶液中的氯气忽略不计,计算结果保留一位小数) 。
正确答案
见解析。
解析
(1) ① Cl2 + S2-= 2Cl-+ S↓
有无色气泡产生,溶液出现浑浊
②
(2) ① Cl2
SO2+Br2+2H2O=2HBr+H2SO4
② 苦卤样品的体积、Mg(OH)2沉淀的质量
③ 97.7 mol
知识点
下图为电解饱和食盐水的装置(阳离子交换膜只允许阳离子通过),下列叙述中正确的是( )
正确答案
解析
略
知识点
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知:
下列说法正确的是
正确答案
解析
略
知识点
工业上电解饱和食盐能制取多种化工原料,下图是离子交换膜法电解饱和食盐水示意图,下列说法中不正确的是
正确答案
解析
略
知识点
扫码查看完整答案与解析