- 化学反应中能量转化的原因
- 共42题
9.在恒容密闭容器中,用铜铬的氧化物作催化剂,用一定量的HCl(g)和O2制取Cl2的原
理为4HCl(g)+O2(g) 
正确答案
解析
A.该反应是一个反应前后气体体积减小、放热的可逆反应,在反应达到平衡之前,随着反应的进行,气体的物质的量逐渐减小,则容器的压强在逐渐减小,故A正确;
B.分离出H2O(g),即减小生成物浓度,逆反应速率减小,故B正确;
C.该反应的正反应是放热反应,升高温度平衡向逆反应方向移动,平衡常数减小,故C错误;
D.使用催化剂只改变化学反应速率但不影响平衡的移动,转化率不变,故D正确
考查方向
化学平衡的影响因素
解题思路
该反应是一个反应前后气体体积减小、放热的可逆反应,在反应达到平衡之前,容器内气体的压强在不断减小,分离出H2O(g),即减小生成物浓度,逆反应速率减小,升高温度平衡向逆反应方向移动,平衡常数减小,使用催化剂只改变化学反应速率但不影响平衡的移动,转化率不变
易错点
催化剂只影响反应速率不影响平衡的移动
教师点评
本题考查了影响化学平衡的因素,难度不大
知识点
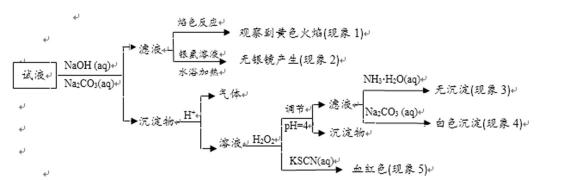
21. 现有一瓶标签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其
成分,取部分制剂作为试液,设计并完成了如下实验:
已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。
该同学得出的结论正确的是
正确答案
解析
A.因加入了NaOH (aq)和Na2CO3(aq),在滤液中引入了Na+,不能根据滤液焰色反应的黄色火焰判断试液是否含Na+,故A错误;
B.试液是葡萄糖酸盐溶液,其中一定含葡萄糖酸根,葡萄糖能发生银镜反应,葡萄糖酸根不能发生银镜反应,故B错误;
C.根据“控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀”信息,在过滤除去Fe(OH)3的滤液中分别加入NH3•H2O(aq)和Na2CO3(aq),加入NH3•H2O(aq)不产生沉淀说明滤液中不含Mg2+,加入Na2CO3(aq)产生白色沉淀,说明滤液中含Ca2+,故C正确;
D.溶液加入H2O2后再滴加KSCN(aq)显血红色,不能证明葡萄糖酸盐试液中是否含Fe2+,正确的方法是:在溶液中滴加KSCN(aq)不显血红色,再滴入滴加H2O2显血红色,证明溶液中只含Fe2+.若此前各步均没有遇到氧化剂,则可说明葡萄糖酸盐试液中只含Fe2+,故D错误
考查方向
物质检验鉴别
解题思路
A.加入了NaOH (aq)和Na2CO3(aq),在滤液中引入了Na+;
B.葡萄糖酸根不能发生银镜反应;
C.加入NH3•H2O(aq)不产生沉淀说明滤液中不含Mg2+,加入Na2CO3(aq)产生白色沉淀,说明滤液中含Ca2+;
D.溶液加入H2O2后再滴加KSCN(aq)显血红色,不能证明葡萄糖酸盐试液中是否含Fe2+.
易错点
加入NaOH和Na2CO3后引入了Na+
教师点评
本题考查物质的检验和鉴别的实验方案的评价,题目难度不大,注意相关物质的性质的掌握,注意物质的鉴别要排除其它离子的干扰
知识点
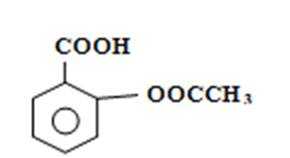
2.阿司匹林(Aspirin)也叫乙酰水杨酸(结构如下图所示)是一种常用的解热镇痛、抗风湿类药物,广泛应用于临床治疗和预防心脑血管疾病,近年来还不断发现它的新用途。下列有关说法正确的是
正确答案
解析
A.具有相同官能团-COOH、-COOC-,-COOH与-OOCCH3具有间、对位,-COOH与-COOCH3具有邻、间、对位,-CH2COOH与-OOCH具有邻、间、对位,还含-CH(COOH)OOCH3,共9种,故A错误;
B.含苯环可发生加成反应、还原反应,含-COOH、-COOC-可发生取代反应,燃烧为氧化反应,故B正确;
C.含甲基为四面体结构,不可能所有原子均在同一平面上,故C错误;
D.该物质含有羧基,具有酸性,所以服用阿司匹林药量过大时,可出现精神错乱、惊厥甚至昏迷等水杨酸反应,可用碳酸氢钠溶液解毒,故D错误
考查方向
有机物的结构和性质
解题思路
该分子中含有羧基和酯基、苯环,具有羧酸、酯、苯的性质,能发生取代反应、酯化反应、中和反应、水解反应、加成反应等,据此分析解答
易错点
A项:同分异构体判断
教师点评
本题考查有机物结构和性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查
知识点
16.向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH(aq),生成沉淀的质量与滴
入NaOH(aq)的体积关系如图。原混合溶液中MgCl2与 FeCl3的物质的量之比为
正确答案
解析
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,首先发生反应NaOH+HCl=NaCl+H2O,即为图象中0-amL,沉淀的质量为0g;FeCl3只能在酸性较强的溶液中存在,当酸性减弱时,会转化为Fe(OH)3沉淀,从amL开始,bmL时沉淀完全.bmL时,溶液仍然呈酸性,到cmL时,才开始产生Mg(OH)2沉淀,
令氢氧化钠浓度为x,
Fe3+完全沉淀消耗氢氧化钠为(b-a)mL,结合Fe3++3OH-═Fe(OH)3↓可知,溶液中
Mg2+完全沉淀消耗氢氧化钠为(d-c)mL,结合Mg2++2OH-═Mg(OH)2↓可知,溶液中
故原混合溶液中
考查方向
混合物的有关计算
解题思路
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,首先发生反应NaOH+HCl=NaCl+H2O,即为图象中0-amL,沉淀的质量为0g;FeCl3只能在酸性较强的溶液中存在,当酸性减弱时,会转化为Fe(OH)3沉淀,从amL开始,bmL时沉淀完全.bmL时,溶液仍然呈酸性,到cmL时,才开始产生Mg(OH)2沉淀,结合Fe3++3OH-═Fe(OH)3↓、Mg2++2OH-═Mg(OH)2↓计算判断
易错点
图像中各段所对应的沉淀
教师点评
本题以图象形式考查混合物的有关计算,题目难度较大,清楚各段发生的反应是解题关键
知识点
2.用试纸检验气体是一种重要的实验方法。下列试纸的选用以及对应的现象、结论都正确的一项是
正确答案
解析
A.二氧化碳气体不能使干燥pH试纸变色,则干燥的pH试纸不能检验CO2,故A错误;
B.二氧化硫使品红褪色,则SO2能使湿润的品红试纸褪色,因二氧化硫具有漂白性,故B正确;
C.检验氨气利用湿润的红色石蕊试纸,则干燥的红色石蕊试纸不能检验NH3,故C错误;
D.具有氧化性的气体能使湿润的淀粉碘化钾试纸变蓝,如氯气、臭氧、二氧化氮等,故D错误
考查方向
本题考查物质的检验和鉴别
解题思路
A.二氧化碳气体不能使干燥pH试纸变色
B.二氧化硫使品红褪色;
C.检验氨气利用湿润的红色石蕊试纸;
D.具有氧化性的气体能使湿润的淀粉碘化钾试纸变蓝
易错点
各种试纸的使用
教师点评
本题考查物质的检验和鉴别,在近几年的各省高考题中出现的频率非常高,常与物质的性质等知识点交汇命题
知识点
扫码查看完整答案与解析