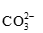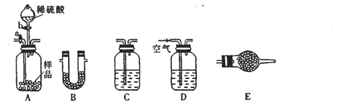- 常见无机物及其应用
- 共1311题
10.下列实验中,所采取的分离方法与对应原理都正确的是
正确答案
B
解析
A.二氧化碳能与碳酸钠溶液反应,将消耗二氧化碳,应该采用饱和的碳酸氢钠溶液,故错误
B.蒸馏分离法利用液态混合物中物质沸点的差异性,差异越大越有利于蒸馏,故正确。
C.采用重结晶法分离是利用物质的溶解度受温度的影响大小,故错误。
D.采用分液漏斗分离液态物质是利用液态物质之间互不相容而导致分层性质,与密度无关,故错误。
考查方向
解题思路
分离提纯需要考虑过程中不能引入新的杂质这一原则。
易错点
元素及其化合物的化学性质、物理性质
知识点
11.下列有关说法正确的是( )
正确答案
解析
本题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
知识点
13.已知:2C(s)+O2(g)=2CO(g)ΔH=-217kJ·mol-1C(s)+H2O(g)=CO(g)+H2(g)ΔH=b kJ·mol-1H-H、O-H和O=O键的键能分别为436、462和495kJ·mol-1,则b为
正确答案
解析
由已知可知2C(s)+2H2O(g)=2CO(g)+2H2(g) ΔH=2b kJ·mol-1,再与2C(s)+O2(g)=2CO(g)ΔH=-217kJ·mol-1相减,得到:2H2(g) + O2(g) =2H2O(g) ΔH=-217-2b kJ·mol-1 ,由于ΔH=反应物总键能 - 生成物总键能,可知:-217-2b = 2*436 + 495 - 4*462。
考查方向
解题思路
先写出目标方程式,ΔH=反应物总键能 - 生成物总键能。
易错点
盖斯定律的应用。
知识点
化学与科学、技术、社会、环境密切相关。下列说法正确的是
正确答案
解析
试题分析:A,盐酸与氢氧化钠的反应不是氧化还原反应,不能用作原电池原理,错误;B,“地沟油”主要成分是高级脂肪酸甘油酯,生物柴油又称为生质柴油,是用未加工过的或者使用过的植物油以及动物脂肪通过不同的化学反应制备出来的一种被认为是环保的生质燃料,故B正确;C.铁粉当为吸氧剂,错误;D.稀硫酸会腐蚀铝表面的氧化膜,错误。
知识点
化学与生活密切相关。下列说法不正确的是
正确答案
解析
略
知识点
光谱研究表明,易溶于水的S02所形成的溶液中存在着下列平衡:
据此,下列判断中正确的是
正确答案
解析
本题主要考察化学平衡状态的特点和外界条件对化学平衡对影响。因为该反应是可逆反应,所以达到平衡后反应物和生成物共同存在与体系中,所以选项A正确;溶液中H+的来源有3个方面,即水的电离、SO2·xH2O和HSO3-的电离,因此溶液中H+浓度不一定是SO32-浓度的2倍,选项B错误;SO2是一种还原性气体,若加入的酸是氧化性酸,SO2将被氧化成硫酸而不会放出SO2气体,选项C错误;NaHSO3是一种酸式盐可以与NaOH反应,方程式为NaHSO3+NaOH=Na2SO3+H2O,选项D也错误。
知识点
甲醛与亚硫酸氢钠的反应方程式为HCHO+NaHSO3
正确答案
解析
从化学组成上讲吊白块相当于钠盐,易溶于水,由于生产吊白块的反应为可逆反应,因此吊白块使用时会释放出甲醛,因此不能用于食品加工,由于甲醛可使蛋白质变性,具有防腐作用,故工业上常用作防腐剂。
知识点
化学与生活密切相关,下列说法不正确的是
正确答案
解析
略
知识点
10.下表中各组物质之间不能通过一步反应实现如图转化的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.2010年元旦,以沉睡在海底800余年的古沉船“南海一号”(图3)为主体建成的广东海上丝绸之路博物馆正式对外开放,翻开了我国考古和科普工作的新篇章。下列叙述中不正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
5.二氧化硫能使溴水褪色,说明二氧化硫具有( )
正确答案
解析
【解析】二氧化硫具有还原性,与溴水发生氧化还原反应生成氢溴酸和硫酸,使溴水褪色,硫元素化合价升高,体现还原性.故选A.
考查方向
解题思路
二氧化硫与溴水发生氧化还原反应生成氢溴酸和硫酸.
易错点
本题主要考查了二氧化硫的性质,侧重考查二氧化硫的还原性,注意中间价态的元素既有氧化性又有还原性,同种元素相邻价态间不发生氧化还原反应,题目难度不大.
知识点
7.下列实验设计正确的是
A.将SO2通入溴水中证明SO2具有漂白性
B.将铁屑放入稀HNO3中证明Fe比H2活泼
C.将澄清石灰水滴入某溶液证明其中存在
D.将乙烯通入KmnO4酸性溶液证明乙烯具有还原性
正确答案
D
知识点
28.某研究小组将纯净的SO2气体通入0.1mol·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能养护通入的SO2,该小组突出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设
该小组涉及实验验证了假设一,请在下表空白处填写相关实验现象
(2) 为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线入下图
实验1中溶液pH变小的原因是____;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)_________。
(3)验证假设二:
(4)验证假设二
请设计实验验证假设二,写出实验步骤,预期现象和结论。
(5)若假设二成立,请预测:在相同条件下,分别欧诺个足量的O2和KNO3,氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反映后两溶液的pH前者_______(填大于或小于)后者,理由是___________。
正确答案
(1)无明显现象 有白色沉淀生成
(2)

(或
(3)
(4)小于 反应的离子方程式表明,足量的



解析
解析已在路上飞奔,马上就到!
知识点
化学源于生活又用于生活,下列有关应用不正确的是
正确答案
解析
试题分析:A,乙烯是植物生长调节剂,高锰酸钾能把乙烯氧化为二氧化碳,从而可以降低乙烯的含量。故用浸泡高锰酸钾溶液的硅土来吸收水果或花朵产生的乙烯以达到保鲜效果。正确。B,我们日常生活经常食用的淀粉、蛋白质都是天然高分子化合物,而豆油是高级脂肪酸的甘油酯,不是高分子化合物。错误。C,船身上附装金属Zn,Fe、Zn及海水就构成了原电池。由于Zn的活动性比Fe强,作原电池的负极,发生氧化反应。Fe就得到了保护。因此是利用了Zn的金属活泼性。正确。D,含硫化石燃料在燃烧时会产生大量的SO2,SO2与空气中的水发生反应产生亚硫酸,进而被空气中的氧气氧化为硫酸导致酸雨。故大量燃烧是酸雨形成的主要原因之一。正确。
知识点
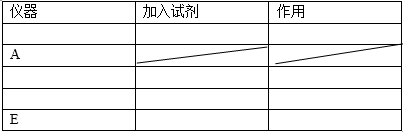
29.完成对硫代硫酸钠(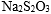
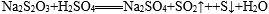
(1)请填写下表(按仪器连接顺序由上到下依次填入,各仪器只能使用一次)。可供选用的试剂有品红溶液、NaOH溶液、浓硫酸、无水硫酸铜、碱石灰。
(2)若实验中称取m1g混合物样品进行实验。
①组装好上述仪器后,应首先进行的实验操作是( ),
②若实验前后装置C的质量分别为m2g、m3g,装置B的质量分别为m4g、m5g,则样品中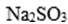
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析