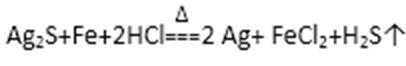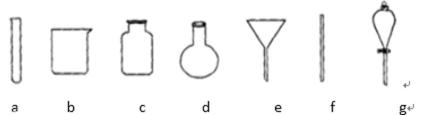- 有机物的性质实验
- 共50题
【选做题】本题包括A、B两小题,请选定一中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A [物质结构与性质](请回答35-41题)
下列反应曾用于检测司机是否酒后驾驶:
2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
B实验化学](请回答38-42题)
实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图,相关物质的沸点见附表)。其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。步骤4:减压蒸馏有机相,手机相应馏分。
35.Cr3+基态核外电子排布式为_________;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是________(填元素符号)。
36.CH3COOH中C原子轨道杂化类型为______________,1mol CH3COOH分子中含有σ键的数目为 。
37.与H2O互为等电子体的一种阳离子为________(填化学式);H2O与CH3CH3OH可以任意比例互溶,除因为它们都是极性分子外,还因为___________。
38.实验装置中冷凝管的主要作用是________,锥形瓶中的溶液应为________。
39.步骤1所加入的物质中,有一种物质是催化剂,其化学式为_________。
40.步骤2中用10%NaHCO3溶液洗涤有机相,是为了除去溶于有机相的______(填化学式)。
41.步骤3中加入无水MgSO4固体的作用是_________。
42.步骤4中采用减压蒸馏技术,是为了防止_____。
附表 相关物质的沸点(101kPa)
正确答案
1s22s22p63s23p63d3 O
解析
(1)Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,则离子的电子排布为1s22s22p63s23p63d3,配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体,O原子提供孤对电子,与Cr3+形成配位键,故答案为:1s22s22p63s23p63d3;O;
考查方向
解题思路
(1)Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体;
易错点
本题涉及核外电子排布、杂化类型等问题,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.
正确答案
sp3和sp2 7mol或7×6.02×1023
解析
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,分别为sp3杂化、sp2杂化,CH3CHOOH分子中含有1个C﹣C、3个C﹣H、1个C﹣O、1个C=O、1个O﹣H等化学键,则1mol CH3COOH分子中含有σ键的数目为7mol或7×6.02×1023,故答案为:sp3和sp2;7mol或7×6.02×1023;
考查方向
解题思路
(2)CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,CH3CHOOH分子中含有1个C﹣C、3个C﹣H、1个C﹣O、1个C=O、1个O﹣H等化学键;
易错点
本题涉及杂化类型,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.
正确答案
H2F+ H2O与CH3CH3OH之间可以形成氢键
解析
(3)与H2O互为等电子体的阳离子应含有3个原子、且电子数为10,应为H2F+,H2O与CH3CH3OH都含有氢键,且都为极性分子,二者互溶,故答案为:H2F+;H2O与CH3CH3OH之间可以形成氢键.
考查方向
解题思路
(3)与H2O互为等电子体的阳离子应含有3个原子、且电子数为10,H2O与CH3CH3OH都含有氢键,且都为极性分子,二者互溶.
易错点
本题考查等电子体等问题,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.
正确答案
冷凝回流 NaOH
解析
(1)因溴易挥发,为使溴充分反应,应进行冷凝回流,以增大产率,反应发生取代反应,生成间溴苯甲醛的同时生成HBr,用氢氧化钠溶液吸收,防止污染空气,故答案为:冷凝回流;NaOH;
考查方向
解题思路
苯甲醛与溴在氯化铝催化作用下在60℃时反应生成间溴苯甲醛,通式生成HBr,经冷凝回流可到间溴苯甲醛,生成的HBr用氢氧化钠溶液吸收,防止污染空气,有机相中含有Br2,加入HCl,可用碳酸氢钠除去,有机相加入无水MgSO4固体,可起到吸收水的作用,减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化,以此解答该题.
(1)因溴易挥发,为使溴充分反应,应进行冷凝回流,以增大产率,反应发生取代反应,生成间溴苯甲醛的同时生成HBr,用氢氧化钠溶液吸收,防止污染空气.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
AlCl3
解析
(2)将三颈瓶中的一定配比的无水AlCl3、1,2﹣二氯乙烷和苯甲醛充分混合,三种物质中无水AlCl3为催化剂,1,2﹣二氯乙烷为溶剂,苯甲醛为反应物,
故答案为:AlCl3;
考查方向
解题思路
(2)将三颈瓶中的一定配比的无水AlCl3、1,2﹣二氯乙烷和苯甲醛充分混合,三种物质中无水AlCl3为催化剂,1,2﹣二氯乙烷为溶剂,苯甲醛为反应物.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
Br2、HCl
解析
(3)将反应混合物含有溴,缓慢加入一定量的稀盐酸中,加入碳酸氢钠,可与Br2、HCl反应,故答案为:Br2、HCl;
考查方向
解题思路
(3)将反应混合物含有溴,缓慢加入一定量的稀盐酸中,加入碳酸氢钠,可与Br2、HCl反应.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
除去有机相的水
解析
(4)经洗涤的有机相含有水,加入适量无水MgSO4固体,可起到除去有机相的水的作用,故答案为:除去有机相的水;
考查方向
解题思路
(4)经洗涤的有机相含有水,加入适量无水MgSO4固体,可起到除去有机相的水的作用.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
正确答案
间溴苯甲醛被氧化
解析
(5)减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化,故答案为:间溴苯甲醛被氧化.
考查方向
解题思路
(5)减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化.
易错点
本题考查有机物的制备,侧重于学生的分析能力和实验能力的考查,注意把握基本实验操作方法以及实验的原理,难度不大.
有文献记载:在强碱条件下,加热银氨溶液可能析出银镜。某同学进行如下验证和对比实验。
该同学欲分析实验Ⅰ和实验Ⅱ的差异,查阅资料:
a, Ag(NH3)-2+2H2O=Ag-+2 NH3+ H2O
b,AgOH不稳定,极易分解为黑色Ag2O
(1)配制银氨溶液所需的药品是 。
(2)经检验,实验Ⅰ的气体中有NH3,黑色物质中有Ag2O.
①用湿润的红色石蕊试纸检验NH3产生的现象是 。
②产生Ag2O的原因是 。
(3)该同学对产生银镜的原因提出假设:可能是NaOH还原Ag2O。实验及现象:向AgNO3
溶液中加入 ,出现黑色沉淀,水浴加热,未出现银镜。
(4)重新假设:在NaOH存在下。可能是NH3, 还原Ag2O。用下图所示装置进行实验.现象:
出现银镜。在虚线框内画出用生石灰和浓氨水制取NH3的装置简图(夹持仪器略)。
(5)该同学认为在(4)的实验中会有Ag(NH3)2OH生成,由此又提出假设:在NaOH存在下,可能是Ag(NH3)2OH也参与了NH3还原Ag2O的反应,进行如下实验:
1 有部分Ag2O溶解在氨水中,该反应的化学方程式是 。
2 验结果证实假设成立,依据的现象是 。
3 用HNO3,消洗试管壁上的Ag,该反应的化学方程式是 。
正确答案
见解析。
解析
(1)AgNO3溶液和氨水。
(2)①试纸变蓝。
②在NaOH存在下,加热NH3·H2O分解,逸出NH3,促使反应:Ag(NH3)2-+2H2O
Ag+与OH-反应立即转化为Ag2O:2OH-+2Ag+=Ag2O↓+H2O
(3)过量NaOH溶液。
(4)
(5)①Ag2O+4NH3·H2O=2Ag(NH3)2OH+3H2O
②与溶液接触的试管壁上析出银镜。
(6)Ag+2HNO3(浓)= Ag NO3+NO2↑+H2O
知识点
下列关于实验室制备乙酸乙酯和乙酸丁酯的描述正确的是
正确答案
解析
略
知识点
下列实验装置或操作正确的是
正确答案
解析
略
知识点
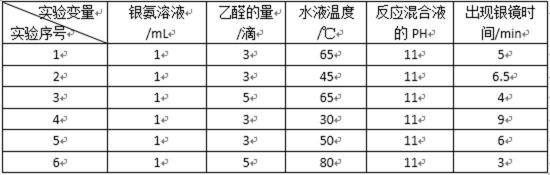
26.乙醛能与银氨溶液反应析出银。如果条件控制适当,析出的银会均匀地分布在试管壁上,形成光亮的银镜,这个反应又叫银镜反应。银镜的光亮程度与反应条件有关。某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究。
Ⅰ. 探究银镜反应的最佳实验条件部分实验数据如下表:
请回答下列问题:
(1)读表若只进行实验1和实验3,其探究目的是()。
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间是();要探索不同水浴温度下乙醛进行银镜反应的最佳条件,除了测量银镜出现的时间外,还需要比较不同条件下形成的银镜的()。
(3)进一步实验 若还要探索银氨溶液的用量对出现银镜快慢的影响,如何进行实验?
Ⅱ. 探究对废液的回收处理:
银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费。通过查找资料,已知从银氨溶液中提取银的一种实验流程为:
操作④的方法是:把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉。反应的化学方程式为:
(4)若获得的银粉中含有少量没有反应完的铁粉,除去铁的反应的离子方程式为(),需要用到的玻璃仪器有()(填编号)。
(5)操作④应在(填实验室设备名称)()中进行。
(6)要洗去试管壁上的银镜,采用的试剂是()(填名称)。
正确答案
见解析。
解析
(1)比较乙醛用量不同时生成银镜的时间(速度或质量均可)
(2)在6.5~9min之间;光亮程度(或亮度、外观、效果等合理均可给分)
(3)保持其他的实验条件不变,改变银氨溶液的用量,测量生成银镜的时间(其它合理表述均可得分)
(4)Fe+2H+==Fe2++H2↑ (其他合理答案也可给分,如Fe +2Fe3+==3Fe2+);b e f(3分)
(5)通风橱
(6)硝酸
知识点
下列有关实验原理或操作正确的是
正确答案
解析
略
知识点
现有下列两套实验装置,用于实验室制取乙酸乙酯或乙酸丁酯。下列说法错误的是
图I 图II
正确答案
解析
略
知识点
8. 乙醛能与银氨溶液反应析出银。如果条件控制适当,析出的银会均匀地分布在试管壁上,形成光亮的银镜,这个反应又叫银镜反应。银镜的光亮程度与反应条件有关。某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究。
一. 探究银镜反应的最佳实验条件部分实验数据如下表:
请回答下列问题:
(1)读表若只进行实验1和实验3,其探究目的是 ___________________ 。
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间是 ___________ ;要探索不同水浴温度下乙醛进行银镜反应的最佳条件,除了测量银镜出现的时间外,还需要比较不同条件下形成的银镜的 ____________。
(3)进一步实验 若还要探索银氨溶液的用量对出现银镜快慢的影响,如何进行实验?
二、探究对废液的回收处理:
银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费。通过查找资料,已知从银氨溶液中提取银的一种实验流程为:
操作④的方法是:把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉。反应的化学方程式为:Ag2S+Fe+2HCl2 Ag+ FeCl2+H2S↑
(4)若获得的银粉中含有少量没有反应完的铁粉,除去铁的反应的离子方程式为:_________
,需要用到的玻璃仪器有 ()(填编号)。
a b c d e f g
(5)操作④应在(填实验室设备名称)() 中进行。
(6)要洗去试管壁上的银镜,采用的试剂是 ()(填名称)。
正确答案
(1)比较乙醛用量不同时生成银镜的时间(速度或质量均可)
(2)在6.5~9min之间;光亮程度(或亮度、外观、效果等合理均可给分)
(3)保持其他的实验条件不变,改变银氨溶液的用量,测量生成银镜的时间(其它合理表述均可得分)
(4)Fe+2H+==Fe2++H2↑;b e f
(5)通风橱
(6)硝酸
解析
略
知识点
29.请回答下列实验中的有关问题。
(1)实验室用浓硫酸与乙醇共热制取乙烯,以下是某同学设计的三套气体发生装置。
其中合理的是( )(填序号),该装置中,反应容器的名称是( ) 。
(2)利用如下实验装置制备氨气,并完成氨气的喷泉实验。
②实验时,组装好装置后,下列步骤的正确顺序是( )(填序号)。
a.加入试剂 b.检查装置的气密性 c.关闭K1、K2,打开K3 d.关闭K3、打开K1、K2
e.给A装置试管进行加热f.撤去酒精灯g.用热毛巾敷盖在烧瓶上
③实验中,说明D部分烧瓶中氨气已经收集满的现象是( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
9.下图所示的实验装置不能够达到实验目的的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析