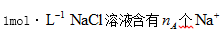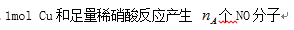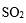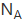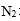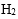- 阿伏加德罗常数
- 共219题
设NA为阿伏伽德罗常数的值。下列说法正确的是
正确答案
解析
本题考查阿伏加德罗常数计算中一些常见问题和注意事项。
A标准状况下,0.1molCl2溶于水,转移的电子数目小于0.1NA,因为Cl2溶于水不可实现完全与水反应。
C标准状况下CH3CH2OH为液态,无法计算。
D常温常压下,2.24L CO和CO2混合气体中含有的碳原子数目不好计算,非标准状况。
解决此类问题的关键是:灵活应用各种知识,尤其基本概念与理论中元素守恒、化学键问题、晶体结构问题、氧化还原中电子转移问题、可逆反应问题及物质的量计算中一些特殊物质的状态等。
知识点
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为ag,则该混合物
正确答案
解析
略
知识点
用NA表示阿伏加德罗常数,下列说法正确的是( )
正确答案
解析
解析:0.1 mol的2H35Cl分子中的中子数是1。9NA,A项错误;气体产物中氮元素的化合价都低于+5价,故气体产物均为还原产物,还原产物氮原子的物质的量大于1mol,根据氮原子的守恒,被还原的硝酸的物质的量也大于1mol, B项正确;铁做阳极电解食盐水时,阳极铁失电子,该极不会产生气体,C项错误;D项忽视了CO2-3和HCO-3的水解以及HCO-3的电离等因素,错误。
知识点
设
正确答案
解析
略
知识点
设nA为阿伏加德罗常数的数值,下列说法正确的是
正确答案
解析
略
知识点
设NA为阿伏伽德罗常数的值。下列说正确的是
正确答案
解析
略
知识点
设NA为阿伏伽德罗常数的值。下列叙述正确的是
正确答案
解析
本题考查阿伏加德罗常数计算中一些常见问题和注意事项。
A.1mol甲醇中含有C—H键的数目为3NA。
B.无溶液体积无法计算OH-的数目。
C.标准状况下已烷为液态,无法计算。
D.Na2O2与足量H2O反应,共生成0.2molO2,O的化合价-1价转变为0价,转移电子1mol,0.2×2=0.4 NA。
解决此类问题的关键是:灵活应用各种知识,尤其基本概念与理论中元素守恒、化学键问题、晶体结构问题、氧化还原中电子转移问题、可逆反应问题及物质的量计算中一些特殊物质的状态等。
知识点
设nA 为阿伏伽德罗常数的数值 ,下列说法正确的是
正确答案
解析
B 应该是转移3 nA 个电子。C 应该是小于0.1nA 个HCO3 —。D条件错误,应为标准状况。
知识点
设NA为阿伏加德罗常数的值,下列叙述正确的是
正确答案
解析
本题考查阿伏伽德罗常数的应用。HF的沸点19.54℃,在标况下是气态,A项错误;乙烯和丙烯的最简式都是CH2,故7.0 g乙烯和丙烯的混合物含有n(CH2)=0.5 mol,则H原子的物质的量为1 mol,B项正确;浓硫酸与Cu的反应,随着反应的进行,浓硫酸的浓度变稀,就与Cu不反应了,故生成的SO2分子数目小于0.46NA,C项错误;N2与H2反应是可逆反应,不能完全转化,D项错误。
知识点
设NA为阿伏加德罗常数,下列叙述中正确的是
正确答案
解析
略
知识点
扫码查看完整答案与解析