- 反应速率的定量表示方法
- 共55题
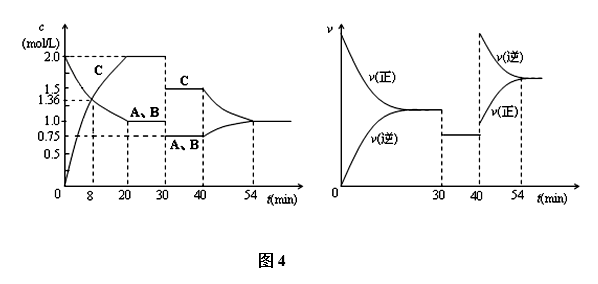
13.某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应是: 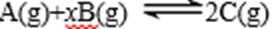
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
29.某化学反应
根据上述数据,完成下列填空:
(1)实验1中,在10~20 min时间内,以A的速率表示的平均反应速率为 ( )。
(2)实验2中,A的初始浓度c2= ( )
(3)测得实验2和实验3各组分百分含量相等。设实验3的化学反应速率为v3,实验1的化学反应速率为v1,则v3 ( ) v1(填“>”“=”或“<”),且c3=( )
(4)实验4和实验1仅起始温度不同。比较实验4和实验1,可推测该反应的正反应是( )反应(填“吸热”或“放热”),理由是( )。
(5)实验4中,假定在50 min将容器的容积缩小为原来的一半,请在下图中用曲线表示体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、D)。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
28.甲醇来源丰富,价格低廉,是一种重要的化工原料,有着非常重要、广泛的用途。工业上通常用水煤气在恒容、催化剂和加热的条件下生产甲醇,其热化学方程式为:2H2(g)+CO(g)
(1)该反应的平衡常数表达式为:K= ,如升高温度,K值将 (填:增大、减小或不变)。
(2)以下各项不能说明该反应达到平衡状态的是 .
(3)在2100C、2400C和2700C三种不同温度、2 L恒容密闭容器中研究合成甲醇的规律。
(4)某兴趣小组设计了如图所示的甲醇燃料电池装置。
② 该电池工作时,正极是 极(填“a”或“b”);
②该电池负极反应的离子方程式为 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.密闭容器中X、Y、Z三种气体的初始浓度和不同温度下的平衡浓度如下表:下列说法错误的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
29.某同学欲探究
请回答下列问题:
(1)用pH试纸测定溶液pH的操作方法是( );
(2)写出生成白色沉淀W所涉及的离子方程式( );
(3)写出
(4)取三支大小相同的试管,通过测定
①V=( );
②探究浓度对化学反应速率的影响,应选择( )(填实验编号)组实验进行对比分析;
③为了准确控制反应的温度,应采用的加热方式为( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析