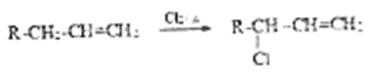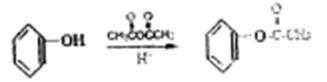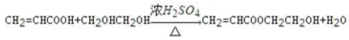- 原子核外电子的运动状态
- 共4题
过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。实验室可用工业碳酸钙(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙,其主要流程如下:
已知:CaO2·8H2O呈白色微溶于水,加热至350℃左右开始分解放出氧气,425℃分解完全。
22.写出反应①中氧化还原反应的离子方程式:___________________________。
23.向反应①后的溶液中加浓氨水的目的是:_________________________________,
______________________________(用方程式表示)
24.反应②常用冰水控制温度在0℃左右,其可能原因是(写出两种):
①__________________________;②__________________________。
25.测定产品中CaO2的含量的实验步骤是
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。已知:I2+2S2O===2I-+S4O。
某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________(填“不受影响”“偏低”或“偏高”),原因是____________________.
正确答案
3FeCO3+10H++NO3-===3Fe3++NO↑+3CO2↑+5H2O
解析
反应①中氧化还原反应的离子方程式:3FeCO3+10H++NO3-===3Fe3++NO↑+3CO2↑+5H2O
考查方向
解题思路
工业碳酸钙(含MgCO3、FeCO3等杂质)加硝酸(强氧化性)反应成Mg2+、Fe3+
易错点
根据图示流程中找出反应物、生成物,写出反应的化学方程式。
正确答案
Mg2+、Fe3+沉淀完全(方程式略)
解析
由流程可知,反应物为Mg2+、Fe3+与氨气和水反应将生成氢氧化镁和氢氧化铁沉淀。
考查方向
解题思路
向反应①后的溶液中加浓氨水的目的由流程可知,反应物为Mg2+、Fe3+与氨气和水反应将生成氢氧化镁和氢氧化铁沉淀。
易错点
根据图示流程中找出反应物、生成物,写出反应的化学方程式。
正确答案
①防止H2O2分解,提高其利用率
②降低CaO2·8H2O溶解度,提高产率
解析
由于双氧水受热易分解,所以温度低可减少过氧化氢的分解,提高过氧化氢的利用率;另一方面该反应是放热反应,温度低有利于提高CaO2·8H2O产率。
考查方向
解题思路
温度低可减少过氧化氢的分解,有利于提高CaO2·8H2O产率。
易错点
根据图示流程中找出反应物、生成物,写出反应的化学方程式。
正确答案
偏高 在酸性条件下空气中的O2也可以把KI氧化为I2,使消耗的Na2S2O3增多,从而使测得的CaO2的质量分数偏高
解析
如果滴速过慢,而空气中的氧气在酸性条件下也可以把KI氧化为I2,使消耗的Na2S2O3增多,从而使测得的CaO2的质量分数偏高。
考查方向
解题思路
空气中的氧气在酸性条件下也可以把KI氧化为I2。
易错点
根据空气中的氧气能够氧化碘离子,使碘单质的量增加,消耗的硫代硫酸钠增加分析。
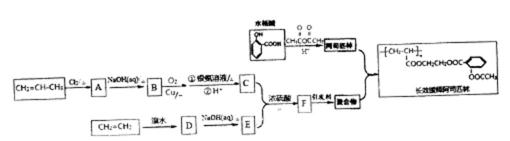
32.【有机化学基础】
阿司匹林,是一种历史悠久的解热镇痛药,还能抑制血小板聚集,广泛应用于心脑血管疾病的治疗,以水杨酸(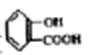
己知:
①
②
③1分子C和1分子 E在浓硫酸作用下脱去1分子水反应生成F,
请回答:
(1)由A生成B的反应类型为_____________。
(2)写出C和E反应生成F的化学方程式_____________
(3)写出符合下列条件的水杨酸的任意一种同分异构体的结构简式______________________。
①含柯苯环结构,苯环上只有两个取代基
②与FeCl3反应显紫色
③能发生银镜反应
(4)1mol阿司匹林与足量NaOH溶液反成,最多消耗________mol NaOH;
(5)长效缓释阿西匹林中含氧官能团的名称为_____________。
正确答案
(1)水解(取代)反应
(2)
(3)
(4)3
(5)酯基
解析
解析已在路上飞奔,马上就到!
知识点
14.图示是

正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.丙烯酸的结构简式为CH2= CH-COOH,下列关于丙烯酸的说法错误的是( )
正确答案
解析
A、丙烯酸含有羧基,所以能与醇发生酯化反应;
B、丙烯酸含有碳碳双键,所以能使酸性高锰酸钾溶液发生氧化反应;
C、丙烯酸与HBr发生加成反应能得到2种产物H加在CH2= CH左侧和右侧;
D、丙烯酸钠溶液中丙烯酸根离子会发生水解;
考查方向
解题思路
丙烯酸中含有的官能团是碳碳双键和羧基,所以丙烯酸具有烯烃和羧酸的性质
易错点
本题考查有机物的结构和性质,易错点在于明确丙烯酸含有的官能团以及官能团所具有的性质是解本题的关键。
知识点
扫码查看完整答案与解析