- 原电池和电解池的工作原理
- 共168题
下列叙述中正确的是
正确答案
解析
略
知识点
下列叙述中正确的是
正确答案
解析
略
知识点
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含氰废水中的CN-有剧毒。
①CN-中C元素显+2价, N元素显-3价,用原子结构解释N元素显负价的原因是 ,共用电子对偏向N原子,N元素显负价。
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为 。
(2)含乙酸钠和对氯酚(
①B是电池的 极(填“正”或“负”);②A极的电极反应式为 。
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如下图所示(图中“HA”表示乳酸分子,A- 表示乳酸根离子)。
① 阳极的电极反应式为 。
② 简述浓缩室中得到浓乳酸的原理: 。
③ 电解过程中,采取一定的措施可控制阳极室的pH约为6-8,此时进入浓缩室的OH-可忽略不计。400mL 10 g•L-1乳酸溶液通电一段时间后,浓度上升为145 g•L-1(溶液体积变化忽略不计),阴极上产生的H2在标准状况下的体积约为 L。(乳酸的摩尔质量为90 g• mol-1)
正确答案
见解析。
解析
(1)①C、N同周期,原子半径:N<C;非金属性:N>C;得电子能力N>C
②2CN-+O2+4H2O 
(2)①负②
(3)①4OH-—4e-=2H2O+O2↑
② 阳极OH-放电,c(H+)增大,H+从阳极通过阳离子交换膜进入浓缩室;A-通过阴离子交换膜从阴极进入浓缩室,H+ +A- = HA,乳酸浓度增大。
③ 6.72
知识点
铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
正确答案
解析
略
知识点
硫化物在自然界中的部分循环关系如下。
(1)H2S在空气中可以燃烧。
已知: 2H2S(g) + O2(g) 
S(s) + O2(g) 
H2S(g)与O2(g)反应产生SO2(g)和H2O(g)的热化学方程式是 。
(2)SO2是大气污染物,海水具有良好的吸收SO2的能力,其过程如下。
① SO2溶于海水生成H2SO3,H2SO3最终会电离出SO32—,其电离方程式是 。
② SO32—可以被海水中的溶解氧氧化为SO42—。海水的pH会 (填“升高” 、“不变”或“降低”)。
③ 为调整海水的pH,可加入新鲜的海水,使其中的HCO3—参与反应,其反应的离子方程式是 。
④ 在上述反应的同时需要大量鼓入空气,其原因是 。
(3)自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS,慢慢转变为铜蓝(CuS),用化学用语表示由ZnS转变为CuS的过程: 。
(4)SO2和O2在H2SO4溶液中可以构成原电池,其负极反应式是 。
正确答案
见解析。
解析
(1)2H2S(g)+3O2(g) 
(2)① H2SO3

② 降低
③ HCO3 —+ H+ 
④提高脱硫海水的溶解氧,将SO32-氧化成为SO42-,有利于平衡H2SO3

(3)
(4)负极:SO2 - 2e—+ 2H2O 
知识点
以铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)为原料,可制得液体聚合氯化铝[Alm(OH) nCl3m-n],生产的部分过程如下图所示(部分产物和操作已略去)。
已知某些硫化物的性质如下表:
(1)操作Ⅰ是 。Al2O3与盐酸反应的离子方程式是 。
(2)滤渣2为黑色,该黑色物质的化学式是 。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。
NaClO的作用是 。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。
反应的化学方程式是 。
(5)将滤液3电解也可以得到液体聚合氯化铝。装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)。
① 写出阴极室的电极反应: 。
② 简述在反应室中生成聚合氯化铝的原理: 。
正确答案
见解析。
解析
(1)过滤 Al2O3+6H+=2Al3++3H2O
(2)CuS(2分)
(3)将Fe2+氧化为Fe3+,使Fe3+转化为Fe(OH) 3沉淀
(4)mAlCl3+nH2O = Alm(OH) nCl3m-n+nHCl
(5)①2H++2e-=H2↑
②电解过程中反应室中的Cl-通过阴离子交换膜进入阳极室,阴极室中的OH-通过阴离子交换膜进入反应室,生成聚合氯化铝。
知识点
由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的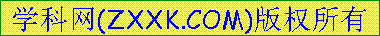
正确答案
解析
略
知识点
某兴趣小组设计如下微型实验装置,实验时,先断开K2,闭合K1,两极均有 气泡产生,一段时间后,断开K1,闭合K2,发现电流计A指针偏转,下列有关描述正确的是
正确答案
解析
略
知识点
下列叙述不正确的是
正确答案
解析
略
知识点
综合下图判断,下列叙述不正确的是
正确答案
解析
略
知识点
扫码查看完整答案与解析