- 元素周期律的实质
- 共71题
9.右表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,Z元素的核电荷数为X与Y元素核电荷数之和。下列说法正确的是
正确答案
解析
由Z元素的核电荷数为X与Y元素核电荷数之和,可得X为C元素,Z为Si元素,Y为O元素,W为S元素,T为Se.元素 。
A选项氢化物稳定性Y比W强即H2O>H2S,是因为O的非金属性强与S,不是因为H2O中存在氢键,错误

C选项一定条件下,X单质能与ZY2反应生成Z单质,即2C + SiO2 Si + 2CO 是熵增反应高温自发反应,并不是C的非金属性比Si强。
D选项根据元素周期律,同主族元素化学性质有相似性,在金属与非金属的分界线附近的元素既具有金属元素的性质,又具有非金属元素的性质,很多是良好的半导体材料,所以Na与Se能形成Na2Se2化合物。正确
A选项不正确,B选项不正确,C选项不正确,所有选D选项。
本题正确答案是D
考查方向
解题思路
由Z元素的核电荷数为X与Y元素核电荷数之和,可得X为C元素,Z为Si元素,Y为O元素,W为S元素,T为Se.元素 。根据各元素的性质,可解答此题。
易错点
元素周期律的推断及同族元素的性质的相似性。
知识点
2.X、Y、Z、W为四种短周期主族元素,且原子序数依次递增,其中X、Z同族,Y是短周期主族
元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,下列说法正确的是()
正确答案
解析
A、HCl为强酸,Cl﹣不水解,故A错误;
B、Cl元素的最高价氧化物对应水化物的酸性一定强于S,不是最高价氧化物的水化物的酸性不能判断酸性强弱,故B错误;
C、X、Y、Z分别为X为O、Na、S,三种元素形成的化合物由Na2SO3、Na2SO4、Na2S2O3等,故C正确;
D、氢化物的稳定性与共价键有关,与氢键无关,O﹣H键能大于H﹣S键能,所以H2O的稳定性大于H2S,故D错误。
故选C
考查方向
解题思路
X原子的最外层电子数是核外电子层数的3倍,则核外各电子层的电子分别为2、6,应为O元素,X、Z同主族,则Z为S元素,W为短周期元素,而且W的原子序数大于S,所以W为Cl元素,Y是短周期主族元素中原子半径最大的,则Y为Na元素
知识点
4.X、Y、Z、W为原子序数依次增大的短周期主族元素,X原子M层有1个电子,Y原子最外层电子数为最内层电子数的2倍,Z元素的最高化合价为最低化合价绝对值的3倍。下列叙述正确的是()
正确答案
解析
元素X是Na, Y是Si, Z是S,W是Cl;
同周期原子半径逐渐减小,正确的是X(Na)>Y(Si)>Z(S),所以A错; 同周期元素的非金属性逐渐增强,最高价氧化物对应的水化物的酸性也是逐渐增强,Y形成的酸是H2SiO3,Z形成的酸是H2SO4,W形成的酸是HClO4,酸性最强的是HClO4,再下来是H2SO4,酸性最弱的是H2SiO3,所以B正确; 气态氢化物的稳定性在同周期从左到右逐渐增强,HCl要比H2S稳定,所以C错误; W分别与X、Y形成的化合物分别是NaCl和SiCl4,NaCl中有离子键,而SiCl4中含有的是共价键没有离子键,化学键类型不相同,所以D错
考查方向
解题思路
X、Y、Z、W为原子序数依次增大的短周期主族元素,X原子M层有1个电子,所以X是Na, Y原子最外层电子数为最内层电子数的2倍,可以确定Y是Si, Z元素的最高化合价为最低化合价绝对值的3倍,则Z是S,那么W是Cl; 同周期原子半径逐渐减小,同周期元素的非金属性逐渐增强,最高价氧化物对应的水化物的酸性也是逐渐增强,气态氢化物的稳定性在同周期从左到右逐渐增强。
易错点
元素的推断和元素周期律的应用出现错误,对最高价氧化物对应的水化物的酸性或是碱性、金属性或非金属性、原子半径、几个元素所形成的化合物的键的类型判断失误
知识点
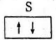
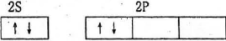
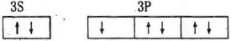
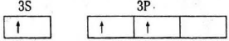
3.轨道表示式是表示原子核外电子运动状态的一种化学用语,下列有关原子的最外层的轨道表示式正确的是
正确答案
解析
A.铍原子最外层应该是2S,故错误。
B.2p能级层上的电子排布违反了洪特规则,同一能级总是先独自占据一个能级轨道。
C.正确。
D.根据能量最低原理,3s轨道低于3p轨道,所以电子先排满3s轨道,故错误
考查方向
解题思路
准确应用构造原理、洪特规则、泡利不相容原理
易错点
构造原理、洪特规则
知识点
8. a、b、c、d为短周期元素,a的M电子层有1个电子,b的最外层电子数为内层电子数的2倍,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c。下列叙述错误的是
正确答案
解析
根据a的M电子层有1个电子可知a元素为金属钠;b的最外层电子数为内层电子数的2倍可知b元素为碳元素;c的最高化合价为最低化合价绝对值的3倍可是c元素为硫元素;c与d同周期,d的原子半径小于c可是d元素为氯元素。综上所述D错误
考查方向
解题思路
根据原子结构以及元素周期表的、元素周期律的相关规律推断元素种类
易错点
元素种类的确定
知识点
2.下列化学用语正确的是
正确答案
解析
A.丙烯的实验式 CH2
B.正确
C.CO2的电子式
D.中子数为18的氯原子符号
考查方向
解题思路
认真读清题目要求,熟练掌握化学用语。
易错点
有机物分子式、实验式、结构简式等易混淆,CO2的电子式易错
知识点
12.4种短周期元素X、Y、Z、W的原子序数依次增大,依据表中信息判断,下列说法不正确的是
正确答案
解析
Na2O2中就有离子键和共价键,所以C错了。
考查方向
解题思路
四种元素0 Na Al S的原子结构,分析化学反应
易错点
化学反应小推断
知识点
3.现有X、Y、Z、M四种短周期元素,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法不正确的是()
正确答案
解析
短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,则X是H元素,Z的核电荷数是M的2倍且Z、M位于同主族,所以Z是S元素、M是O元素,因为Y、Z位于同周期,所以Y是Na元素,即X、Y、Z、M分别是H、Na、S、O元素.
A.原子失电子能力越强,其简单阳离子得电子能力越弱,Na失电子能力大于H,所以得电子能力:H+>Na+,即简单阳离子的氧化性:Y<X;
B.非金属的金属性越强,其气态氢化物越稳定,非金属性M>Z,所以气态氢化物的稳定性:Z<M;
C.电子层数越多,其离子半径越大,电子层结构相同的离子,离子半径随着原子序数的增大而减小,S2-电子层数最多,所以其离子半径最大,Na+半径小于O2-,所以这三种离子半径大小顺序是Z>M>Y;
D.酸或碱抑制水电离,含有弱离子的盐促进水电离,等浓度的H2S与Na2S的溶液中,硫化氢抑制水电离,硫化钠促进水电离,所以水的电离程度:X2Z<Y2Z。
考查方向
解题思路
短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,则X是H元素,Z的核电荷数是M的2倍且Z、M位于同主族,所以Z是S元素、M是O元素,因为Y、Z位于同周期,所以Y是Na元素。
A.原子失电子能力越强,其简单阳离子得电子能力越弱;
B.非金属的金属性越强,其气态氢化物越稳定;
C.电子层数越多,其离子半径越大,电子层结构相同的离子,离子半径随着原子序数的增大而减小;
D.酸或碱抑制水电离,含有弱离子的盐促进水电离.
易错点
本题考查了元素位置结构性质相互关系及应用,解答此题时要熟悉元素周期表的结构及原子之间的关系,再结合元素周期律来分析解答,知道哪些物质促进水电离、哪些物质抑制水电离,同时考查学生灵活运用知识能力。
知识点
4.X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子能形成最轻的气体单质;Y原子的最外层电子数是次外层的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法正确的是()
正确答案
解析
“X元素的原子能形成最轻的气体单质”推得:X是H;“Y原子的最外层电子数是次外层的2倍”推得:Y是C;“Z、W在元素周期表中处于相邻的位置”且都是原子序数比6C大的非金属,“它们的单质在常温下均为无色气体”推得:Z是N、W是O;“M是地壳中含量最高的金属元素”,故M为Al。
A.五种元素的原子半径从大到小的顺序是:Al>C>N>O>H,故M>W>Z>Y>X错误;
B.X、Z两元素能形成原子个数比(X:Z)为3:1的化合物,即NH3,故正确;
C.化合物YW2、ZW2分别是CO2、NO2,只有CO2是酸性氧化物,故错误;
D.用M单质作阳极,石墨作阴极,电解NaHCO3溶液,电解一段时间后,阳极放电产生的Al3+与定向移动到阳极区的HCO3— 发生双水解,而在阳极区会出现白色沉淀,故错误。
考查方向
解题思路
从“最轻的气体单质”入手,结合“位置——结构——性质”的关系逐层推理。
易错点
选项D,白色沉淀应该是在阳极区。
知识点
6.X、Y、Z、W、R均为短周期主族元素,原子序数依次增加,X与W、Y与R分别同主族。Z在短周期元素中金属性最强,W元素原子的次外层电子数为最外层电子数的2倍,R的原子序数是Y的2倍。下列叙述错误是()
正确答案
解析
X是C; Y是O; Z是Na; W是Si; R是S。
A选项中的W和Y的半径大小就是比较,Si在原子半径大于O的半径,是W>Y,所以A对; B选项中比较W和R的最高价含氧酸的酸性的强弱,其中W对应的最高价含氧酸是H2SiO3,R对应的最高价含氧酸是H2SO4,H2SO4的酸性强于H2SiO3的,是R>W,所以B错; C选项是比较Y和R的气态氢化物的稳定性的大小,Y的氢化物是H2O,R的氢化物是H2S,H2O的稳定性强于H2S的,所以,气态氢化物的稳定性是Y>R,所以C对; D选项中Y和Z形成的离子具有相同的电子层结构,核电荷数越大,离子半径越小,所以离子半径是Y>Z,所以D是对的。所以本题选B
考查方向
解题思路
先要推断出各个元素,然后按照同周期和同主族中的周期性变化规律来判断即可。X、Y、Z、W、R均为短周期主族元素,原子序数依次增加,X与W、Y与R分别同主族。Z在短周期元素中金属性最强,短周期中金属性最强的是Na,所以Z为Na元素,W元素原子的次外层电子数为最外层电子数的2倍,可以判定W为Si元素,那么X为C元素,R的原子序数是Y的2倍,可以断定Y为氧元素,R为S元素,
易错点
元素推断错误,对元素周期律中原子半径、离子半径、气态氢化物的稳定性以及非金属性的变化规律的推断错误
知识点
扫码查看完整答案与解析