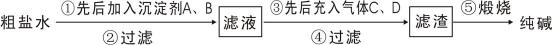- 烃
- 共211题
开学初,小源到建设银行营业网点兑换了此前在网上预约的中国高铁纪念币。这枚纪念币由中国人民银行发行,面额10元,每人限兑20枚,且需要提前预约。小源打算与班上同学分享自己的喜悦。他可以向大家这样介绍
①纪念币面额和实际购买力都是由中国人民银行规定的
②纪念币可以直接购买商品,也具有支付手段等货币职能
③纪念币发行量有限,具有一定的收藏价值和升值空间
④纪念币不能与同面额人民币等值流通,必须在规定时间地点使用
正确答案
解析
①错误,国家无权规定纪念币的实际购买力;④错误,纪念币与同面额人民币等值流通,在任何时间地点都可使用;由中国人民银行发行的纪念币属于法定货币,可以直接购买商品,也具有支付手段等货币职能,因其发行量有限,具有一定的收藏价值和升值空间,故②③正确。
知识点
24.高分子材料PAA、接枝PAA、以及化合物己的合成路线如下:
已知:
Ⅰ.
Ⅱ.两个羧酸分子的羧基之间能失去一分子水:2RCOOH → RCOOOCR +H2O
Ⅲ.
请回答:
(1)F中的官能团名称是( )。
(2) ①Y→W的化学反应方程式( )。
②F → PAA的化学反应方程式是 ( )。
(3)B为中学常见有机物,B与甲均可与FeCl3溶液发生显色反应,丙中的两个取代基互为邻位。
①关于丙的说法正确的是( ) 。
a. 能与银氨溶液发生银镜反应 b. 与有机物B互为同系物
c. 不存在芳香醇类的同分异构体 d.1mol丙与足量的钠反应生成1molH2
②丙有多种同分异构体,写出符合下列条件的同分异构体的结构简式:( )
ⅰ.能发生银镜反应 ⅱ.1mol该物质可与2molNaOH反应
(4)丁的核磁共振氢谱只有一种峰,在酸性条件下能水解,水解产物能与NaHCO3反应产
生CO2。己的结构简式是( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
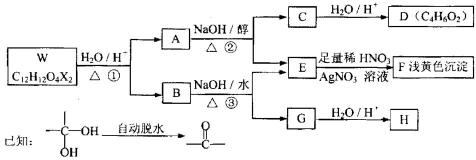
30.有机物W~H有如下的转化关系。已知W、B为芳香族化合物,X为卤素原子,W、A、B均能与NaHCO3溶液反应,A分子中有2个甲基,H分子中含有醛基且苯环请回答下列有关问题:
请回答下列有关问题:
(1)反应①、②分别属于_______反应、________反应(填有机反应类型),
A、B中均含有的含氧官能团的名称是_____________。
(2)F的化学式 _____________,B的结构简式 _____________。
(3)反应②的化学方程式是_________ 。
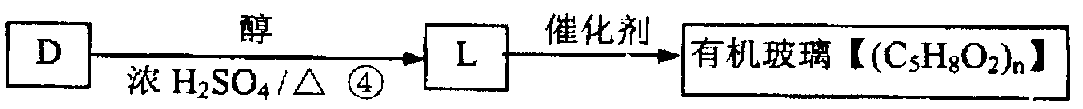
(4)若
反应④的化学方程式是 __________________。
(5)H有多种同分异构体,写出任意一种同时满足(i)遇FeCl3显紫色(ii)苯环上—取代物有两种(iii)除苯环外无其它环状结构3个条件的H的同分异构体结构简式 ___________。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题作答。
36.【化学—选修2化学与技术】(15分)
工业生产纯械的工艺流程示意图如下
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(A来源于石灰窑厂),则B的化学式( )。
(2)②过滤后滤液中要通入C和D气体,则先通入的C气体是( ) (填化学式),原因是
(3)通入C和D气体后发生反应的化学方程式是 ( ) 。
(4)④过滤后,向滤液中通氨气,加入细小食盐颗粒,析出副产品 ( )(填写化学式),
通氨气与加入细小食盐颗粒的作用是 ( ) 。
(5)写出⑤锻烧发生反应的化学方程式 ( )
产品纯碱中含有碳酸氢钠。若用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数ω(NaHCO3)= __________________
[加热前后的质量分别用m(加热前)和m(加热后)表示]
37.【化学——选修物质结构与性质】(15分)元素周期表是研究元素原子结构及性质的重要工具。现有X、Y和Z三种元素,其原子序数依次减小。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子,X跟Y可形成化合物X2Y3。Z元素既可以形成正一价离子也可形成负一价离子。请回答下列问题:
(1)Y元素原子的价层电子的轨道表示式为 ( ),该元素的名称是( );
(2)在X与Z形成的化合物XZ3中,X的杂化类型是 ( ),该化合物的空间构型为_______;短周期元素形成的化合物中与XZ3互为等电子体的是 ( );
(3)请写出X的两种含氧酸的化学式( ) 、( ),其中酸性较强的是( ) 。
(4)Q与Z同主族。Q单质的晶胞如下图所示,若设该晶胞的密度为ag/cm3,阿伏加德罗常数为NA,Q原子的摩尔质量为M,则表示Q原子半径的计算式为( ) 。
38 【化学——选修有机化学基础】(15分)有机物X、Y、Z都是芳香族化合物,X与Z互为同分异构体,Y的分子式为C9H8O,试回答下列问题。
其中Y不能跟金属钠反应;A能跟NaHCO3溶液反应,能使溴的四氯化碳溶液褪色,且苯环上只有一个取代基。Y的分子中所含官能团的名称 ( ) 。
(3)Z可由A经一步反应制得。
①Z的结构简式为 ( ) 或 ( ) ,写出其中一种结构简式与乙醇发生酯化反应的化学方程式 ( )。
②Z有多种同分异构体,其中属于饱和脂肪酸的酯类,且苯环上只有一个侧链的同分异构体有 种,写出其中一种同分异构体的结构简式 ( ) 。
36.【化学—选修2化学与技术】(15分)
工业生产纯械的工艺流程示意图如下
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(A来源于石灰窑厂),则B的化学式 。
(2)②过滤后滤液中要通入C和D气体,则先通入的C气体是 (填化学式),原因是
(3)通入C和D气体后发生反应的化学方程式是 。
(4)④过滤后,向滤液中通氨气,加入细小食盐颗粒,析出副产品 (填写化学式),
通氨气与加入细小食盐颗粒的作用是 。
(5)写出⑤锻烧发生反应的化学方程式
产品纯碱中含有碳酸氢钠。若用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数ω(NaHCO3)= __________________
[加热前后的质量分别用m(加热前)和m(加热后)表示]37.【化学——选修物质结构与性质】(15分)元素周期表是研究元素原子结构及性质的重要工具。现有X、Y和Z三种元素,其原子序数依次减小。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子,X跟Y可形成化合物X2Y3。Z元素既可以形成正一价离子也可形成负一价离子。请回答下列问题:
(1)Y元素原子的价层电子的轨道表示式为 ,该元素的名称是 ;
(2)在X与Z形成的化合物XZ3中,X的杂化类型是 ,该化合物的空间构型为_______;短周期元素形成的化合物中与XZ3互为等电子体的是 ;
(3)请写出X的两种含氧酸的化学式 、 ,其中酸性较强的是 。
(4)Q与Z同主族。Q单质的晶胞如下图所示,若设该晶胞的密度为ag/cm3,阿伏加德罗常数为NA,Q原子的摩尔质量为M,则表示Q原子半径的计算式为 。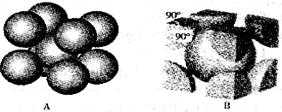
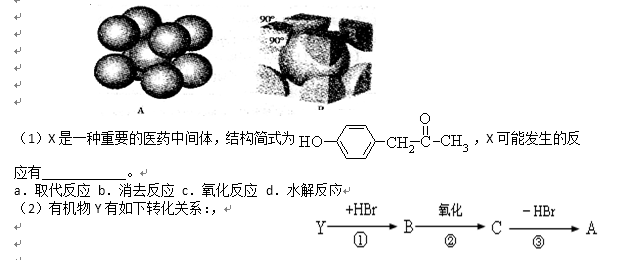
(1)X是一种重要的医药中间体,结构简式为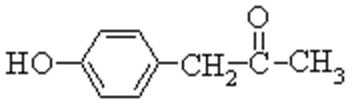

(2)有机物Y有如下转化关系:,
其中Y不能跟金属钠反应;A能跟NaHCO3溶液反应,能使溴的四氯化碳溶液褪色,且苯环上只有一个取代基。Y的分子中所含官能团的名称 。
(3)Z可由A经一步反应制得。
①Z的结构简式为 或 ,写出其中一种结构简式与乙醇发生酯化反应的化学方程式 。
②Z有多种同分异构体,其中属于饱和脂肪酸的酯类,且苯环上只有一个侧链的同分异构体有 种,写出其中一种同分异构体的结构简式 。
正确答案
8. 二氧丙烷(C3 H6 Cl2)的同分异构体共有(不包栝立体异构)()
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
36.【化学一选修2:化学与技术】(15分)
农业生产中使用最广泛的磷肥是过磷酸钙,其主要成分是( )(填化学式);在实际使用中,其不能与草木灰混合施用的原因是(用离子方程式表示) ( ) 。目前常用的湿法磷肥生产工艺是用硫酸分解磷矿石(主要成分为Ca5(PO4)3F),这样处理的主要目的是( ) 。
该生产工艺的有关反应为:
生成的氟化氢会和磷矿中带入的二氧化硅反应生成SiF4,若直接排放到空气中,将严重污染环境。某磷肥厂改进工艺,在吸收塔中将SiF4经水吸收后转化为氟硅酸(H2SiF6)溶液和硅胶(SiO2),实现氟的循环使用和硅胶的合理利用,以减小对环境的污染,同时创造经济效益。工艺流程如下:
(1)写出吸收塔中反应的化学方程式( ) 。
(2)该工艺流程中,设计两个吸收塔的目的是 ( ) 。
(3)氟硅酸与磷酸钙和水反应可生成磷酸二氢钙,原理是:
若利用氟硅酸与磷酸钙和水反应代替硫酸与磷酸钙反应生产Ca(H2PO4)2,理论上lkg氟硅酸可替代_____kg硫酸。
(4)分离得到的硅胶中因含有H2SiF6而称含氟硅胶,含氟硅胶中SiO2易溶于沸腾的氟化铵溶液,得到(NH4)2SiF6溶液,此反应为可逆反应,加入氨水后,二氧化硅重新析出。写出SiO2与氟化铵反应的化学方程式________。
37.【化学——选修物质结构与性质](15分)
(1)右图所示为冰晶石(化学式为Na3AlF6)的晶胞。图中●位于大立方体顶点和面心,○位于大立方体的12条棱的中点和8个小立方体的体心,▽是图中●、○中的一种。图中●、○分别指代哪种粒子 ( ) 、( );大立方体的体心处▽所代表的是( ) (用化学式表示)。
(2)H2S和H2O2的主要物理性质比较如下:
H2S和H2O2的相对分子质量基本相同,造成上述物理性质差异的主要原因
( ) 。
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有_______(填元素符号)。实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有 ( ) 。实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4·H2O晶体。实验中所加C2H5OH的作用是 ( ) 。
38.【化学——选修有机化学基础】(15分)
用作软质隐形眼镜材料的聚合物E是:
一种合成聚合物E的路线如下:
回答下列问题:
(1)A能与新制Cu(OH)2悬浊液反应产生砖红色沉淀,A的结构简式是( );
(2)D中含有的官能团名称为 ( );
(3)D→E的反应类型是 ( ) 反应;
(4)C有多种同分异构体。属于酯且含有碳碳双键的同分异构体共有( ) 种(不考虑顺反异构),写出其中核磁共振氢谱峰面积之比为1:1:1:3的同分异构体的结构简式 ( ) ;
(5)写出由乙烯合成乙二醇的化学方程式。
( ) 。
36.【化学一选修2:化学与技术】(15分)
农业生产中使用最广泛的磷肥是过磷酸钙,其主要成分是 (填化学式);在实际使用中,其不能与草木灰混合施用的原因是(用离子方程式表示) 。目前常用的湿法磷肥生产工艺是用硫酸分解磷矿石(主要成分为Ca5(PO4)3F),这样处理的主要目的是 。
该生产工艺的有关反应为:
2Ca5(PO4)3F+7H2SO4=Ca3(PO4)2+4H3PO4+7CaSO4+2HF
正确答案
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
36.【化学—选修2:化学与技术】(15分)
利用天然气合成氨的工艺流程示意如下:
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH4经一次转化后产生CO 0.9n mol、产生H2 mol(用含n的代数式表示)
(3)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是 .
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于
(写出CO2的一种重要用途)。
(5)整个流程有三处循环(流程图中未完全标出),一是 循环(写循环
物质的化学式,下同),二是 循环,三是 循环。37.[化学——选修3:物质结构与性质](15分)
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)气态氟化氢中存在二聚分子(HF)2,这是由于 。
(2)I3+属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为 ,中心
I原子的杂化轨道类型为 。
(3)基态溴原子的电子排布式为 ,碘原子价电子的电
子排布图为_________________。
(4)卤素互化物如IBr、ICl等与卤素单质结构相似、性质相近。Cl2、IBr、ICl沸点由
高到低的顺序为 ,I和Cl相比,电负性较大的是 ,ICl中I元素的化合价为 。
(5)请推测 ① HClO4、② HIO4、③ H5IO6 [可写成(HO)5IO] 三种物质的酸性由强到弱的顺序为 (填序号)。
(6)卤化物RbICl2加热时会分解为晶格能相对较大的卤化物和卤素互化物,该反应的化学方程式为 。RbICl2的晶体结构与CsCl相似,晶胞边长为685.5pm,RbICl2晶胞中含有 个氯原子,RbICl2晶体的密度是
g·cm-3(只要求列算式,不必计算出数值。阿伏伽德罗常数为NA)。38.【化学—有机化学基础】(15分)
化合物A、B、C、D互为同分异构体,相对分子质量为136,分子中只含碳、氢、氧元素,其中氧的含量为23.5%。实验表明:化合物A、B、C、D均是一取代芳香族化合物, 4种化合物在碱性条件下可以进行如下反应:
回答下列问题
(1)A物质的分子式 。C的结构简式
(2)按要求写出下列化学反应方程式及反应类型
①E和G: ,反应类型 。
②I和浓溴水: 。
(3)符合下列条件的A的同分异构体有多种。写出其中一种苯环上仅含二个支链的同分异构体的结构简式 。
①遇FeCl3显紫色,②可发生银镜反应。
正确答案
8.分子式为C2H7Br,具有苯环的同分异构体共有 ( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
36.“C1化学”是指以研究分子中只含一个碳原子的化合物为原料来合成一系列化工原料和燃料的化学。
(1)煤的气化是获得合成气的一种方法,写出煤气化的主要化学反应方程式:( );
(2)天然气的重整的化学反应方程式为( );
(3)最近科学家提出一种“绿色自由’’构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使空气中的CO2转变为甲醇。其技术流程如下:
①碳酸钾溶液所起的作用是( ) ;
②写出上述流程中分解池中发生反应的化学方程( );
③写出合成塔中发生的化学反应方程式( );
④“绿色自由”构想技术流程中常包括物质和能量的循环利用,上述流程中能体现循环利用的物质有( )。
37.在电解炼铝过程中加入冰晶石(用“A”代替),起到降低Al2O3的熔点等诸多作用,冰晶石的生产原理如下:
2Al(OH)3+ 12HF+ 3 Na2CO3 = 2A+ 3CO2↑+ 9H2O
根据题意完成下列填空:
(1)冰晶石的化学式为( ),含有离子键、( )等化学键;
(2)生成物中含有10个电子的分子是 (写分子式),该分子的空间构型为 ( ),中心原子的杂化方式为 ( );
(3)反应物中电负性最大的元素为( ),写出其原子最外层的电子排布图:
(4)冰晶石由两种微粒构成,冰晶石晶胞结构如图丁所示,位于大立方体顶点和面心,位于大立方体的12条棱的中点和8个小立方体的体心,那么大立方体的
体心处▽所代表的微粒是 ( )(填具体的微粒符号)
(5)Al单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如
下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,请回答:
一个晶胞中Al原子的数目为( );Al晶体的密度为( ) (用字母表示)
38.酒石酸(tartaric acid),即,2,3-二羟基丁二酸,是一种羧酸﹐存在于多种植物中﹐也是葡萄酒中主要的有机酸之一。作为食品中添加的抗氧化剂﹐可以使食物具有酸味。酒石酸最大的用途是饮料添加剂。也是药物工业原料,以烃A为原料合成酒石酸的流程如下:
(1)A的名称为:( ),分子中最多有( )个原子共面;
(2)B中所含官能团的名称是( ),B存在顺反异构,它的顺式结构为( );
(3)C转化为D的反应类型是 ( ),
F转化为G的化学反应方程式是 ( );
(4)F与乙二醇在一定条件下可以发生缩聚反应,该反应的化学方程式是___________
(5)C的同分异构体有多种,其中含有“—COO—”结构的有 ( )种;
(6)欲得到较纯净的酒石酸,需将G从其溶液中分离提纯,查阅相关资料得知G的溶解度受温度影响较大,则分离提纯G的方法是 ( )。
36.“C1化学”是指以研究分子中只含一个碳原子的化合物为原料来合成一系列化工原料和燃料的化学。
(1)煤的气化是获得合成气的一种方法,写出煤气化的主要化学反应方程式:
;
(2)天然气的重整的化学反应方程式为 ;

①碳酸钾溶液所起的作用是 ;
②写出上述流程中分解池中发生反应的化学方程 ;
③写出合成塔中发生的化学反应方程式 ;
④“绿色自由”构想技术流程中常包括物质和能量的循环利用,上述流程中能体现循环利用的物质有 。37.在电解炼铝过程中加入冰晶石(用“A”代替),起到降低Al2O3的熔点等诸多作用,冰晶石的生产原理如下:
2Al(OH)3+ 12HF+ 3 Na2CO3 = 2A+ 3CO2↑+ 9H2O
根据题意完成下列填空:
(1)冰晶石的化学式为 ,含有离子键、 等化学键;
(2)生成物中含有10个电子的分子是 (写分子式),该分子的空间构型为 ,中心原子的杂化方式为 ;
(3)反应物中电负性最大的元素为 ,写出其原子最外层的电子排布图:



体心处▽所代表的微粒是 (填具体的微粒符号)

下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
若已知Al的原子半径为d,NA代表阿伏加德罗常数,Al的相对原子质量为M,请回答:
一个晶胞中Al原子的数目为 ;Al晶体的密度为 (用字母表示)38.酒石酸(tartaric acid),即,2,3-二羟基丁二酸,是一种羧酸﹐存在于多种植物中﹐也是葡萄酒中主要的有机酸之一。作为食品中添加的抗氧化剂﹐可以使食物具有酸味。酒石酸最大的用途是饮料添加剂。也是药物工业原料,以烃A为原料合成酒石酸的流程如下:
已知:① 烃A中碳氢质量比为8:1
②
③ D的分子组成是C4H8O2Cl2 ,核磁共振氢谱显示其有三个峰。
(1)A的名称为: ,分子中最多有 个原子共面;
(2)B中所含官能团的名称是 ,B存在顺反异构,它的顺式结构为 ;
(3)C转化为D的反应类型是 ,
正确答案
请考生从给出的3道物理题、3道化学题、2道生物题中每科任选一题做答。
36.(1)粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO2-4等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号)
(2)工业生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。选择适宜的催化剂,是否可以提高SO2的转化率? (填“是”或“否”),是否可以增大该反应所放出的热量?
(填“是”或“否”);
(3)水是一种重要的自然资源,天然水在净化处理过程中加入的混凝剂可以是 __ (填两种物质名称),其净水作用的原理是
(4)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若某天然水中
c(Ca2)=1.2×10-3mol/L,c(Mg2+)=6×10-4mol/L,则此水的硬度为_________。
(5)若(4)中的天然水还含有c(HCO3-)=8×10-4mol/L,现要软化10m3这种天然水,则需先加入


请回答下列问题:
(1)请写出A的分子式
(2)1molA在氢氧化钠溶液中加热,充分反应消耗氢氧化钠 mol
(3)有机物C可以由乳酸(
a.消去、加成、水解、酸化
b.氧化、加成、水解、酸化
c.取代、水解、氧化、酸化
d.消去、加成、水解、氧化
(4)写出由E制得F的化学方程式: ,
反应类型是
(5)有机物B与乙酸酐(CH3COOCOCH3)直接反应制得阿司匹林(即乙酰水杨酸,分子式 C9H8O4),满足以下条件的阿司匹林的同分异构体有 种。
①苯环上只含有两个侧链 ②有两个酯基 ③能发生银镜反应
写出其中核磁共振氢谱是3:2:2:1的结构简式: 、
正确答案
正确答案
扫码查看完整答案与解析