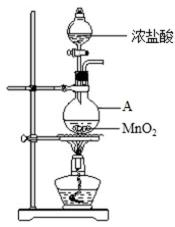
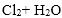- 氯气的实验室制法
- 共24题
下列有关实验原理或实验操作正确的是
正确答案
解析
本题属于基础实验与基本实验操作的考查范畴。
A.pH试纸用水湿润将冲稀待测溶液。
B.0.5000 mol·L-1 H2SO4溶液与水混合,混合溶液的体积不是两者的简单之和。
C.收集试管带塞子将无法收集到氨气。
D.根据溶解平衡原理,Cl2在饱和食盐水溶解度很小,而HCl极易溶解。
本题以pH试纸试用、常见气体制取、溶液配制、除杂中的实验操作为素材,考查学生对实验操作的熟悉程度和实验原理的应用能力,试图引导中学化学教学关注化学实验操作的真实性。
知识点
实验室常用

(1)制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
a往烧瓶中加入
b加热
c往烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出的下列实验方案:
甲方案:与足量

乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量

丁方案:与足量

继而进行下列判断和实验:
①判定甲方案不可行,理由是 。
②进行乙方案实验:准确量取残余清液稀释一定的倍数后作为试样。
a,量取试样20.00mL,用0.1000

b,平行滴定后获得实验结果。
③判断丙方案的实验结果 (填“偏大”、“偏小”或“准确”)。
[已知:



④进行丁方案实验:装置如右图所示(夹持器具义略去)。
(i)使Y形管中的残余清液与锌粒反应的正确操作是将 转移到 中。
(ii)反应完毕,每间隔1分钟读取气体体积、气体体积逐渐减小,直至不变。气体体积逐次减小的原因是 (排除仪器和实验操作的影响因素)。
正确答案
见解析。
解析
(1) ACB
考察实验基本素养。MnO2是固体,浓盐酸是液体,先加固体,后加液体(若颠倒可能引起液体飞溅),最后加热。
(2)①盐酸的浓度不能与溶液中氯离子的浓度。
② 0.1000molL-1,考察酸碱中和滴定的基本原理。注意保留4个有效数字。
③偏小。由于MnCO3的Ksp比CaCO3小,实验中加入过量CaCO3后,部分CaCO3转化为MnCO3,而MnCO3相对分子质量,导致剩余的CaCO3质量偏大,参加反应的CaCO3偏小,盐酸的浓度也就偏小。
④(ⅰ)Zn粒 残余清液,若顺序颠倒,会使残余清液不能完全转移,盐酸就无法完全反应
(ⅱ)气体尚未冷却到室温
知识点
某学习小组依据SO2具有还原性,推测SO2能被Cl2氧化生成SO2Cl2。
查阅资料:SO2Cl2常温下为无色液体,极易水解,遇潮湿空气会产生白雾。
Ⅰ.化合物SO2Cl2中S元素的化合价是 。
Ⅱ.用二氧化锰和浓盐酸制氯气的化学方程式是 。
Ⅲ.在收集氯气前,应依次通过盛有饱和食盐水和 的洗气瓶。
Ⅳ.用如图所示装置收集满Cl2,再通入SO2,集气瓶中立即产生无色液体,
充分反应后,将液体和剩余气体分离,进行如下研究。
(1)研究反应的产物。向所得液体中加水,出现白雾,振荡、静置得到无色溶液。经检验该溶液中的阴离子(除OH-外)只有SO42-、Cl- ,证明无色液体是SO2Cl2。
① 写出SO2Cl2与H2O反应的化学方程式 。
② 检验该溶液中Cl-的方法是 。
(2)继续研究反应进行的程度。用NaOH溶液吸收分离出的气体,用稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀。
① 该白色沉淀的成分是 。
② 写出SO2与Cl2反应的化学方程式,并阐述理由______。
正确答案
见解析。
解析
I.+6价;
II.
Ⅲ.浓硫酸;
Ⅳ.(1)① SO2Cl2+2H2O=H2SO4+2HCl 。
② 取少量该溶液于试管中,加入过量Ba(NO3)2溶液,过滤,向滤液中滴加
HNO3酸化,再加入AgNO3溶液,若产生白色沉淀,则说明溶液中有Cl-;
(2)① BaSO4;
②
由于白色沉淀是BaSO4,所以反应后的混合气体中必然存在SO2和Cl2两种气体。因此SO2和Cl2生成SO2Cl2的反应为可逆反应。
知识点
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:_______。
(2)装置B中饱和食盐水的作用是_______;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:_______。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是_______(填字母编号)。
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是_______,该现象_______(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是_______。
(5)装置F的作用是_______,其烧杯中的溶液不能选用下列中的_______(填字母编号)。
A.饱和NaOH溶液
B.饱和Ca(OH)2溶液
C.饱和Na2SO3溶液
D.饱和Na2CO3溶液
正确答案
(1)Ca(ClO) 2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
(2)除去Cl2中的HCl;B中长颈漏斗中液面上升,形成水柱
(3)d
(4)E中溶液分为两层,上层(苯层)为紫红色;不能;过量的Cl2也可将I-氧化为I2
(5)吸收余氯,防止污染大气;b
解析
略。
知识点
某兴趣小组设计并进行了以下实验来探究Cl2、漂白粉的制备及有关性质。
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:
H→ 、 → 、 → ;广口瓶Ⅱ中的试剂为 。
(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式: ;
某学生设计如下实验进一步探究SO2与漂粉精的反应:
(3)pH试纸颜色的变化说明漂粉精溶液具有的性质是:
(4)该同学推测现象i的雾状物由盐酸小液滴形成,进行如下实验加以进一步验证:
a,用湿润的碘化钾淀粉试纸检验雾状物,无变化;
b,搜集雾状物,用酸化的AgNO3溶液检验,产生白色沉淀。
实验a的目的是 。
(5)现象ⅱ中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的某些成份之间发生反应。请设计实验方案,进一步确认这种可能性,方案为 。
(6)用化学方程式解释现象ⅲ中黄绿色褪去的原因: 。
检验褪色后溶液中是否有
正确答案
(1) BACDE ;饱和食盐水
(2)2Ca(OH)2 +2 Cl2 →Ca(ClO)2 +CaCl2 +2H2O
(3)碱性、漂白性
(4)排除氯气干扰
(5)向漂粉精溶液中逐滴加入硫酸,观察溶液是否变为黄绿色
(6)SO2 +Cl2 +2H2O → H2SO4 +2HCl ;取样,加入足量的硝酸钡,带沉淀沉积后,取上层清夜,滴入硝酸银与稀硝酸,产生白色沉淀,说明有Cl—
解析
略
知识点
某化学研究小组探究溴化亚铁水溶液与氯气反应的性质。
(1)该小组同学用下图所示装置制取氯气。
①写出仪器A的名称_______。
②请写出用浓盐酸和MnO2反应制取Cl2的离子方程式是_______。
③如要制取纯净干燥的氯气,写出仪器C和D中加入的试剂的名称C_______,D_______。
④装置F的作用是_______。
(2)该小组同学对Cl2与FeBr2溶液的反应进行实验探究。
①0.1 mol/L FeBr2溶液显酸性(pH≈4)的原因是_______(用离子方程式表示)。
②现象i中溶液由浅绿色逐渐变黄。某学生猜测可能的原因:
a .Cl2将Fe2+氧化为Fe3+,使溶液呈黄色;
b. Cl2将Br-氧化为Br2,使溶液呈黄色。
请设计实验验证哪种猜测合理_______(说明实验操作、现象和结论)。
③现象ⅱ中,溶液变为棕黄色。某生猜测可能的原因是:
a .可能是Cl2先将Fe2+氧化生成Fe3+, Cl2又继续氧化Br-生成Br2。
b.可能是Cl2先将Fe2+氧化,生成Fe3+,Fe3+将Br-氧化生成Br2。
该小组学生设计如下实验进行验证,请完成下列表格:
根据该实验得出的结论,向含有0.1 molFeBr2的溶液中分别通入0.1molCl2充分反应,写出反应的离子方程式:_______。
正确答案
(1) ①分液漏斗;②MnO2+4H++2Cl-
(2)①Fe2++2H2O
解析
略。
知识点
研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。
(1)仪器A的名称为 ;
A中反应的离子方程式为 。
(2)甲同学将A中产生的气体通入下列溶液:
①实验a中的现象为 。
②不能证明产生的气体中含有HCl的实验是 (填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因: 。
(4)已知:2S2O32- + I2 === S4O62- + 2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 mol•L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 mol•L-1 AgNO3溶液滴定所得溶液中的Cl-。
① X中的HClO不会影响I的测定结果,原因是 。
② 由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 mol•L-1 AgNO3溶液的体积应大于 mL(用含V的代数式表示)。
正确答案
见解析。
解析
(1)圆底烧瓶 MnO2 + 4H++ 2Cl-
(2)①溶液先变红再褪色
②a、b
(3)Cl2+ H2O
(4)
①答案一:生成1 mol HClO需消耗1 mol Cl2, HClO也有氧化性,1 mol HClO和1 mol Cl2均能将2 mol KI氧化成I2。
答案二:


②0.4V
知识点
29.二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。
(1)写出圆底烧瓶中反应的化学方程式 ( )。
(2)A中m管的作用是 ( );装置F的作用是 ( )。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是( ),C中应盛放的试剂是 ( ) 。
(4)E中若装有FeCl2溶液,反应的离子方程式为 ( );E中若装有淀粉碘化钾溶液,能观察到的实验现象是 ( )。
(5)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象,化学小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通人HCl气体,加热
b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸,加热
d.MnO2与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是( );实验c的目的是( ) 。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 ( )。
29.二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。
(1)写出圆底烧瓶中反应的化学方程式 。
(2)A中m管的作用是 ;装置F的作用是 。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是 ,C中应盛放的试剂是 。
(4)E中若装有FeCl2溶液,反应的离子方程式为 ;E中若装有淀粉碘化钾溶液,能观察到的实验现象是 。
(5)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象,化学小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通人HCl气体,加热
b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸,加热
d.MnO2与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是 ;实验c的目的是 。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 。
正确答案
28.氯气和二氧化硫是中学化学中常见的气体。某活动小组设计如下图所示装置图,分别研究氯气和二氧化硫的性质。
(1)下列装置常用于实验室制取气体,其中制取氯气选用的装置为( ),反应的离子方程式为 ( ),制取二氧化硫选用的装置为( );
(2)从左端分别通入氯气或二氧化硫时,装置B中观察到的现象是否相同( )(填“相同”或“不相同”);装置A反应后溶液均褪色,如何利用褪色后的溶液判断是何种气体使其褪色(写出简要的实验步骤) ( );
(3)装置F中盛放的溶液为( );若装置E中试剂为铁丝,则通入氯气
(4)当通入足量SO2完全反应后,向C中滴加淀粉溶液,无明显现象。该反应的离子方程式为 ( )。
正确答案
(1)甲 (1分);
(2)
(3)
(4)
解析
解析已在路上飞奔,马上就到!
知识点
29.某实验小组开展自主实验活动,学校实验室提供如下实验试剂和实验装置:实验试剂:A.浓盐酸 B.稀盐酸 C.浓硫酸 D.稀硫酸 E.MnO2粉末 F.
实验装置:
I.该小组拟制备Cl2和SO2两种气体,请为其选择适当的试剂和装置(用字母表示)并填入下表:
上述制备Cl2的反应的离子方程式是:( )。
II.该小组进一步探究Cl2和SO2两种气体的化学性质,设计如图装置。
首先将C中少量SO2通入B中,请书写SO2与过量NaOH稀溶液反应的化学方程式:(
);为验证此时溶液中大量存在的阴离子,该小组又设计了若干实验方案,其实验简要操作及结论是:( ) 。待SO2与过量NaOH稀溶液反应完全后再将过量Cl2通入B中充分反应,此时溶液中一定能大量存在的阴离子是:( )。(不考虑空气中的CO2的影响)
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析