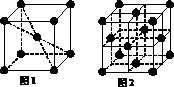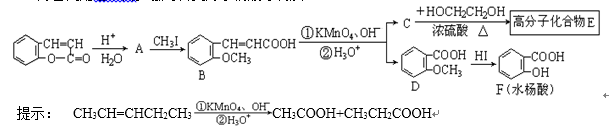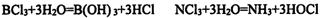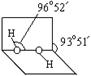- 有机物的推断
- 共316题
17.(9分)有机物A、B、C有如图所示转化关系,A的分子式为C3H4O2,A可与Br2的四氯化碳溶液发生加成反应,1 mol A能与1molNaHCO3溶液恰好完全反应。B所含元素种类与A相同,相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13%。试回答下列问题:
(1)A中所含官能团的名称为 ( )。
(2)B的分子式为( ),B的同系物D的相对
分子质量为60,则D可能的结构简式为( )。
(3)A与B反应生成C的化学方程式为( ),该反应属于( )反应。
(4)A、B的混合物共1mol,无论二者以何种比例混合,完全燃烧时下列量始终为定值的是( ) 。
a.消耗氧气的量 b.生成水的量 c.生成二氧化碳的量
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
考生从两道物理题、两道化学题中各任选一题作答。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
请考生在第18、19、20三题中任选一题做答,如果多做,则按所做的第一题计分。
18.(20分)
(I)多项选择题(6分)
莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料。鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机物的说法不正确的是( )。
A.两种酸都能与溴水反应
B.两种酸遇三氯化铁溶液都显紫色
C.鞣酸分子与莽草酸分子相比多了两个碳碳双键
D.等物质的量的两种酸与足量金属钠反应时,产生氢气的量相同
E.等物质的量的两种酸与足量氢氧化钠溶液反应时,消耗氢氧化钠的量相同
(II)(14分)
近年来,金属有机化合物的研究越来越引起化学家的重视,其研
究成果已应用于有机合成。
(一)二茂铁[Fe(C5H5)2]是铁的一种金属有机化合物,结构如图(E表示铁),其中氢原子的化学环境完全相同。但早期人们却错误地认为它的结构为:
核磁共振法能够区分这两种结构,在核磁共振氢谱中,正确的结构有 种峰,错误的结构有 种峰。
(二)Grignard试剂是镁的一种金属有机化合物,它的合成方法是:
生成的卤代烃基镁与具有羰基结构的化合物(醛、酮等)发生反应,再水解就能合成各种指定结构的醇:
现以2-丁烯和必要的无机物为原料合成3,4-二甲基-3-己醇,进而合成一种分子式为C10H16O4的具有六元环的物质J,合成线路如下:(提示:H的一氯代物只有3种)
请按要求填空:
(1)3,4-二甲基-3-己醇的结构简式是 ( ),它是图示中的哪种物质( )(填A~J的符号)。
(2)C+D→E的反应类型是______________,F→G的反应类型是________________。
(3)写出下列化学反应方程式(有机物请用结构简式表示):
A→B:( ) 。
(4)图示中的二元酸的名称是( );I和该二元酸除了能反应生成J外,还可以在一定条件下发生缩聚反应生成高聚物。试写出此高聚物的结构简式( )。
19.(20分)
(I)多项选择题(6分)
CH3+、CH3-、CH3-都是重要的有机反应中间体,有关它们的说法正确的是 ( )。
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个CH3-或一个CH3+和CH3-结合均可得到CH3CH3
(II)(14分)
锌是一种重要的金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置:( ) 周期,( )族,( )区。
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式( );葡萄糖分子中碳原子杂化方式有( ) 。
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于( )(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在左下图中表示[Zn(NH3)4]2+中Zn2+与N之间的化学键。
(4)右上图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为( );该化合物的晶体熔点比干冰高得多,原因是( )。
20.(20分)
(I)多项选择题(6分)
关于化工生产的下列叙述中,正确的是( ) 。
A.生产普通玻璃的原料是石灰石、石英、纯碱,在玻璃熔炉中发生复杂的物理化学变化
B.工业上合成氨没有采用更大的压强是从设备和动力要求方面考虑的
C.加热法只适用于软化暂时硬度的硬水
D.工业上采用电解熔融氯化铝生产金属铝
E.用高纯度焦炭与石英砂反应可制得纯度达到9个9的单晶硅材料
(II)(14分)
工业上制取硝酸铵的流程图如下,请回答下列问题:
(1)1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

(2)在合成氨的设备(合成塔)中,设置热交换器的目的是( );在合成硝酸的吸收塔中通入空气的目的是( )。
(3)生产硝酸的过程中常会产生一些氮的氧化物,可用如下两种方法处理:
请从绿色化学的角度分析两种方法的优劣:
(4)某化肥厂用NH3制备NH4NO3。已知:由NH3制NO的产率是96%、NO制HNO3的产率是92%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的( )%。
(5)硝酸铵是一种常用的氮肥,在贮存和使用该化肥时,把应注意的事项及理由填入下表。
18.(20分)
(I)多项选择题(6分)
莽草酸是一种合成治疗甲型H1N1流感药物达菲的原料。鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机物的说法不正确的是 。
正确答案
28、29题为物理题,第30、31题为化学题,考生从两道物理题、化学题中各任选一题作答。
30.[化学---物质结构与性质]
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)P、S、Cl三种元素中,第一电离能最小的是( ) 。
(2)PCl3和CH4中心原子的杂化类型相同,PCl3分子的空间构型是( ) 。
(3)钛原子的电子排布式为 ( ) 。在浓的TiCl3溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,将1 mol该物质溶于水,加入足量硝酸银溶液,立即产生1 mol氯化银沉淀,则该配合物阳离子的化学式为 ( ),形成该离子时提供孤电子对的分子或离子是( ) (填化学式)。
(4)铁元素在1183 K以下形成的晶体的基本结构
单元如图1所示,1183 K以上转变为图2所示结构的
基本结构单元。两种晶体的基本结构单元中的原子个
数之比为( ) 。
31.[化学---有机化学基础]
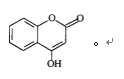
香豆素是广泛存在于植物中的一类芳香族化合物,具有抗菌和消炎作用。它的核心结构是芳香内酯,其结构简式为
(1)下列关于芳香内酯的叙述正确的是( ) 。
A.分子式为C9H8O2 B.可发生加聚反应
C.能与溴水发生反应 D.1mol芳香内酯最多能和5mol氢气发生加成反应
(2)写出芳香内酯在酸性条件下水解的化学方程式:( )。
(3)芳香内酯经下列步骤可转变为水杨酸等物质:
请回答下列问题:
① 指出D → F的反应类型为( ) 。
② 请写出反应C → E的化学方程式:( ) 。
③在一定条件下阿司匹林(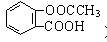
a.三氯化铁溶液 b.碳酸氢钠溶液 c.石蕊试液 d.氢氧化钠溶液
④水杨酸的同分异构体中含有酚羟基且属于酯类的共有3种,写出其中一种同分异构体的结构简式( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
第29、30题为物理题,第31、32题为化学题,考生从两道物理题、两道化学题中各任选一题作答。
31.〔化学选考1:物质结构与性质〕
VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为( ) 。
(2)N、P、As原子的第一电离能由大到小的顺序为( ) 。
(3)NH3的沸点比PH3高,原因是( );PO43-离子的立体构型为( ) 。
(4)PH3分子中P原子采用( )杂化。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3 酸性强的原因 ( )。
(6) CuCl2与氨水反应可形成配合物[Cu(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 ( ) 。
32.〔化学选考2:有机化学基础〕
有机物H是用于合成药物的中间体,G为合成涤纶。请根据下列转化关系回答有关问题:
已知以下信息:
①B能与碳酸氢钠溶液反应产生二氧化碳,其苯环上一氯代物只有2种
②G为C和F一定条件下1:1反应生成的高分子化合物

(-R1、-R2表示氢原子或烃基)
(1)A的化学名称为( );C中含氧官能团名称为( ) 。
(2)H的结构简式为( );A→D的反应类型为( )。
(3)写出C和F反应生成高分子化合物的化学方程式( )。
(4)同时符合下列条件的B的同分异构体共有( ) 种(不考虑立体异构);
①能发生银镜反应 ②含有苯环结构 ③能在碱性条件下水解
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
第29、30题为物理题,第31、32题为化学题,考生从两道物理题、两道化学题中各任选一题作答。
31.[化学——物质结构与性质]
由Cu、N、B等元素组成的新型材料有着广泛用途。
(1)基态Cu+的核外电子排布式为___________。高温下CuO能转化为Cu2O,试从原子结构角度解释其原因:_______________________。
(2)立方氮化硼是一种新型的超硬、耐磨、耐高温的结构材料,它属于___________晶体。
(3)化合物A(H3BNH3)是一种潜在的储氢材料,它可由六元环状化合物(HB=NH)3通过
反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3而制得。
①与上述化学方程式有关的叙述不平碜的是——(填标号)。
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
②1 mol(HB=NH)3分子中有_________mol
(4)在硼酸盐中,阴离子有链状、立体状等多种结构形式。图(a)是一种长链结构的硼酸根,则该硼酸根离子的化学符号为_________。图(b)是硼砂晶体中阴离子的立体状结构,
其中硼原子采取的杂化轨道类型有__________________。
32.[化学一有机化学基础]
甲苯是一种重要的化工原料。以甲苯为原料通过以下转化可得多种化工产品。
(1)写出指定物质的结构简式:A______________,M______________。
(2)C中苯环上的侧链所含官能团的名称是_______________________。
(3)E→F的反应类型是______________。
(4)关于B的说法正确的是__________(填标号)。
a.能发生银镜反应 b.遇FeCl3溶液发生显色反应
c.能发生消去反应 d.能与H2发生加成反应
(5)写出D→E反应的化学方程式:_______________________。
(6)写出符合下列条件的A的同分异构体的结构简式:__________________。
a.苯环上一氯代物只有3种
b.不能与新制氢氧化铜悬浊液反应

甲苯是一种重要的化工原料。以甲苯为原料通过以下转化可得多种化工产品。

(2)C中苯环上的侧链所含官能团的名称是_______________________。
(3)E→F的反应类型是______________。
(4)关于B的说法正确的是__________(填标号)。
a.能发生银镜反应 b.遇FeCl3溶液发生显色反应
c.能发生消去反应 d.能与H2发生加成反应
(5)写出D→E反应的化学方程式:_______________________。
(6)写出符合下列条件的A的同分异构体的结构简式:__________________。
a.苯环上一氯代物只有3种
b.不能与新制氢氧化铜悬浊液反应
正确答案
第29、30题为物理题,第31、32题为化学题,考生从两道物理题、两道化学题中各任选一题作答。
31.[化学——物质结构与性质]
物质结构决定物质的性质,物质性质反映了物质结构。
(1)BCl3、NCl3与水反应化学方程式如下:
分析上述反应,判断B、N、Cl三种元素的电负性由大到小的顺序是____。上述两个反应所含的微粒中,呈三角锥形的是( )(填化学式)
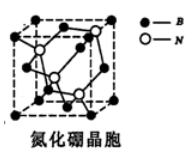
(2) BN是一种新型无机非金属材料,熔点很高、硬度很大,
晶胞结构如图。BN晶体中存在的作用力有____(填选项)。
A.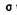
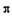
C.配位键 D.分子间作用力
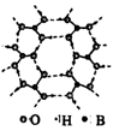
(3)B(OH)3的晶体结构如图所示。晶体中B原子的轨道杂化方
式是 ;B(OH)3可能具有的性质是( )(填选项)。
A.能溶于水 B.熔点很高
C.能形成
E.熔化状态下能导电
(4)还原铁粉可作为合成氨的触媒。基态Fe原子的核外有( )个,
未成对电子。从原子结构的角度分析,二价铁易被氧化为三价铁的
原因是____。
32.[化学——有机化学基础]
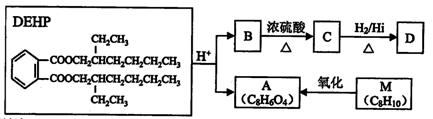
增塑剂(又称塑化剂)是工业上使用的塑料添加剂,但严禁用于食品。塑料增塑剂DEHP有如下的转化关系:
完成下列填空:
(1)用系统命名法命名D:( ),B分子中所含官能团的名称为 ( ),
(2)B—C的反应类型为( ) 。
(3)①关于A的下列说法正确的是 ( )(填选项)
A.属于芳香烃 B.能发生加成反应和取代反应
C.不能与碳酸钠溶液反应 D. M~A可用酸性高锰酸钾溶液做氧化剂
②A的一种同分异构体Q具有下列特征:
a.是苯的邻位二元取代物b.遇氯化铁溶液显紫色c.能与碳酸氢钠溶液反应
写出Q的结构简式为( )。
(4)写出DEHP在酸性介质中水解的化学反应方程式( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
第28、29题为物理题,第30、31题为为化学题,考生从两道物理题、两道化学题中各任选一题作答。
29.[化学—物质结构与性质] 目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。
(1)配合物Ni(CO)4常温为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于( )晶体;基态Ni原子的电子排布式为 ( )。
(3)配合物
用力是( )(填编号)。
A.氢键 B.离子键 C.范德华力 D.配位键
(3)很多不饱和有机物在Ni催化下可以与H2发生加成反应。
其中C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合
物。根据上图回答问题:
(1)B分子中的含氧官能团名称是_________________________;
写出一个同时符合下列四个条件的B的同分异构体的结构简式______________。
a.含苯环结构,取代基位于间位 b.能发生水解反应
c.能发生银镜反应 d.与FeCl3溶液发生显色反应。
(2)写出②的反应方程式:___________________________________________。
(3)写出D与浓硫酸在加热条件下发生的反应( )。
(4)A的结构筒式是______________________。
(5)若B分子(发生分子间脱水)发生酯化反应生成高分子的结构简式为( ) 。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
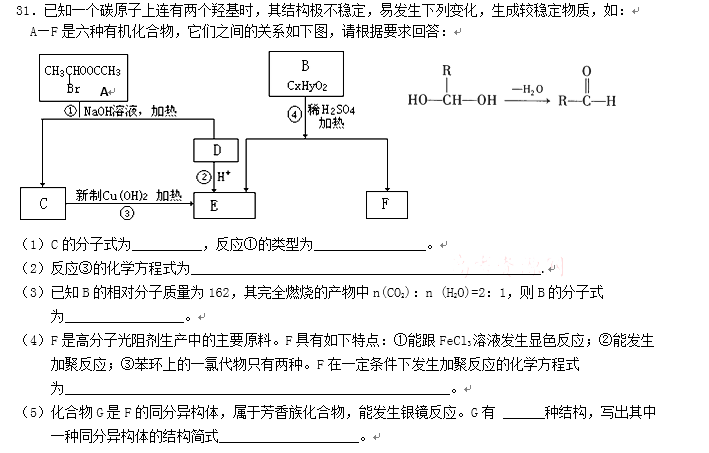
29.有机物A是一种镇痛解热药品,其结构简式为
(1)①、③反应类型分别是____________、________________;B和D的关系是 __________(选填“同种物质”、“同系物”或“同分异构体”)。
(2)写出反应②的化学方程式 ______________________ 。
(3)写出C与NaHCO3溶液反应的化学方程式___________________________。
(4)1 mol A在氢氧化钠溶液中水解,最多消耗氢氧化钠 ___________________ mol。
(5)能与FeCl3溶液发生显色反应,且属于酯类的C的同分异构体有多种,写出其中一种的结构简式__________________________。
正确答案
(1)水解反应、酯化反应(填取代反应亦可),同系物
(2)
(3)
(4)5 (5)
解析
解析已在路上飞奔,马上就到!
知识点
第30、31题为化学题,考生从两道化学题中任选一题作答。
[化学——物质结构与性质]
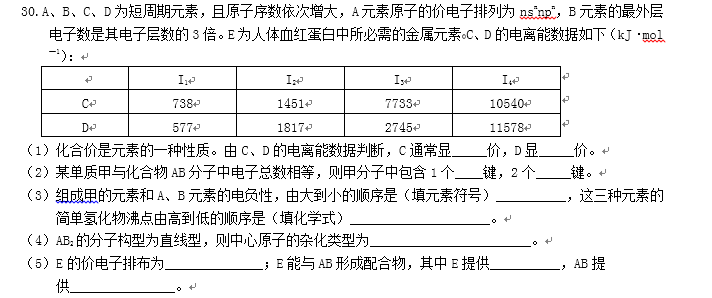
30、(1)在短周期主族元素中,氯及其相邻元素的电负性由大到小的顺序是( )(用元素符号表示)
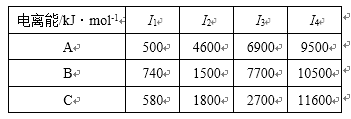
(2)A、B、C为同一短周期金属元素。依据下表数据分析,C元素在化合物中的主要化合价为 ;第二电离能(I2)B小于A的原因是( ) 。
(3)已知过氧化氢分子的空间结构如右图所示,分子中
氧原子采取( )杂化;通常情况下,H2O2与水任意比互溶的主要原因是( )。
(4)R是1~36号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:
R3+ 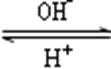
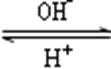
①基态R原子的价电子排布式为 ( ) 。
②[R(OH)4]-中存在的化学键是 ( ) 。
A.离子键 B.极性键 C.非极性键 D.配位键
31、[化学—有机化学基础]
某种医药中间体G,常用来制备抗凝血药,其结构简式是:
(1)G中含氧官能团是 ( ) 。
(2)下列关于G的说法正确的是( )。
a.能与溴单质反应 b.能与金属钠反应
c.1 molG最多能和3 mol氢气反应 d.分子式是C9H7O3
可通过下列路线合成此医药中间体:
请回答下列问题:
(3)A与银氨溶液反应有银镜生成,则A的结构简式是 ( );B→C的反应类型是( )。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:( )。
(5)E的结构简式是( );与D互为同分异构体且含苯环、属于酯类的有机物有( ) 种。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析