- 氧化还原反应方程式的配平
- 共44题
27.A:请回答
(1)H2O2的电子式___________。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由________________。
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式_____________。
(4)完成以下氧化还原反应的离子方程式:
( )MnO4-+( )C2O42-+______=( )Mn2++( )CO2↑+________
B:化合物甲和NaAlH4都是重要的还原剂。一定条件下金属钠和H2反应生成甲。甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的H2。
请推测并回答:
(1)甲的化学式__________。
(2)甲与AlCl3反应得到N
(3)NaAlH4与水发生氧化还原反应的化学方程式__________。
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式 ( )。
(5)某同学认为:用惰
判断该同学设想的制备和验纯方法的合理性并说明理由___________。
正确答案
A:
(1) 

(3) AgCl + Br-== AgBr + Cl-
(4) 2MnO4- + 5C2O42- + 16H+ == 2Mn2+ + 10CO2↑+ 8H2O
B:
(1)NaH (2) 4NaH+AlCl3==NaAlH4+3NaCl
(3) NaAlH4+2H2O==NaAlO2+4H2↑ (4) 3NaH+Fe2O3==2Fe+3NaOH
(5) 制备过程不合理,因为盐酸易挥发,H2中混有HCl,导致产物中有NaCl
验纯方法不合理,如果有Na残留,Na与水反应也产生H2;没有考虑混入的NaCl
解析
解析已在路上飞奔,马上就到!
知识点
二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂。
(1)氯化钠电解法是一种可靠的工业生产ClO2方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO等杂质。其次除杂操作时,往粗盐水中先加入过量的 (填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。经检测发现滤液中仍含有一定量的SO,其原因是 。【已知:Ksp(BaSO4)= 1.1 ×10—10 Ksp(BaCO3)= 5.1 ×10—9】
②该法工艺原理如图。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有 (填化学式),发生器中生成ClO2的化学方程式为 。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
(3)ClO2和Cl2均能将电镀废水中的CN—氧化为无毒的物质,自身被还原为Cl—。处理含CN—相同时的电镀废水,所需Cl2的物质的量是ClO2的 倍
正确答案
解析
(1)①BaCl2 BaSO4和BaCO3的Ksp相差不大,当溶液中存在大量CO32 -时,BaSO4(s)会部分转化为BaCO3(s)(或其它合理答案)
② H2、Cl2 2NaClO3 + 4HCl 
(2)1 C6H12O6 + 24 NaClO3 + 12H2SO4 
(3)2.5
知识点
用含有A1203、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ。向铝灰中加入过量稀H2SO4,过滤:
Ⅱ。向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ。加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ。加入MnSO4至紫红色消失,过滤;
Ⅴ。浓缩、结晶、分离,得到产品。
(1)H2S04溶解A1203的离子方程式是
(2)KMnO4 - 氧化Fe2+的离子方程式补充完整:
(3)已知:
生成氢氧化物沉淀的pH
根据表中数据解释步骤Ⅱ的目的:
(4)己知:一定条件下,MnO4 - 可与Mn2+反应生成MnO2,
① 向 Ⅲ 的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是 .
② Ⅳ 中加入MnS04的目的是
正确答案
答案:
(1)
(2)5、8H+、5、4H2O;
(3)将Fe2+氧化为Fe3+,调节pH值使铁完全沉淀;
(4)①、生成有黄绿色气体;
②、加入MnSO4,除去过量的MnO4-。
解析
(1)氧化铝与硫酸反应生成硫酸铝与水;
(2)反应中MnO4-→Mn2+,Fe2+→Fe3+, MnO4-系数为1,根据电子转移守恒可知, Fe2+系数为
(3)滤液中含有Fe2+,由表中数据可知,Fe(OH)2开始沉淀的pH大于Al(OH)3 完全沉淀的pH值,而Fe(OH)3完全沉淀的pH值小于Al(OH)3开始沉淀的pH值,pH值约为3时,Al3+、Fe2+不能沉淀,步骤Ⅱ是将Fe2+氧化为Fe3+,调节pH值使铁完全沉淀;
(4)①、MnO2能将HCl氧化为Cl2,若有黄绿色气体生成说明沉淀中存在MnO2;
②、Ⅲ 的上层液呈紫红色,MnO4-过量,加入MnSO4,除去过量的MnO4-。
知识点
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式________。
(2)已知:Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O→Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是______。
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3→Na2S4O6+2NaI
配平方程式①,标出电子转移的方向和数目。
(4)实验中,准确称量SeO2样品0.1500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的质量分数为___。
正确答案
(1)Se+2HNO3(浓)→H2SeO3+NO↑+NO2↑ ;
(2)H2SO4(浓)>SeO2>SO2
(3) 
(4)0.925
解析
利用题中信息可知Se与浓HNO3反应,Se被氧化为+4价的H2SeO3,HNO3还原为NO与NO2,利用电子守恒和限定条件(生成NO与NO2的物质的量之比为1:1,即二者计量系数比为1:1)可得方程式。利用氧化性:氧化剂>氧化产物,结合题中方程式可知氧化性:H2SO4(浓)>SeO2>SO2。在反应①I-失电子,转移SeO2,+4价Se得到电子还原为单质Se。利用前面配平的方程式可得关系式:SeO2~2I2~4Na2S2O3,故样品中SeO2的质量分数为:[111g·mol-1×(0.2000mol/L×0.025L)/4]/0.1500g=0.925。
知识点
部分弱酸的电离平衡常数如下表:
(1)在温度相同时,各弱酸的Ki值与酸性的相对强弱的关系为:________________________。
(2)下列离子方程式正确的是
A,2ClO- + H2O + CO2 → 2HClO + CO32-
B,2HCOOH + CO32- → 2HCOO- + H2O + CO2↑
C,H2SO3 + 2HCOO- → 2HCOOH + SO32-
D,Cl2 + H2O+2CO32- → 2HCO3- + Cl- + ClO-
(3)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为 。
亚硒酸(H2SeO3)也是一种二元弱酸,常温下是一种无色固体,易溶于水,有较强的氧化性。
(4)往亚硒酸溶液中不断通入SO2 会产生红褐色单质,写出该反应的化学方程式: 。
(5)将亚硒酸与30%的H2O2加热可制得硒酸(H2SeO4),反应方程式如下:
H2SeO3 + H2O2 → H2SeO4+H2O,下列说法中正确的是
A,H2O2既是氧化剂又是还原剂
B,H2O 既不是氧化产物又不是还原产物
C,H2SeO4既是氧化产物又是还原产物
D,氧化性:H2SeO3>H2SeO4
碲酸(H6TeO6)是一种很弱的酸,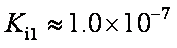
HI+ H6TeO6
(6)若反应中生成的TeO2与Te的物质的量之比为
正确答案
(1)Ki值越大,酸性越强
(2)BD
(3)C(HCOO—)>C(Na+)>C(H+)>C(OH—)
(4)H2SeO3 + 2SO2 +H2O → Se ↓+ 2H2SO4
(5)C
(6)8HI + 2H6TeO6 → TeO2 + Te +4I2 + 10H2O
解析
略
知识点
扫码查看完整答案与解析