- 化学实验
- 共767题
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数。
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。实验中加热至恒重的目的是________。
(2)方案二:按下图装置进行实验。并回答以下问题。
① 实验前先________。分液漏斗中应该装________(“盐酸”或“硫酸”)。D装置的作用是________。
② 实验中除称量样品质量外,还需称________装置前后质量的变化。
③ 根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显缺陷,该缺陷是________。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤洗涤,干燥沉淀,称量固体质量,计算:
① 过滤操作中,除了烧杯,漏斗外,还用到的玻璃仪器有________。
② 实验中判断沉淀是否完全的方法是________。
③ 已知称得样品21.2g,干燥的沉淀质量为19.7g,则样品中碳酸钠的质量分数为________。
正确答案
(1)保证NaHCO3全部分解
(2)①检查装置的气密性;硫酸;防止空气中水蒸气、CO2进入C管被吸收 ②C ③需设计一个将A、B中的CO2全部吹入C中的装置
(3)①玻璃棒 ②取少量上层清液,滴加少量BaCl2溶液,如无白色沉淀说明沉淀完全 ③50%
解析
略。
知识点
2013年6月11日,神舟十号由长征二号F改进型运载火箭成功发射,其后完成了与天宫一号的对接任务,实现了中国航天史上首次太空授课。下列操作在太空舱可以实现的是
正确答案
解析
略
知识点
用下列各组仪器或装置,不能达到实验目的的是
正确答案
解析
略
知识点
本题包括ab两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按a题评分。
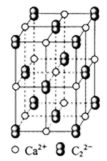
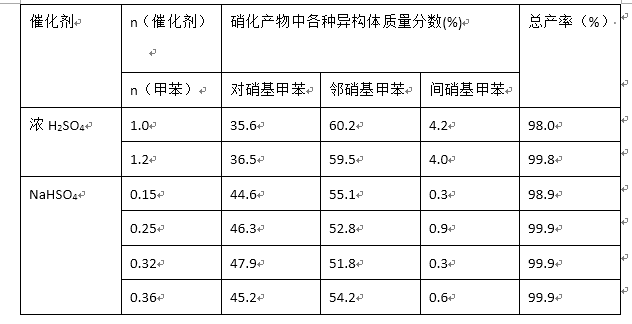
a乙炔是

(1)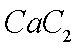

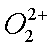
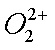
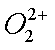

(2)将乙炔通入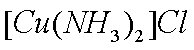
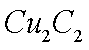
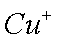
(3)乙炔与氢氰酸反应可得丙烯腈
(4)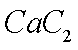


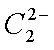
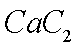

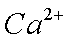

b对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。
一种新的制备对硝基
(1)上述实验中过滤的目的是 。
(2)滤液在分液漏斗中洗涤静置后,有机层处于 层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有 。
(3)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
① NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是 。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有_ 、 。
正确答案
a、(1)
(2)1s2 2s2 2p6 3s2 3p6 3d10
(3)sp2杂化、sp3 杂化 3
(4)4
b、(1)回收NaHSO4
(2)下 分液漏斗上口塞子未打开
(3)①0.32
②甲苯硝化主要得到对硝基甲苯和邻硝基甲苯
③在硝化产物中对硝基甲苯比例提高 催化剂用量少且能循环使用
解析
略
知识点
用图示装置(试剂任选)能完成下列实验的是
正确答案
解析
略
知识点
11.下列对有关实验的说法正确的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
10.下列实验操作或对实验事实的描述中正确的说法共有( )
①燃着的酒精灯不慎碰翻失火,可立即用湿布盖灭
②滴定用的锥形瓶和滴定管都要用所盛溶液润洗
③分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
④配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸
⑤不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
⑥用托盘天平称量时,所称药品均可放在纸上,并置于天平的左盘
⑦测定溶液的pH时,可用洁净、干燥的玻璃棒蘸取溶液,滴在pH试纸上,再与标准比色卡比较
⑧浓硝酸与浓盐酸均易挥发,故均应保存在棕色试剂瓶中,并置于阴凉处
⑨配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液的浓度偏高
⑩可以用酸式滴定管量取20.00mL0.1000mol·L-1KMnO4溶液
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.下列说法不正确的是()
①用浓硝酸清洗做过银镜反应的试管 ②用氢氧化钠溶液清洗盛过苯酚的试管 ③若不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 ④若不慎将硫酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 ⑤配制硫酸溶液时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸 ⑥用蒸馏水润湿的pH试纸,测定某溶液的pH ⑦钠着火,用泡沫灭火器扑灭
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
11.下列说法不正确的是()
①用浓硝酸清洗做过银镜反应的试管 ②用氢氧化钠溶液清洗盛过苯酚的试管 ③若不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 ④若不慎将硫酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 ⑤配制硫酸溶液时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸 ⑥用蒸馏水润湿的pH试纸,测定某溶液的pH ⑦钠着火,用泡沫灭火器扑灭
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
6.生活中下列处理方法没有科学道理的是( )
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
5.下列有关实验的叙述正确的是
正确答案
解析
A.过滤时,不可用玻璃棒搅拌漏斗中的液体,防止弄破滤纸,错误;
B.用湿润的pH试纸测溶液的pH,酸溶液测量值变大,碱溶液测量值变小,错误;
C.酸碱滴定管、容量瓶、分液漏斗是带有旋塞和瓶塞的仪器,使用前需要检查是否漏水,正确;
D.酸碱滴定实验中,用待滴定溶液润洗锥形瓶会使得标准液消耗过多,增大实验误差,错误;故选C。
考查方向
解题思路
A.过滤时,不可用玻璃棒搅拌漏斗中的液体,防止弄破滤纸;
B.用湿润的pH试纸测溶液的pH,酸溶液测量值变大,碱溶液测量值变小;
C.酸碱滴定管、容量瓶、分液漏斗是带有旋塞和瓶塞的仪器,使用前需要检查是否漏水;
D.酸碱滴定实验中,用待滴定溶液润洗锥形瓶会使得标准液消耗过多,增大实验误差;
易错点
酸碱滴定实验中,用待滴定溶液润洗锥形瓶会使得标准液消耗过多,增大实验误差;
知识点
9.对中学化学实验:①中和热的测定、②中和滴定、③硝基苯的制取、④乙酸乙酯的制取,叙述正确的是( )
正确答案
解析
A.中和热的测定不需要用指示剂,故A错误;B.实验③④都需要使用浓硫酸作催化剂,故B正确;C.中和热的测定实验需用温度计,但不用水浴加热;硝基苯的制取必须用温度计且水浴加热;乙酸乙酯的制取既不用温度计也不用水浴加热。故C错误;D.乙酸乙酯的制取实验不需要烧杯,故D错误。
考查方向
解题思路
中和滴定需在指示剂作用下进行,中和热的测定需要保温隔热避免热量的损失,硝基苯的制取需在浓硫酸催化作用下进行,需要用温度计测量水浴的温度,并控制水浴温度为50℃~60℃,乙酸乙酯的制备在加热条件下进行,不用水浴,需要浓硫酸作催化剂,也不使用温度计。
易错点
硝基苯的制取实验中涉及到的仪器。
知识点
10.下列操作或装置能达到实验目的的是
正确答案
解析
A.配制溶液不能用容量瓶来溶解固体物质,故不能达到试验目的
B.HCl要和饱和碳酸氢钠溶液反应产生二氧化碳气体,故不能达到试验目的
C.正确
D. 电石与水反应有硫化氢杂质生成,具有还原性,使酸性高锰酸钾溶液褪色,故不能达到试验目的。
考查方向
解题思路
本题考查化学实验方案的评价,明确反应的条件和发生的副反应是解题的关键。
易错点
1、电石与水反应有硫化氢杂质生成
2、吸氧腐蚀
知识点
利用右图实验装置,能得出相应实验结论的是
正确答案
解析
略
知识点
27.工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用生产ZnSO4·6H2O晶体,其工艺流程如下,有关氢氧化物沉淀时的pH如下表。
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪有( ) 。
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是( )。为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为( )。为控制上述PH范围可选择加入的试剂或药品是( )。
A.ZnO
B.氨水
C.固体NaOH
D.ZnCO3
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是( )。“操作A”的名称是 ( )。
(4)常温下,已知Ksp〔Cu(OH)2〕=2×10-20,某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于( )。
正确答案
解析
解析已在路上飞奔,马上就到!
知识点
扫码查看完整答案与解析